
题目列表(包括答案和解析)
3.分类方法在化学学科发展中起到了非常重要的作用。下列分类标准合理的是
① 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
② 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③ 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④ 根据反应中的热效应将化学反应分为放热反应和吸热反应
⑤ 根据碱在水溶液中的溶解性将碱分为强碱和弱碱
⑥ 根据和水反应的产物将氧化物分为酸性、碱性或两性氧化物
A.①③⑤ B.②④ C.①②④ D.②④⑥
2.正确掌握好化学用语是学好化学的基础,下列有关表述正确的是
A.H2、D2、T2互为同素异形体
B.氨气分子构型为正四面体形
C.NH4Cl的电子式为:
D.S2-的结构示意图为: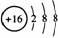
1.能源危机是制约现代社会发展的严重问题,开发和利用新能源是中国立足自身解决能源困扰的重要举措之一。背景材料:①2005国际油价飙升,新型纳米金属燃料面世;②2006年1月1日,“苏北五市”全面推广使用乙醇汽油;③到2010年,江苏省将打造成为全国最重要的太阳能产业基地;④生物柴油是以油脂为原料,通过水解、酯化所得高级脂肪酸甲酯。下列说法正确的是
A.乙醇汽油的推广使用大大降低了国际市场的油料价格
B.用油料作物生产的生物柴油成分与从石油中提取的柴油成分相同,生物柴油燃烧不会产生二氧化碳,是一种清洁能源
C.太阳能能量大,无污染,是一种不可再生能源
D.纳米金属燃料表面积大因而活性高,易引发,能量释放快,是一种清洁能源
13.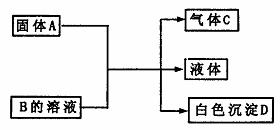 A、B、C、D、均为中学化学常见的物质,它们间的反应关系如下图所示。
A、B、C、D、均为中学化学常见的物质,它们间的反应关系如下图所示。
(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式 。有关反应的化学方程式为 。
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液。
①A是NaHCO3时,该反应的离子方程式为: 。
②A是一种淡黄色固体,且A与B以物质的量之比为2:1相混合时,推知B的化学式为 。
(3)若A是碳化钙(CaC2),A与B的溶液反应时只生成气体C、CaCO3和水;C的燃烧热为1300kJ·mol-1,则B的化学式为 ;C燃烧的热化学方程式为
12.A、B、C、D均为短周期主族元素,A、C、D在不同周期,A和C同主族,B、C同周期,A、B、C三种元素的原子序数之和为37,且B元素的最外层电子数与其电子层数相同,则:
(1)D元素的名称为 。
(2)写出元素A、D形成的化合物D2A的电子式 ,其熔点比D2C的熔点 (用“高”或“低”填写),理由是 。
(3)A、B、C三种元素所形成的常见化合物溶于水呈酸性,用离子方程式表示其原因 。
(4)A、B、C、D四种元素的原子半径从小到大的顺序为(用元素符号表示)
11. A、B、C、D、E均为短周期元素,且原子序数逐渐增大。A、D同主族,A与B的质子数之和等于C的质子数,A+离子与C2-离子的核外电子数之和等于D+离子的核外电子数,B原子与D+离子的核外电子数之和等于 E原子的核外电子数。
(1)A、B、C、D、E的元素符号分别为 。
(2)D、E元素可组成化合物甲,电解甲的水溶液时,反应的离子方程式为 ;A、C元素可组成原子个数比为1:1的化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为 。
(3)A、B、C、E中的任意三种元素可组成多种化合物,其中既含离了键又含共价键,且水溶液呈酸性的化合物有(写出两种化合物) 。
(4)A、C、D、E中的任意三种元素可组成多种化合物,其中溶于水时能抑制水电离的化合物有(各写一种不同类别的化合物) ,它们能抑制水电离的理由是 。
10.同周期中A、B、C、D、E、F为原子序数依次增大的短周期元素。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。请回答下列问题:
(1)根据以上条件一定能判断出的元素有几种,请在下列写出相对应的元素符号:
A B C D E F 。
(2)已知 D单质在 F单质中燃烧可能生成两种化合物,请分别写出生成两种化合物的化学方程式: ; 。
(3)若1 mol F的最高价氧化物水化物与C的最高价氧化物水化物恰好完全反应,则等物质的量的C的最高价氧化物与A的最高价氧化物水化物反应消耗 mol A的最高价氧化物水化物。
9. A、B、C是短周期主族元素,且原子序数依次增大,A元素的原子最外层电子数是次外层电子数的3倍,B和C的原子序数之和是A的原子序数的3倍,B和C形成的离子具有相同的电子层结构.试回答下列问题:
(1)C离子的结构示意图是___________________;由A和B形成的含有非极性键的离子化合物的电子式是___________________;
(2)B离子半径(填“<”或“>”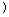 ________C离子半径,B和C元素最高价氧化物的水化物之间反应的离子方程式为______________________________________;
________C离子半径,B和C元素最高价氧化物的水化物之间反应的离子方程式为______________________________________;
(3)化合物X由元素A、B、C组成,写出X的溶液与过量盐酸反应的离子方程式:
_____________________________________.
8. A.B.C.D.E、F是中学化学中常见的6种物质,它们在一定条件下可发生如下反应: ①A+B C+D ②B+E
C+D ②B+E D+F
③C+E
D+F
③C+E A+F
A+F
(1)若A、D、E为卤素单质,反应①、②、③均为在水溶液中进行的置换反应,则A、D、E与氢气化合由难到易的顺序为____________,A跟B反应的离子方程式是__________________________。
(2)常温下,若D是液态金属,A是红色固体单质,反应①、②、③也都在水溶液中进行,E是短周期元素的单质,则E可能是_______________,A跟B反应离子方程式是_____ __________________。
(3)若A、D、E是单质,C是有磁性的固体,F是无色、无味、有毒的气体,则A在周期表中的位置是_____________ ,A和B反应的化学方程式是_____ ____,B和E反应的化学方程式是_ ________________
7.现有A、B、C、D四种短周期元素,已知A、B同主族,B、C、D同周期,A、B的原子序数之和等于C、D的原子序数之和,C的单质能分别跟B和D的最高价氧化物的水化物反应。请回答:
(1)B和C的元素符号分别为______________;
(2)上述四种元素的原子半径由大到小的顺序(用元素符号表示)为_____________;
(3)D单质在A单质中燃烧的产物与二氧化碳反应的化学方程式为___________;
(4)B单质能跟D的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种盐的水溶液均呈碱性,该氧化还原反应的离子方程式为________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com