
题目列表(包括答案和解析)
6、 用NA表示阿伏加德罗常数,下列说法中正确的是( )
用NA表示阿伏加德罗常数,下列说法中正确的是( )
A.1L 1 mol·L-1的醋酸溶液中离子总数为2 NA
B.0.05 mol碳酸钠晶体中含离子总数大于0.15NA
C.0.4mol NaCl晶体中含有右图所示的结构单元的
数目为0.1 NA
D.标准状况下,22.4L CH3Cl和CHCl3的混合物
所含有分子数目为NA
5、下列排列顺序错误的是( )
A.金属性Rb>K>Mg>Al B.常压下沸点:H2O<H2S<H2Se
C.稳定性AsH3<PH3<H2S<HF D.原子半径Na>P>O>F
4、已知反应:①101kPa时,2C(s)+O2(g)=2CO (g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是( )
A.碳的燃烧热大于110.5kJ/mol
B.碳的燃烧热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
3、无论是传统的还是新型的无机非金属材料,硅元素都占有非常重要的地位。由于
硅在太阳能发电中的重要作用,有些科学家称硅是“二十一世纪 的能源”,下列关
于硅的说法错误的是( )
A 二氧化硅可用于做光导纤维
B 高纯度的硅是制半导体的重要材料
C 水泥、玻璃、陶瓷都是传统的硅酸盐工业产品
D 自然界中硅元素的含量居各元素的第一位
2、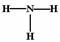 氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
A.乙烯的结构式CH2CH2 B.NH3的结构式为:

C.HCl的电子式为 D.热稳定性:H2S>HF
1、在2006年两会期间,许多代表认为环境污染已经成为当前中国发展中的一个重大问题。在一些生产和生活中产生的某气体在近地面空气中浓度稍大时是一种污染物,而在高空却对人类有保护作用,该气体是 ( )
A.NO B.O3 C .SO2 D. 氟氯烃
25.(10分)硫酸工业生产应考虑综合经济效益。
(1)工业生产硫酸的原料气成分(体积分数)为:SO2 7%,O2 11%,N2 82%。
 压强及温度对SO2转化率的影响如下:
压强及温度对SO2转化率的影响如下:
|
|
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
工业上,二氧化硫催化氧化过程采用的是常压而不是高压,主要原因是
____________________________________________________________________。
分析上表数据可知,二氧化硫的催化氧化是放热反应,理由是____________________________________________________________________。
(2)据测算,接触法制硫酸过程中,每生产1 t 98%的硫酸需消耗3.60×105 kJ能量。
若反应:2SO2(g)+O2(g)  2SO3(g),ΔH=-196.6 kJ /mol放出的热量完全被利用,则每生产1 t 98%的硫酸可为外界提供_____________kJ能量(不考虑其他过程释放的能量)。
2SO3(g),ΔH=-196.6 kJ /mol放出的热量完全被利用,则每生产1 t 98%的硫酸可为外界提供_____________kJ能量(不考虑其他过程释放的能量)。
(3)依据题给数据计算:在500℃0.1MPa条件下,二氧化硫的催化氧化达到平衡时,各种气体的体积比V(SO2)∶V(SO3)∶V(O2)∶V(N2)= ∶ ∶ ∶82
(结果保留两位有效数字)。
24.(9分)能源是人类社会发展进步的物质基础。在当代,能源同信息、材料一起构成了现代文明的三大支柱。
(1)为了降低汽车尾气对大气的污染,江苏有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。请写出表示甲醇燃烧热的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.1000g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL 0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点。
已知:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②求此工业甲醇中CH3OH的质量分数。
23.(10分)
将化学知识的系统化,有助于对化学问题的进一步认识。请你参与下列关于化学反应的讨论。
问题1:化学变化过程中的平衡状态可以通过改变反应条件而发生变化。对电离平衡、水解平衡、化学平衡等各种平衡移动的方向与外界条件变化的关系请你运用一句话进行总结:_________________________________________________________。
问题2:不同化学反应进行的快慢和程度千差万别。在复杂的反应中,要考虑反应的先后顺序。已知NH4++AlO2-+H2O=Al(OH)3↓+NH3·H2O,向含有等物质的量的NH4+、Al3+、H+、混合溶液中,慢慢滴加NaOH溶液,直至过量,并不断搅拌,依次发生了数个离子反应;其中
(1)第二个离子反应的离子方程式是________________________________
(2)最后一个离子反应的离子方程式是______________________________
问题3:化学反应的复杂性决定了反应方程式计量数的复杂性。对下列化学反应:
8KMnO4+15Kl+17H2SO4→8MnSO4+5I2+5KIO3+9 K2SO4+17H2O
如果该反应方程式中I2和KIO3的系数不是5,可能的配平系数还有许多组。请你再写出一个配平的该反应的化学方程式:________________________________________。
问题4:1840年盖斯根据一系列实验事实得出规律:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。”这是在各反应于相同条件下完成时的有关反应热的重要规律。已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(金刚石、s)+O2(g)=CO2(g):△H=-395.41kJ/mol,C(石墨、s)+O2(g)=CO2(g):△H=-393.51kJ/mol,则金刚石转化石墨时的热化学方程式为:______________
2l.(8分)
锌一锰干电池是普遍使用的化学电池,如图是干电池的基本构造图,其中含有MnO2、NH4Cl、ZnCl2等糊状物。
(1)干电池工作时正极上的反应是NH4++e-=NH3+ H2,则负极
H2,则负极 上的电极反应式是_____,MnO2的作用是除去正极上的产物,本身生成Mn2O3,该反应的化学方程式是__________。
上的电极反应式是_____,MnO2的作用是除去正极上的产物,本身生成Mn2O3,该反应的化学方程式是__________。
(2)干电池用久了就会变软,其原因是_____________________。
(3)将1L含有0.4mol CuSO4和0.2mol NaCl的水溶液用惰性电极电解一段时间后,在一个电极上得到0.1molCu,另一电极上析出气体(在标准状况下)的体积是_______升。
22.(8分)在20L恒容的密闭容器中,加入3molSO3(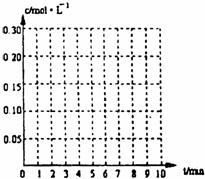 g)和lmo1氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.09mol·L-1,当反应到8min时,反应到达平衡,此时三氧化硫浓度c(SO3):a mol·L-1。
g)和lmo1氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.09mol·L-1,当反应到8min时,反应到达平衡,此时三氧化硫浓度c(SO3):a mol·L-1。
(1)0min-4min内生成O2平均速率v(O2)=__________mol·L-1min-1
(2)达到平衡时C(O2)=C(SO2),则a=___________mol·L-1,在下列坐标系中作出0min-8min及之后SO2、O2、SO3浓度随时间变化曲线.
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于amol·L-1的是________________
|
|
A |
B |
C |
D |
|
SO3 |
1mol |
3mol |
3mol |
0mol |
|
SO2 |
2mol |
1.5mol |
0mol |
6mol |
|
O2 |
2mol |
1mol |
0mol |
5mol |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com