
题目列表(包括答案和解析)
5.NA代表阿伏加德罗常数的值,下列说法正确的是
A.1 mol HNO3见光分解,转移电子数4NA
B.28 g晶体硅中含有Si-Si键的数目为2NA
C.100 mL 0.5 mol/L的(NH4)2SO4溶液中,含有0.1NA个NH4+
D.Cu与浓硝酸产生的22.4 L(标准状况)气体中含原子数为3NA
4.在体积不变的密闭容器中进行的反应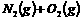
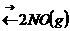 ,能说明该反应一定处于平衡状态的是
,能说明该反应一定处于平衡状态的是
A、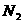 的浓度不再变化
的浓度不再变化
B、容器内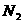 和
和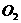 的浓度相等
的浓度相等
C、单位时间内每消耗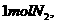 同时消耗
同时消耗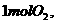
D、单位时间内每生成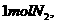 同时消耗
同时消耗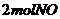
3.室温时,将x mL pH=a 的稀NaOH溶液与ymL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是:
A、若x=y,且a+b=14,则pH>7
B、若10x=y,且a+b=13,则pH=7
C、若ax=by,且a+b=13,则pH=7 D、若x=10y,且a+b=14,则pH>7( )
2.下图中每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化(外压为1atm),其中a点代表的是:( )
A、 H2Se B、HBr C、 AsH3 D、 GeH4
1.背景材料:①2004年夏季,特氟隆不粘锅事件引起公众关注;②2004年冬季,诺贝尔化学奖授予研究蛋白质的科学家;③2005年初春,广东大部分地区进行人工降雨;④2005年春末,某高速公路发生液氯运输车翻倒泄露事故。下列相应说法正确的是:( )
A、特氟隆(聚四氟乙烯)的单体是氟利昂
B、蛋白质是由氨基酸形成的不可降解的高分子化合物,其水溶液有丁达尔现象
C、AgI和干冰都可用于人工降雨
 D、附近人员应迅速远离液氯泄露地点,并顺风往安全区域疏散
D、附近人员应迅速远离液氯泄露地点,并顺风往安全区域疏散
12.下列物质间在一定条件下可实现图中所示的一系列变化。其中固体W的焰色反应呈紫色,A是一切生物都不能缺少的气体。
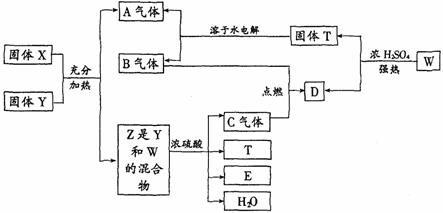
请回答:
(1)判断X、Y各是什么物质?X__________Y__________。
(2)写出有关反应的化学方程式:
①Z+H2SO4 (浓)→C
②W+H2SO4 (浓)→D+T
11.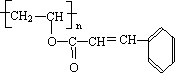 (16分)感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料。其结构简式为:
(16分)感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料。其结构简式为:
(1)在一定条件下,该高聚物可发生的反应有 (填代号)
① 加成反应 ② 氧化反应 ③ 消去反应 ④ 酯化反应 ⑤ 卤代反应
(2)该高聚物在催化剂的作用下,水解后的产物中有一种相对分子质量较小的R,其分子式为 。
(3)写出R在一定条件下与乙醇反应的化学方程式: 。
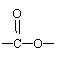
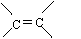
(4)R的同分异构体有多种,其中含有苯环、 和 ,且苯环上有两个对位取代基的结构简式是 。
10.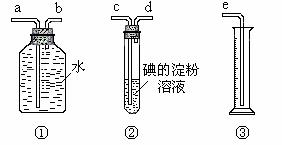 (12分).某化学兴趣小组模拟测定工业原料气SO2、N2、O2混合气体中SO2含量,选用了下列简易实验装置:
(12分).某化学兴趣小组模拟测定工业原料气SO2、N2、O2混合气体中SO2含量,选用了下列简易实验装置:
(1)若原料气从左向右流向时,上述装置组装连接的顺序是:
原料气→ (填a、b、c、d、e)。
(2)装置②中发生反应的离子方程式为 ;当装置②中出现 现象时,立即停止通气。若此时没有及时停止通气,则测定的SO2含量
(选填“偏高”、“偏低”或“不受影响”)。
(3)你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是 (填编号)
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
(4)若碘溶液的浓度为0.05mol/L、体积为20mL,收集到的N2和O2的体积为297.6mL(已折算为标准状况的体积)。SO2的体积分数为 。
9.X、Y、Z、W四种短周期元素,若X的阳离子与Y的阴离子具有相同的电子层结构,W的阳离子氧化性强于等电荷的X阳离子的氧化性,Z的阴离子半径大于等电荷的Y的阴离子半径,且Z离子所带电荷数的绝对值是W离子的两倍,W离子与Z离子的电子层相差两层。试推断这四种元素X_______,Y_________,Z_________,W_______。
8.M层电子数是K层的3倍。下列判断错误的是 ( )
A、R元素处于第三周期 族
B、R元素的最低化合价为-2价
族
B、R元素的最低化合价为-2价
C、R原子的核外共有14个电子 D、R元素为非金属元素
第Ⅱ卷(满分60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com