
题目列表(包括答案和解析)
23.(7分) 850℃时反应A(g)+B(g) C(g)+D(g) ΔH<0,K=l。t℃时,在一定体积的容器中,通入一定量的A和B发生化学反应,各物质浓度随时间变化如下表:
C(g)+D(g) ΔH<0,K=l。t℃时,在一定体积的容器中,通入一定量的A和B发生化学反应,各物质浓度随时间变化如下表:
t℃时物质的浓度(mol·L-1)变化
|
时间/min |
A |
B |
C |
D |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
0.100 |
0.200 |
0.100 |
0.100 |
|
4 |
0.100 |
0.200 |
0.100 |
0.100 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
(1)计算t℃该化学反应的平衡常数:
(2)t℃ 850℃(填大于、小于或等于)。判断依据是
(3)反应在4min-5min之间,平衡 (填“向左”、“向右”或“不”)移动,可能的原因是
a.增加A的浓度 b.增加D的浓度 c.加压 d.使用催化剂
(4)某温度下反应C(g)+D(g)  A(g)+B(g)的平衡浓度符合c(C)·c(D)=2c(A)·c(B),则此时的温度
8500C(填大于、小于或等于)
A(g)+B(g)的平衡浓度符合c(C)·c(D)=2c(A)·c(B),则此时的温度
8500C(填大于、小于或等于)
22.(8分)下列框图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。已知:A是固体单质,Y是一种无色液体,既可作氧化剂,又可作还原剂,B、X、秒为气体单质,D属于可溶于水的强电解质,一个D分子含有18个电子。
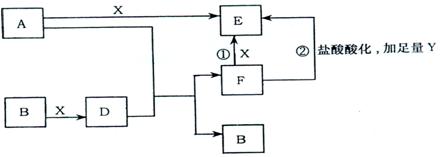
(1)化学式:B为 ,F为 。
(2)写出反应①和②的化学方程式
。
(3)用离子方程式表示E物质能用于净水的原理
21.(8分)现有第二、三周期元素性质的部分数据,其中X数值表示不同元素的原子吸引电子的能力大小,若X值越大,元素的非金属性越强,金属性越弱。X值相对较大的元素在所形成的分子中化合价为负价:
|
编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|
|
X |
3.44 |
2.55 |
0.98 |
2.04 |
2.19 |
3.16 |
0.93 |
3.04 |
1.61 |
|
|
常见化合价 |
最高价 |
|
+4 |
+1 |
+3 |
|
|
+1 |
|
+3 |
|
最低价 |
-2 |
|
|
|
-3 |
-1 |
|
-3 |
|
(1)画出元素⑥的离子结构示意图
(2)元素⑦和元素⑨的氢氧化物反应的离子方程式为
(3)“神舟五号”飞船内采用一种化合物来吸收航天员呼出的CO:,你认为该物质
应该是由上表中的 (填序号)元素组成的,用电子式表示仅由以上元素形成另外一种化合物的过程
(4)将8g元素②的单质在足量的元素①的单质中燃烧,所得气体通入1Llm01·L-1。
的NaOH溶液中,完全吸收后,溶液中离子浓度由大到小的顺序
20.(13分)某课外活动小组利用以下装置探究氯气与氨气之间的反应。其中 A 、F 分别为氨气和氯气的发生装置,C为纯净的氯气于氨气反应的装置。

请回答下列问题:
(1)装置F中发生反应的离子方程式 。
(2)装置A中烧瓶内固体可以选用 (选填以下选项的代号)。
A.碱石灰 B.生石灰 C.二氧化硅
D.五氧化二磷 E.烧碱 F.氢氧化钠和氯化铵的混合物
(3)上图A-F是按正确实验装置顺序排列的。虚线框内应添加必要的除杂装置,
请从上图的备选装置中选择,并将编号填人下列空格:B
D ,E
(4)氯气和氨气在常温下混合就会反应生成氯化铵和氮气,写出反应的化学方程式
。装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案检验其中的NH4+
(5)若从装置C的G处逸出的尾气只含有N2和少量Cl2,应如何处理才能不污染
环境?
19.(4分)下列有关实验或做法中,正确的是(填序号,错选倒扣分)_______________。
A.配制480mL 1.0mol·L-1NaOH溶液时,需称取NaOH固体的质量为20.0g
B.用分液的方法分离苯和水的混合物
C.同温同压下,等质量的硫在足量的氧气中比在足量的空气中燃烧放出的热量多
D.将mgCO和H2的混合气体完全燃烧后通过过量的Na2O2固体(气体充分反应),固体增重mg
E.排空气法收集一瓶干燥的氨气做喷泉实验,最后液体充满整个容器
F.试纸在使用前需用蒸馏水湿润,然后进行相应试验
18.将5.6gCu、Mg合金投入到一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下混合气体VL(HNO3被还原为NO和NO2);若向反应后的溶液中加入足量氢氧化钠溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、干燥后称量其质量为10.7g,则收集到的气体体积V值可为
A.2.24L B.4.48L C.6.72L D.7.84L
保密★启用前 试卷类型:A
2006-2007届河东三中高三化学教学质量检测题
2006-12-6
第Ⅱ卷(非选择题,共52分)
17.将某些化学知识用数轴表示,可以收到直观、简明、易记的效果。用数轴表示的下列知识正确的是
A.硫及其化合物的化会价与氧化还原反应的关系.

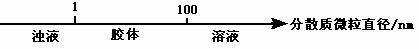
B.分散系的分类:
C.硫单质在02中燃烧后的产物:

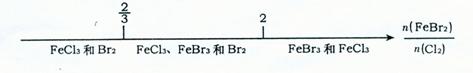
D.已知:还原性Fe2+>Br-,则FeBr2溶液与CI2反应的产物
16.在某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:
aA(气)+ B(气)  C(气)+ D(气)
5 min后达到平衡。已知该温度下其平衡常数K=1,若在温度不变情况下将容器的体积扩大为原来的10倍,其A的转化率不发生变化,则B的转化率为( )
C(气)+ D(气)
5 min后达到平衡。已知该温度下其平衡常数K=1,若在温度不变情况下将容器的体积扩大为原来的10倍,其A的转化率不发生变化,则B的转化率为( )
A.60% B.40% C.25% D.50%
15.短周期元素中,若两种元素的原子序数相差3,周期数相差1,它们形成常见化合物时原子数之比为1:2,那么这些化合物共有
A.1种 B.2种 C.3种 D.4种
14.已知25℃时,下列酸的电离常数:
醋酸:1.75×10-5 氢氰酸:4.93×10-10 氢氟酸:7.2×10-4 甲酸:1.77×10-4
则物质的量浓度均为0.1mol·L-1的上述溶液pH最大的是
A、 醋酸 B、 氢氰酸 C、氢氟酸 D、甲酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com