
题目列表(包括答案和解析)
24.(8分)化合物A[KxFe(C2O4)y·2H2O]是一种重要的光化学试剂。化学兴趣小组的同学为测定A的化学式,依次做了如下实验探究:
(A)取样品溶于水,向其中滴加KSCN试液,溶液呈血红色。
(B)准确称取A样品0.491 g,于110℃干燥脱水至恒重,质量为0.437 g.
(C)另取A 0.491 g置于锥形瓶中,加人是量的3 mol·Lˉ1的H2SO4溶液和适量蒸馏水,微热且加人0.050 mol·Lˉ1的KMnO4溶液24.0 mL,恰好完全反应。
(D)将(B)所得固体溶于水,加入还原铁粉至0.028 g时,恰好反应完全。
若已知:①A中铁元素只呈一种价态,
 ②
②
试完成下列问题:
(1)0.491 g A中所含结晶水的物质的量为____;
(2)A中n(Fe):n(C2O4)=___;
(3)A 的化学式____。
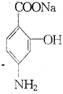
23.(10分)对氨基水杨酸钠( )是常用的抗结核菌药物(PAS)。
以下是它的一种合成路线。其关键步骤是中间产物C的合成。

请回答下列问题:
(1)写出化合物B的结构简式 。
(2)反应③所属的有机化学反应类型是 。
(3)化合物C有多种同分异构体,其中一类是苯的二取代物,该类物质的分子结构中,不可能含有下列基团(官能团)的是___(填名称)。
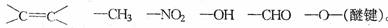
其中能与羧酸(浓H2SO4作催化剂、加热),发生酯化反应的同分异构体的结构简式是
(任写一个)。
(4)反应⑦的化学方程式是 。
22.(8分)(1)分子式为C5H11Br的有机物A与稀NaOH溶液共热后生成有机物B,B能与金属钠反应放出气体,但不能发生消去反应。C与B互为同分异构体,C分子中含有一个支链,且分子内脱水可生成两种不同的烯烃。则A的结构简式为 ;写出符合题意的C可能的结构简武为
(2)有机物M(C6H8O4)为食品包装纸的常用防腐剂,能使溴水褪色;M难溶于水,但在酸性条件下可发生水解反应得到N(C4H4O4)和甲醇。N结构中没有支链,能与氢氧化钠溶液反应。则由N 制 M的化学方程式为 。
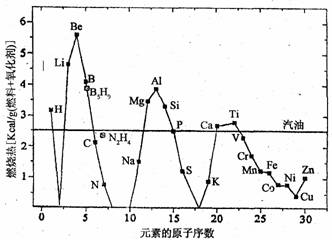
21.(10分)应用纳米技术制各的纳米金属燃料已应用到社会生活和高科技领域。一些原子序数较小的金属、非金属和常用燃料的单位质量燃烧热的比较如下图所示[肼(N2H4)和硼烷(B5H9)为传统火箭燃料]。
请回答下列问题:
(1)结合元素在地壳中的含量,在单位质量燃烧热大于汽油和氢单质的物质中,最具发展潜力的两种新型燃料可以是____(填写元素符号)。这些物质作为燃料使用,除具有高燃烧热值外,还具有的优点是____(填一项)。
(2)使金属在较低温度下燃烧的关键技术之一是将其制成纳米、微米级的颗粒。如此,不仅降低了金属燃料的燃点,也使得燃烧更为容易和充分,其原因是
(3)Be粉和MnO2粉末在高温下可以反应(类似铝热反应),请写出反应的化学方程式
;根据图示推测可能的原因是 。
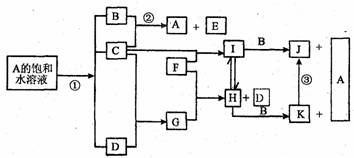
20.(8分)江苏省东部沿海有954 km的海岸线,合理开发和利用海洋资源对江苏经济发展意义重大。下图是部分元素的单质及其化合物的转化关系图(有关反应条件及部分反应物
或生成物已略去)。已知:A是海水中的重要资源;C、D、F是单质,其中C、D在常温常压下是气体;反应②是化工生产中的重要反应,生成物E是84消毒液的有效成份;J、K均为不溶于水的物质,其中J为红褐色。
请按要求填空:
(1)反应①的离子方程式(请注明反应条件) 。
(2)B的电子式____;E的化学式____。
(3)③的化学方程式 。
(4)D被誉为很有发展前途的未来燃料。你所了解的实现该目标尚存在的实际问题有
(列举一条)。
19. (10分)下列表示分子结构的图示中,●表示短周期的几种元素的“原子实”[指原子除去最外电子层电子后剩余的部分,周围小黑点表示没有用于形成共价键的最外层电子,短线代表共价键。例如X2(X代表卤素原子):
]
(10分)下列表示分子结构的图示中,●表示短周期的几种元素的“原子实”[指原子除去最外电子层电子后剩余的部分,周围小黑点表示没有用于形成共价键的最外层电子,短线代表共价键。例如X2(X代表卤素原子):
]
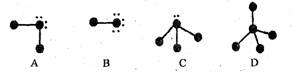
试回答下列问题:
(1)A、B、C、D四种“图示”中,所表示的物质可分为四组共____种。这些物质的分子中的电子总数可能为___或____。
(2)分子的空间构型为正四面体的物质的分子式是 。该组中,物质的稳定性顺序是____;它们沸点的变化与其余各组相比____(填“相同”或“不相同”),其原因是
(3)写出上述物质中的两种间相互反应生成离子化合物的化学方程式
(任写一个)。
18.(14分)某工业铁红中混有一种黑色的铁的氧化物杂质,为了解杂质的成分及测定铁红的纯度,化学兴趣小组的同学进行了实验探究。请你参与过程分析与交流。
[查阅资料]
①铁的常见氧化物
氧化亚铁(FeO)黑色固体,ω(Fe)=77.8%; 氧化铁(Fe2O3)红色固体,俗称铁红,
ω(Fe)=70.0%;四氧化三铁(Fe3O4)黑色固体,俗称磁性氧化铁,ω(Fe)=72.4%。
②草酸(乙二酸H2CO4)在浓H2SO4存在下受热分解的化学方程式为:
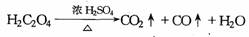
[实验准备]
①实验的装置图如下
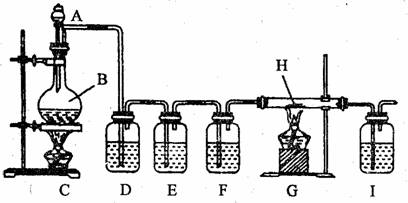
②药品及试剂
A、草酸 b、工业铁红 c、NaOH溶液 d、澄清石灰水
E、浓H2SO4 f、盐酸
[实验及数据]
取不同质量的样品进行实验,所得实验数据如下:
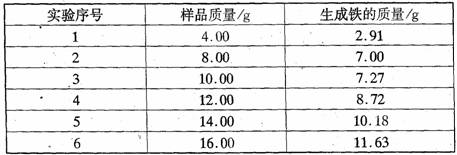
讨论与分析]
(1)兴趣小组的同学拟以纯净的CO还原铁的氧化物,所设计的实验装置中D、E、F应分别盛放的试剂为 、 、 、(填写序号,下同),其作用依次是
。
上述装置还有不完善之处,你建议改进措施是
(2)由实验数据不难得出,有-组实验数据不可靠,该组数据是 (填序号),该工业粗铁红所含杂质的化学式为 。
(3)该工业铁红中ω(Fe2O3)= 。
17.(8分)检查装置气密性是化学实验中的重要操作之一。试按要求回答下列问题:
(1)下列仪器或装置在使用前一定要检查气密性的是____(填序号,下同)。
A、容量瓶 B、洗气瓶 C、分液漏斗 D、酸(碱)式滴定管
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是____。
A、收集不到气体 B、造成环境污染
 C、观察到的实验现象有误 D、引发爆炸事故 ·
C、观察到的实验现象有误 D、引发爆炸事故 ·
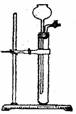
(3)为检查右图所示简易气体发生装置的气密性,甲、乙两位同学进行了以
下操作和方案设计。
①甲同学认为,只要往漏斗中加水,便可检验其气密性是否良好。经检验他
的方案可行。则甲同学的操作方法、现象和结论是 。
②乙同学设计的方案是:往漏斗中注人一定量的水至浸没长颈漏头下端。
关闭活塞,用手捂住试管中上部,待漏斗中液面上升一定高度,打开活塞让液面回落后,迅速关闭活塞,松开手,见漏斗中液面低于试管中液面且不再升降,说明气密性良好。乙同学设计方案的原理是 。
16.向某NaOH溶液中通人CO2气体后得溶液M,因CO2通人量的不同,溶液M的组成也不同。若向M中逐滴加人盐酸,产生的气体体积V(CO2)与加人盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)
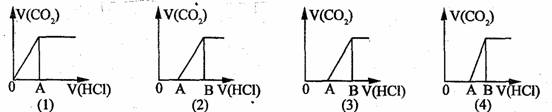
A、M中只有一种溶质的有(1)和(3)
B、M中有两种溶质的有(2)和(4)
C、(2)图显示M中c(NaHCO3)>c(Na2CO3)
D、(4)图显示M中c(NaHCO3)>c(Na2CO3)
15.25℃时,在25 mL o.1 mol·L-1的NaOH溶液中,逐滴加入
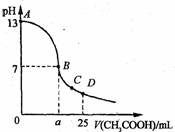 0.2 mol·Lˉ1的CH3COOH溶液。溶液pH的变化曲线如图
0.2 mol·Lˉ1的CH3COOH溶液。溶液pH的变化曲线如图
所示。下列分析的结论中,正确的是 ·
A、B点的横坐标a=12,5
B、C点时c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C、D点时c(CH3COO-)+c(CH3COOH)=2c(Na+)
D、曲线上A、B间任一点,溶液中都有:
c(Na+)>c(CH3COOˉ)>c(OH-)>c(H+)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com