
题目列表(包括答案和解析)
10.(15分)根据下列框图填空。已知反应①是工业上生产化合物D 的反应,反应⑤是实验室鉴定化合物E的反应。
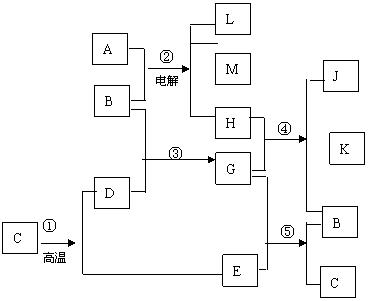
(1)单质L是 。
(2)化合物B是 。
(3)图中除反应①以,还有两个用手工业生产的反应,是 (填代号)。
(4)写出②、④、⑤化学反应方程式: ,
|
。
9.(15分)有四种化合物:W(有机物,通常状态下是气态)、X(通常状态下是液体)、Y、Z(通常状态下是固体,Y呈淡黄色)都是由短期周期元素A、B、C、D、E中的元素组成。已知:①A、B、C、D、E原子序数依次增大,且A与D同主族,C与E同主族,B与C同周期。②W由A和B组成,且W分子中原子个数比为A:B=1:1,X由A和C组成,且X的分子中原子个数比为A:C=2:1;Y由C和D组成,属离子化合物,且Y固体中原子个数比为C:D=1:1;Z由D和E组成,属离子化合物,且其中阳离子比阴离子少一个电子层。
(1)写出四种化合物的化学式:W ,
X ,
Y ,
Z ;
(2)W的分子构型为 型;
(3)Y的电子式 ;
(4)写出Y和X反应的化学方程式: ;
(5)用离子方程式表示Z的水溶液呈碱性的原因: 。
7.14gCu、Ag合金与足量的某浓度的硝酸反应,将放出的气体与1.12L标准状况下的氧气
混合,通入水中恰好被全部吸收。则原合金中铜的质量是 ( )
A.8.0g B.6.4g C.3.2g D.1.6g
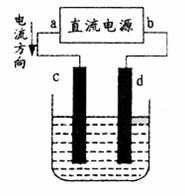 8.下图是电解CuC12溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是
8.下图是电解CuC12溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是
( )
A.a为负极、b为正极 B.a为阳极、b为阴极
C.电解过程中,氯离子浓度不变 D.电解过程中,d电极质量增加
6.某有机物的结构式为
它在一定条件下能发生的反应有 ( )
①加成 ②水解 ③酯化 ④氧化
⑤中和 ⑥消去 ⑦缩聚
A.①③⑤⑥ B.①③④⑤⑦
C.②③④⑦ D.②③④⑤⑥
5.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同
时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法正确的是 ( )
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量小
B.甲烧杯中的酸过量
C.两烧杯中参加反应的锌等量
D.反应开始后乙烧杯中的c(H+)始终比甲烧中的c(H+)小

4.用NA表示阿伏加德罗常数值,下列说法正确的是 ( )
A.常温时,1L0.1mol·L-1MgC12溶液中含Mg2+数为0.1NA
B.0℃1.01×105Pa时,2.24LCH4所含的电子数为2NA
C.20℃1.01×105Pa时,28gN2所含的电子数为1NA
|
3.质量分数为a的某物质的溶液mg与质量分数为b的该物质溶液ng混合后,蒸发掉pg水,
得到的溶液每毫升质量为qg,物质的量浓度为c。则溶质的相对分子质量为 ( )
A.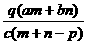 B.
B.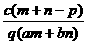
C. D.
D.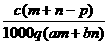
2.下列反应的离子方程式书写正确的是 ( )
A.向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液
Ca2++HCO3-+OH-=CaCO3↓+H2O
B.金属铝溶于氢氧化钠溶液 A1+2OH-=A1O2-+H2↑
C.用氢氧化钠溶液吸收过量二氧化碳 2OH-+CO2=CO32-+H2O
D. Fe2(SO4)3的酸性溶液中通入足量的硫化氢
Fe3++H2S=Fe2++S↓+2H+
1.第116号元素假如于2008年被发现。若IUPAC(国际纯粹与应用化学联合会)推荐该
元素的符号为Ch,以纪念该元素的发现地(China,中国)。下列关于Ch的说法正确的
是 ( )
A.Ch的最高价氧化物的水化物是强酸
B.Ch是超铀元素,其原子的质量数为116
C.Ch的氧化物有两种,即ChO2和ChO3,其钠盐的化学式为Na2Ch
D.Ch原子核外的电子层数为7,且是金属元素
25.(10分)化学实践活动小组参与某硝酸生产厂家的尾气处理设计。他们开展了以下的学习与工作:
(1)查阅资料:碱液吸收法是氮的氧化物的常用吸收处理方法之一。其化学反应原理为:
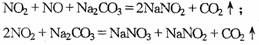
(2)经采样分析,该厂尾气中氮的氧化物有NO2(其中含体积分数为20%的N2O4)和NO。
(3)为进行理论研究,化学小组同学开展了模拟实验:
制取a L(已折合成标准状况,下同)NO2〈该条件下其中N2O4体积分数同采样)与b L NO混合后通人100 mL Na2CO3溶液。
试回答下列问题:
(1)若模拟实验中氮的氧化物全部被吸收,则a∶b应满足的条件是 ;
c(Na2CO3)应满足的条件是 (用含有a、b的代数式表示)。
(2)试分别给出生成的NaNO3和NaNO2物质的量与a、b的函数关系式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com