
题目列表(包括答案和解析)
12.在容积1升的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:(1)2A(g)  2B(g)+C(g);(2)A(g)
2B(g)+C(g);(2)A(g)  C(g)+D(g)。当达到平衡时,测得c(A)=2.5
mol·L-1,c(C)=2.0 mol·L-1。则下列说法中正确的是
C(g)+D(g)。当达到平衡时,测得c(A)=2.5
mol·L-1,c(C)=2.0 mol·L-1。则下列说法中正确的是
A.达到平衡时A的总转化率为40% B.达到平衡时c(B)为1.0 mol·L-1
C.达到平衡时c(B)=2c(D) D.达到平衡时c(D)=2c(B)
11.当前燃料电池发展迅速。固体氧化物燃料电池是由美国西屋(Westinghouse)公司研
制开发的。它以固体氧化锆一氧化钇为电解质,这种固体
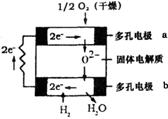 电解质在高温下允许氧离子(O2-)在其间通过。该电池的工
电解质在高温下允许氧离子(O2-)在其间通过。该电池的工
作原理如图所示,其中多孔电极a、b均不参与电极反应。
下列判断正确的是
A.有O2放电的a极为电池的负极
B.有H2放电的b极为电池的正极
C.a极对应的电极反应为:O2+2H2O+4e-=4OH-
D.该电池的总反应方程式为:2H2+O2=2H2O
10.下列离子方程式书写正确的是
A.NaClO溶液中通入少量二氧化硫:SO2+H2O+ClO-=SO42-+Cl-+2H+
B.碳酸氢钙溶液跟氢氧化钠溶液混合:HCO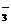 +OH-=CO
+OH-=CO +H2O
+H2O
C.金属钠加入水中:Na+H2O=Na++OH-+H2↑
D.苯酚钠溶液与氯化铝溶液反应:C6H5O-+Al3++3H2O=C6H5OH+Al(OH)3↓
9. TCL集团将于2006年全面采用钛金属技术。单质钛的机械强度高,抗蚀能力强,有“未来金属”之称。工业上常用硫酸分解钛铁矿(FeTiO3)的方法来制取TiO2,再由TiO2制金属钛,主要反应有:
①FeTiO3+3H2SO4 Ti(SO4)2+ FeSO4+3H2O
|
|
 ④TiO2+2C+2Cl2 TiCl4↑+2CO↑
④TiO2+2C+2Cl2 TiCl4↑+2CO↑
⑤TiCl4+2Mg=2MgCl2+Ti
下列叙述错误的是
A.反应①是非氧化还原反应 B. 反应②是水解反应
C.反应④中TiO2是氧化剂 C. 反应⑤是置换反应
8.设阿伏加德常数为NA。则下列说法正确的是
A.常温常压下,11.2L甲烷中含有的氢原子数为2NA
B.标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA
C.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA
D.常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA
7.继科学家发现C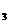 O
O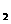 是金星大气成分之后,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质。已知硫化羰与二氧化碳的结构相似,但在氧气中会燃烧,下列有关C
是金星大气成分之后,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质。已知硫化羰与二氧化碳的结构相似,但在氧气中会燃烧,下列有关C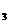 O
O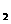 与硫化羰的说法中不正确的是
与硫化羰的说法中不正确的是
A.C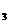 O
O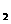 与CO一样可以在氧气中燃烧生成CO
与CO一样可以在氧气中燃烧生成CO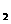
B.CO、C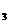 O
O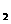 、CO
、CO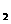 都是碳的氧化物,它们互为同素异形体
都是碳的氧化物,它们互为同素异形体
C.COS是由极性键构成的极性分子,分子中所有原子都满足8电子稳定结构
D.硫化羰在氧气中完全燃烧后的生成物是CO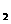 和SO
和SO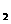
6. 下列说法正确的是
A.常温常压下,只有一种元素的单质呈液态
B.周期表中所有元素都是从自然界中发现的
C.过渡元素不全是金属元素
D.常温常压下,气态单质的分子都是由非金属元素的原子形成的
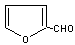
28.
 已知:HCN的结构为H-C≡N,R-CN
RCOOH,R-Cl+CN-
已知:HCN的结构为H-C≡N,R-CN
RCOOH,R-Cl+CN-
 R-CN+Cl-(R为烃基)。玉米芯、甘蔗渣等废物水解发酵后可制得糠醛 ,
它是重要的化工原料,它在一定条件下可发生以下变化:
R-CN+Cl-(R为烃基)。玉米芯、甘蔗渣等废物水解发酵后可制得糠醛 ,
它是重要的化工原料,它在一定条件下可发生以下变化:
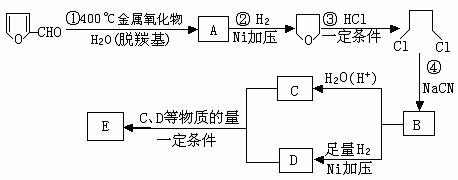
⑴写出反应类型:② ,④ 。
⑵写出反应③的化学方程式: ;
写出能证明糠醛中含有醛基的一个化学反应方程式 。
⑶若E为环状化合物,则其结构简式 。
⑷若E为高聚物,则其结构简式 。
26、(8分)(1)质子核磁共振谱(PMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中等性氢原子在PMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中氢原子数成正比。如CH3CHO分子的PMR谱有两个峰,其强度比是3:1。
若某分子式为C5H10O2的化合物在酸性条件下水解成甲和乙两种有机物,在相同的温度和压强下,同质量的甲和乙的蒸汽所占体积相同,则C5H10O2的PMR谱峰的强度之比可为 、 。
(2)有机物A与乙酸无论以何种比例混合,只要质量一定,完全燃烧后产生的水的质量也一定,试回答:
若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为___________。如果A分子每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为________________________。(用不含C原子的键线式表示)
28.(14分)钨是我国丰产元素,是熔点最高的金属 , 广泛用于拉制灯泡的灯丝 , 有“光明使者”的美誉。钨在自然界主要以钨 (+6价) 酸盐的形式存在。有开采价值的钨矿石是白钨矿和黑钨矿。白钨矿的主要成分是钨酸钙 (CaWO4);黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成(Fe,Mn)WO4。黑钨矿传统冶炼工艺的第一阶段是碱熔法:
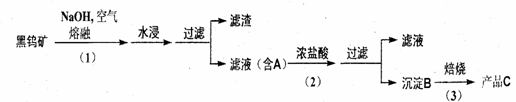
其中 A、B、C 都是钨的化合物。回答:
(1) 74W在周期表的位置是第 周期,第 族。
(2) 写出上述流程中 A 、B 、C 的化学式。
A_____________; B____________; C_____________
(3) 钨冶炼工艺的第二阶段则是用碳、氢等还原剂把氧化钨还原为金属钨。对钨的纯度要求不高时 , 可用碳作还原剂。写出用碳还原氧化钨制取金属钨的化学方程式:_______________________________________________________;
为了获得可以拉制灯丝的高纯度金制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂 ,为什么 ? _________________________________________。
(4) 仲钨酸的阱盐在热分解时会发生内在氧化还原反应 ,我国钨化学研究的奠基人顾冀东先生采用这一反应制得了蓝色的、非整比的钨氧化物 WO3-x。 这种蓝色氧化钨具有比表面大、易还原的优点 , 在制钨粉时温度容易控制 ,目前冶炼拉制钨丝的金属钨都用蓝色氧化钨为原料。经分析 , 得知蓝色氧化钨中钨的质量分数为 0.7985。
①计算 WO3-x中的x值。X=__________________
②一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在五价和六价两种价态的钨。则蓝色氧化钨中这两种价态的钨原子数比为________:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com