
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
5ЎўПВБРёчУР»ъОпЦР·РөгЧоөНөДКЗ(ЎЎЎЎЎЎ ) AЎўCH3(CH2)4CH3ЎЎЎЎ ЎЎ BЎўCH3(CH2)3CH3 ЎЎ CЎўCH3CH2C(CH3)3ЎЎ ЎЎDЎў(CH3)2C(CH3)2
4ЎўПВБРёчМюТ»¶Ё»ҘОӘН¬ПөОпөДКЗ(ЎЎ )
ўЩЈ®CH4Ј»ЎЎ ўЪЈ®CH3-(CH2)4-CH3 Ј»ЎЎ ўЫЈ®C2H4Ј»ЎЎ ўЬЈ®C6H12Ј»
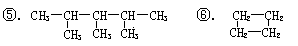
AЎўўЫўЬўЮ ЎЎЎЎЎЎBЎўўЫўЬЎЎ ЎЎЎЎCЎўўЩўЪўЭ ЎЎЎЎЎЎЎЎDЎўўЩўЫўЬўЮ
2ЎўҪ«ЕЁдеЛ®јУИлұҪЦРЈ¬деЛ®өДСХЙ«ұдЗіЈ¬ХвКЗУЙУЪ·ўЙъБЛ(ЎЎ )
AЎўСх»Ҝ·ҙУҰЎЎЎЎЎЎЎЎ BЎўИЎҙъ·ҙУҰЎЎЎЎЎЎЎЎ CЎўјУіЙ·ҙУҰЎЎЎЎ ЎЎЎЎ DЎўЭНИЎЧчУГ 3ЎўФЪ№вХХөДМхјюПВЈ¬ВИЖшёъјЧНй·ўЙъ»ҜС§·ҙУҰЈ¬ПВБРРрКцЦРХэИ·өДКЗ(ЎЎ )
AЎў·ўЙъөДКЗИЎҙъ·ҙУҰЎЎЎЎЎЎЎЎЎЎ BЎў·ўЙъөДКЗјУіЙ·ҙУҰ
CЎўЙъіЙөДІъОпТ»¶ЁУРЛДЦЦЎЎЎЎЎЎ DЎўЙъіЙөДІъОпЦРОпЦКөДБҝЧо¶аөДКЗЛДВИ»ҜМј
1ЎўПВБРОпЦКЦРЈ¬І»КфУЪУР»ъОпөДКЗ(ЎЎ )
AЎўДтЛШЎЎЎЎЎЎ BЎўҫЖҫ«ЎЎЎЎЎЎЎЎ CЎўЛХҙтЎЎЎЎЎЎЎЎ DЎўЛЬБП
25Ј®(10·Ц)
МјЛбЗвп§әНКмКҜ»Т№ІИИКұҝЙДЬ·ўЙъИзПВ·ҙУҰЈә
NH4HCO3+Ca(OH)2 CaCO3+NH3Ўь+2H2O
CaCO3+NH3Ўь+2H2O
NH4HCO3 NH3Ўь+CO2Ўь+H2O
NH3Ўь+CO2Ўь+H2O
ИЎМјЛбЗвп§әНКмКҜ»ТөД»мәПОп№І0Ј®1 molЈ¬ФЪГЬұХИЭЖчЦРјУИИЦБ200Ўж(200ЎжКұCaCO3ЎўCa(OH)2І»·ЦҪв)Ј¬ід·Ц·ҙУҰәуЈ¬ЕЕіц¶аУаЖшМеЈ¬АдИҙәуіЖБҝЈ¬№ММеКЈУаОпЦКБҝОӘa gЎЈ
(1)ИфМјЛбЗвп§әНКмКҜ»ТТФөИОпЦКөДБҝ»мәПКұЈ¬a=_________gЎЈ
(2)ИфТФbmolұнКҫ»мәПОпЦРМјЛбЗвп§өДОпЦКөДБҝЈ¬НЁ№эјЖЛгИ·¶ЁaЛжbұд»ҜөДКэС§ұнҙпКҪЎЈ
24Ј®(8·Ц)
ФЪДіЕЁ¶ИөДВИ»ҜұөИЬТәV mLЦРЈ¬јУИлТ»¶ЁМе»эЎўОпЦКөДБҝЕЁ¶ИОӘ0Ј®0500molЈҜLөДПЎБтЛбКұЈ¬БҪХЯЗЎәГНкИ«·ҙУҰЈ¬ҙЛКұИЬТәөДpH=3ЎЈКФЗуЈә
(1)јУИлПЎБтЛбөДМе»э(УГә¬VөДКэС§КҪұнКҫЈ¬БҪИЬТә»мәПКұМе»эұд»ҜәцВФІ»јЖ)ЎЈ
(2)ФӯВИ»ҜұөИЬТәөДОпЦКөДБҝЕЁ¶ИЎЈ
23Ј®(11·Ц)
ИшВЮ(Salol)КЗТ»ЦЦПы¶ҫјБЈ¬ЛьөД·ЦЧУКҪОӘC13Hl0O3Ј¬Жд·ЦЧУДЈРНИзПВНјЛщКҫ(НјЦРЗтУлЗтЦ®јдөДБ¬ПЯҙъұн»ҜС§јьЈ¬ИзөҘјьЎўЛ«јьөИ)Јә
(1)ёщҫЭУТНјДЈРНРҙіцИшВЮөДҪб№№јтКҪ__________ЎЈ
(2)ИшВЮҫӯЛ®ҪвЎў·ЦАлЎўМбҙҝҝЙөГөҪҙҝҫ»өДұҪ·УәНЛ®СоЛб(БЪфЗ»щұҪјЧЛб)ЎЈЗл»ШҙрН¬Кұ·ыәППВБРЛДёцТӘЗуөДЛ®СоЛбөДН¬·ЦТм№№Ме№ІУР___________ЦЦЎЈ
ўЩә¬УРұҪ»·Ј»
ўЪДЬ·ўЙъТшҫө·ҙУҰЈ¬І»ДЬ·ўЙъЛ®Ҫв·ҙУҰЈ»
ўЫФЪПЎNaOHИЬТәЦРЈ¬1 moёГН¬·ЦТм№№МеДЬУл2molNaOH·ўЙъ·ҙУҰЈ»
ўЬұҪ»·ЙПЦ»ДЬЙъіЙБҪЦЦТ»ВИҙъІъОпЎЈ
(1)ҙУ(2)И·¶ЁөДН¬·ЦТм№№МеЦРИОСЎТ»ЦЦЈ¬Цё¶ЁОӘПВБРҝтНјЦРөДAЎЈ
ЎЎ ЎЎ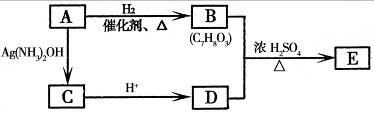
ТСЦӘEЦРә¬УР1 4ёцМјФӯЧУЎЈРҙіцПВБРБҪёц·ҙУҰөД»ҜС§·ҪіМКҪ(УР»ъОпУГҪб№№јтКҪұнКҫ)Ј¬ІўЦёіцПаУҰөД·ҙУҰАаРНЎЈ
ЎЎ ўЩAЎъB_______________________________ЎЈ·ҙУҰАаРНЈә______________ЎЈ
ЎЎ ўЪB+DЎъE_____________________________ЎЈ·ҙУҰАаРНЈә______________ЎЈ
22Ј®(7·Ц)
LТ»¶а°НКЗТ»ЦЦУР»ъОпЈ¬ЛьҝЙУГУЪЕБҪрЙӯЧЫәПЦўЦОБЖЈ¬Жд·ЦЧУКҪОӘЈәC9H11O4NЎЈХвЦЦТ©ОпөДСРЦЖКЗ»щУЪ»сөГ2000ДкЕөұҙ¶ыЙъАнС§»тТҪС§ҪұәН»сөГ2001ДкЕөұҙ¶ы»ҜС§ҪұөДСРҫҝіЙ№ыЎЈТСЦӘә¬МјЎўЗвЎўСхЎўөӘ4ЦЦФӘЛШөДУР»ъОпФЪҝХЖшЦРНкИ«ИјЙХЙъіЙ¶юСх»ҜМјЎўЛ®әН°ұЖшЎЈ
(1)LТ»¶а°Н·ЦЧУФЪҝХЖшЦРИјЙХөД»ҜС§·ҪіМКҪКЗ_________________________Ј»
(2)ИфМюC7H12әНC5H12өД»мәПОп1 molФЪҝХЖшЦРНкИ«ИјЙХКұПыәДөДСхЖшОӘ9 molЈ¬Фт»мәПОпЦРC7H12әНC5H12өДЦКБҝұИОӘ______________Ј»
(3)ИфДіМюөДоҙСхСЬЙъОп0Ј®1 molФЪҝХЖшЦРНкИ«ИјЙХКұПыәДөДСхЖшөДОпЦКөДБҝУлөИОпЦКөДБҝөДL-¶а°Н·ЦЧУНкИ«ИјЙХКұПыәДөДСхЖшПаН¬Ј¬ЗТЙъіЙ¶юСх»ҜМј17Ј®92L(ұкЧјЧҙҝц)Ј¬ФтёГМюөДә¬СхСЬЙъОпНЁКҪОӘ_________________ (УГә¬nөД»ҜС§КҪұнКҫ)ЎЈ
21Ј®(9·Ц)
ҙуЖшОӘөШЗтЙПёчЦЦЙъОпөДЙъҙжМṩБЛМхјюЎЈө«КЗЈ¬ЛжЧЕ№ӨТөәНҪ»НЁФЛКдСёЛЩ·ўХ№Ј¬іЗКРИЛҝЪёЯ¶ИјҜЦРЈ¬ИЛАаПтҙуЖшЦРҙуБҝЕЕ·ЕСМіҫәНУРәҰЖшМеөИЈ¬ХэФЪ¶ФҙуЖшФміЙОЫИҫЎЈОТ№ъДі№ӨТөіЗКРөДЎ°ҝХЖшЦКБҝИХұЁЎұПФКҫЈ¬ёГіЗКРөДҝХЖшКЬөҪТ»¶ЁіМ¶ИөДОЫИҫЎЈДіСРҫҝРФС§П°РЎЧй¶ФёГіЗКРөДҝХЖшОЫИҫҪшРРБЛПВБРСРҫҝЎЈ
(1)РЎЧйДЪТ»Н¬С§іхІҪ·ЦОцөГіцЈ¬ёГіЗКРҝХЖшОЫИҫөДЦчТӘФӯТтУР
AЈ®К№УГКҜУНТә»ҜЖш
BЈ®ИјЙХә¬БтГә
 CЈ®·ЫіҫОЫИҫИэёцЎЈБнТ»Н¬С§ИПОӘ»№УРТ»ёцІ»ҝЙЕЕіэөДФӯТтКЗЈә
CЈ®·ЫіҫОЫИҫИэёцЎЈБнТ»Н¬С§ИПОӘ»№УРТ»ёцІ»ҝЙЕЕіэөДФӯТтКЗЈә
DЈ®______________________________________ЎЈ
СРҫҝРФС§П°РЎЧйҫНФміЙёГіЗКРҝХЖшОЫИҫөДЧоЦчТӘФӯТтөчІйБЛёГКР100ГыКРГсәН100О»»·ұЈІҝГЕИЛКҝЎЈөчІйҪб№ыИзПВНјЛщКҫЈәЎЎ

(1)ҙУ»·ұЈИЛКҝөД№ЫөгЙП·ЦОцЈ¬ДгИПОӘФміЙёГіЗКРҝХЖшОЫИҫөДЦчТӘУРәҰіЙ·ЦКЗ_______________ (УГ»ҜС§КҪұнКҫ)ЎЈ
(2)ҝХЖшОЫИҫТЧРОіЙЛбУкЎЈСРҫҝРФС§П°РЎЧй¶ФёГіЗКРөДУкЛ®ҪшРРБЛІЙСщУл·ЦОцЈ¬ёХІЙјҜКұІвөГpHОӘ4Ј®82Ј¬·ЕФЪЙХұӯЦРҫӯ2 hәуЈ¬ФЩҙОІвөГpHОӘ4Ј®68ЎЈ¶ФҙЛЈ¬ДгөДәПАнҪвКНКЗ___________________ЎЈ
(3)СРҫҝРФС§П°РЎЧйН¬С§ИЎҝХЖш(ә¬өӘЖшЎўСхЖшЎў¶юСх»ҜМјЎў¶юСх»ҜБтөИ)10Ј®0 L_(ТСХЫЛгіЙұкЧјЧҙҝц)Ј¬»әВэНЁ№эЧгБҝдеЛ®Ј¬ФЪЛщөГИЬТәЦРјУИл№эБҝөДВИ»ҜұөИЬТәЈ¬ІъЙъ°ЧЙ«іБөнЈ¬Ҫ«іБөнПҙөУЎўёЙФпЈ¬іЖөГЖдЦКБҝОӘ0Ј®0233gЎЈКФ»ШҙрёГ°ЧЙ«іБөнөД»ҜС§КҪОӘ_________________Ј¬НЁ№эјЖЛгөГёГҝХЖшЦРЦчТӘУРәҰЖшМеіЙ·ЦөДМе»э·ЦКэОӘ____________________________ЎЈ
(4)ёГРЎЧйН¬С§МбіцПВБРҙлК©ТФјхЙЩҝХЖшОЫИҫөДЦчТӘУРәҰіЙ·ЦЕЕ·ЕБҝЈ¬ДгИПОӘәПАнөДКЗ____________ (МоРтәЕ)ЎЈ
ЎЎЎЎ ўЩУГМмИ»ЖшҙъМжГәМҝЧцГсУГИјБПЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎ ўЪёДҪшИјГәјјКхЈ¬јхЙЩГәөДУГБҝ
ЎЎЎЎ ўЫ№Өі§ЙъІъКұҪ«ИјГә№шВҜөДСМҙСФмөГёьёЯЎЎЎЎ ўЬИјГәЦРјУИлККБҝКҜ»ТКҜәуК№УГ
20Ј®(10·Ц)
·ўЙдәҪМм»рјэіЈУГөӘөДЗв»ҜОплВ(N2H4)ЧчИјБПЎЈКФ»ШҙрПВБРУР№ШОКМвЈә
(1)РҙіцN2өДөзЧУКҪЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)ТәМ¬NH3АаЛЖH2OЈ¬ТІДЬОўИхөзАлЗТІъЙъөзЧУКэПаН¬өДБҪЦЦАлЧУЈ¬ФтТәМ¬NH3өзАл·ҪіМКҪОӘ_________________________________ЎЈ
(3)25ЎжКұЈ¬0Ј®1 molЎӨL-1 NH4NO3ИЬТәЦРЛ®өДөзАліМ¶И________________ (МоЎ°ҙуУЪЎұЎўЎ°өИУЪЎ°»тЎ°РЎУЪЎұ)0Ј®1 molЎӨL-l NaOHИЬТәЦРЛ®өДөзАліМ¶ИЎЈИфҪ«0Ј®1molЎӨL-1NaOHәН0Ј®2molЎӨL-1 NH4NO3БҪИЬТәөИМе»э»мәПЈ¬ЛщөГИЬТәЦРАлЧУЕЁ¶ИУЙҙуөҪРЎөДЛіРтОӘ___________________________________________ЎЈ
ЎЎЎЎ (4)ФЪҪб№№ЙПN2H4әНNH3өД№ШПөУРИзH2O2әНH2OөД№ШПөЎЈN2H4ДЬ·ўЙъПВБР·ҙУҰЈә
ЎЎЎЎ
N2H4+H3O+==N2H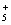 +H2OЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
N2H4+H2O
+H2OЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
N2H4+H2O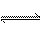 N2H
N2H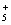 +OH-
+OH-
ЎЎЎЎЎЎ
N2H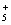 +H2O
+H2O N2H
N2H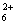 +OH-ЎЎЎЎ
ЎЎЎЎЎЎЎЎ ЎЎЎЎN2H
+OH-ЎЎЎЎ
ЎЎЎЎЎЎЎЎ ЎЎЎЎN2H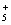 + H2O
+ H2O N2H4+H3O+
N2H4+H3O+
ЎЎЎЎ ҫЭҙЛҝЙөГіцөДҪбВЫКЗ______________________ЎЈ
ЎЎЎЎЎЎ AЈ®лВЛ®ҪвПФЛбРФЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ BЈ®лВФЪЛ®ЦРөзАліцH+АлЧУ
ЎЎЎЎЎЎ CЈ®лВКЗ¶юФӘИхјоЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ DЈ®лВКЗ¶юФӘИхЛб
ЎЎЎЎ (5)НкіЙПВБР·ҙУҰ·ҪіМКҪІўЕдЖҪЈәЎЎ
ЎЎЎЎ ______NH3+______NaClO==_________NaCl+_______N2H4+_____ЎЎ _____
(6)·ўЙд»рјэКұлЭ(N2+H4)ОӘИјБПЈ¬¶юСх»ҜөӘЧчСх»ҜјБЈ¬БҪХЯ·ҙУҰЙъіЙөӘЖшәНЖшМ¬Л®ЎЈТСЦӘ4gN2H4(g)ФЪЙПКц·ҙУҰЦР·Еіц71kJөДИИБҝЈ¬РҙіцёГ·ҙУҰөДЧӘ»ҜС§·ҪіМКҪЎЎЎЎЎЎ
_______________________ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com