
题目列表(包括答案和解析)
11.下列各组离子能大量共存,当溶液中C(H+)=10-1mol·L-1时,有气体产生;
而当溶液中C(H+)=10-13mol·L-1时,又能生成沉淀。则该组离子可能是:
A.Na+、Cu2+、NO3-、CO32- B.Ba2+、K+、Cl-、HCO3-
C.Fe2+、Na+、SO42-、NO3- D.Mg2+、NH4+、SO42-、Cl-
10.下列各组物质的颜色变化,可用勒夏特列原理解释的是:
A.光照氯水,颜色变浅 B.向盛有NO2的集气瓶中投入活性炭,颜色变浅
C.加热氯化铁溶液,溶液变浑 D.压缩H2与I2(g)反应的平衡混合气体,颜色变深
9.对已达到平衡的反应:2X(g)+Y(g) 2Z(g),减小压强时,对反应产生的影响是:
2Z(g),减小压强时,对反应产生的影响是:
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
8.NH4+浓度相同的下列各物质的溶液中,溶液的物质的量浓度最大的是:
A.NH4Al(SO4)2 B.NH4HCO3 C.NH4HSO4 D.NH4NO3
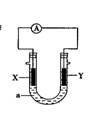
7.如图:X为单质硅,Y为金属铁,a为NaOH溶液,
按图组装一个原电池,下列说法正确的是:
A.X为负极,电极反应为:Si-4e-=Si4+
B.X为正极,电极反应为:4H2O+4e-=4OH-+2H2↑
C.X为负极,电极反应为:Si+6OH--4e-=SiO32-+3H2O
D.Y为负极,电极反应为:Fe-2e-=Fe2+
6.室温下对pH相同、体积相同的醋酸和硫酸两种溶液分别采取下列措施,
有关叙述中正确的是
A.加水稀释2倍后,两溶液的pH均减小
B.使温度都升高20℃后,两溶液的pH均不变
 C.加适量的醋酸钠晶体后,两溶液的pH均增大
C.加适量的醋酸钠晶体后,两溶液的pH均增大
D.加足量的锌充分反应后,两溶液中产生的氢气一样多
5.下列有关中和滴定的叙述中正确的是:
A.滴定时,标准液的浓度一定越稀越好
B.用盐酸作标准液滴定NaOH溶液时,指示剂加入越多越好
C.滴定管在滴液前和滴液后均有气泡一定不会造成误差
D.滴定时眼睛应注视锥形瓶内溶液的颜色变化而不应注视滴定管内的液面变化
4.下列金属组合中,一般用电解法冶炼的是
A.Fe、Hg、Na B.A1、Na、K C.A1、Fe、Ag D.Cu、Ag、Au
3.要使氯化铝溶液中的A13+完全转化成A1(OH)3沉淀,应选用的试剂是:
A.NaOH溶液 B.稀盐酸 C. 氨水 D.AgNO3溶液
2.下列物质的稀溶液中不存在除水以外的其他分子的是:
A.KHCO3 B.KCl C.HF D.NH4Cl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com