
题目列表(包括答案和解析)
21.(8分)A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,
C、D、E同处另一周期.C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙。D、A可按原子个数比3:2形成离子化合物丙。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)B元素在周期表中的位置是 丙的化学式是
(2)由上述元素中的三种组成的水溶液呈碱性的盐的化学式为 ,
其水溶液呈碱性的原因是 (用离子方程式表示)。
20.(13分)在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是:
(填粒子的化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物
是
(2)现提供以下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
请判断哪位同学的推断是正确的,并用两种方法加以验证,写出选用的试剂编号
及实验中观察到的现象。
|
同学正确 |
选用试剂 |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子
是 若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,
你认为是否可行?
理由是:
19.(9分)在常温常压下,注射器甲中装有N02气体,注射器乙中
装有相同体积的空气(如图所示,夹持仪器均已略去)
(1)常温下,打开两个止水夹后,同时向外拉动两注射器的活
塞,且拉动的距离相同,将会看到U形管中液面
a. (填升高、下降 或不变)。
试解释这一现象:
(2) 如将注射器甲中的气体换成NH3、U形管中的CCl4换成水,
仍在常温下,打开两个止水夹后,同时向里推动两注射器的活塞,且推动的距离相同,将会看到U形管中液面a (填升高 、 下降 或 不变 )。
试解释这一现象
18.MOH和ROH两种一元碱的溶液分别加水稀释时,
pH变化如右图所示。下列叙述中不正确的是
A.ROH是一种强碱
B.在x点,MOH完全电离
C.在x点,c(M+)==c(R+)
D.稀释前,c(ROH)==10c(MOH)
第Ⅱ卷 (非选择题 共76分)
17.已知NaHS04在水中的电离方程式为:NaHSO4==Na++H++SO42-。某温度下,
向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。
则下列对该溶液的叙述中不正确的是
A.该温度高于25℃
B.由水电离出来的C(H+)=1×10-10 mol·L-1
C.该温度下加入等体积pH为12的NaOH溶液可使反应后的溶液恰好呈中性
 D.等物质的量浓度的NaHSO4与盐酸的酸性相当
D.等物质的量浓度的NaHSO4与盐酸的酸性相当
16.已知Zn(OH)2与A1(OH)3一样,是一种两性氢氧化物,它与强酸、强碱反应的
离子方程式分别为:Zn(OH)2+2H+==Zn2++2H20,Zn(OH)2+20H-==ZnO22-+2H20,
但Zn(OH)2能溶于过量的氨水中,而Al(OH)3却不能,其反应的离子方程式
为;Zn(OH)2十4NH3·H20==Zn(NH3)42++20H-+4H2O。则下面四组物质的溶液,不能运用滴加顺序进行鉴别的是:
A.A1Cl3、NH3·H20 B.ZnCl2、NH3·H20
C.A1Cl3、NaOH D.ZnCl2、NaOH
15.已知在一绝热容器中,饱和石灰水中存在溶解平衡:Ca(OH)2(s) 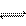 Ca2++20H-
Ca2++20H-
现向其中加入少量生石灰,则下列说法中不正确的是
A.溶液中固体的质量增加 B.溶液中Ca2+的浓度减小
C.溶液中OH-的数目减少 D.溶液的pH不变
14.常温下,把盐酸和氨水等体积混合后,其混合液的pH为7,则下列说法中正确的是
A.盐酸中的c(H+)一定大于氨水中的c(OH-)
B.反应后生成的盐在溶液中不能发生水解
C.盐酸的物质的量浓度一定小于氨水的物质的量浓度
D.盐酸中氯化氢的物质的量一定等于NH3·H2O的物质的量
13.已知NaH2P04、NaHC204、NaHS03的水溶液的pH均小于7,由此可以推断
A.H3PO4、H2C204、H2SO3都是弱酸
B.H2PO4-、HC2O4-、HSO3-、的电离程度小于其水解程度
C.H3PO4、H2C2O4、H2SO3、的酸性均强于H2CO3
D.NaH2PO4、NaHC2O4、NaHSO3只能与强碱反应,不能与强酸反应
12.下列说法中不正确的是:
A.增大反应物浓度,可使单位体积内活化分子数增加,反应速率加快
B.在其它条件不变时,升高温度一定会加快化学反应的反应速率
C.使用合理的催化剂,可以改变化学反应速率,但不能改变化学平衡状态
D.对于任何化学反应来说,反应速率越大,反应现象就越明显
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com