
题目列表(包括答案和解析)
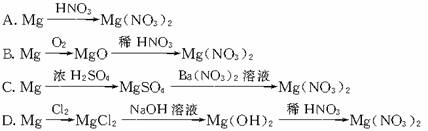
15.“绿色化学”是从经济、环保和技术上设计符合“原子经济性”(原子节约)要求的化学反应。理想的原子经济反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。下列几种生产Mg(NO3)2的方法中,最符合“绿色化学”新理念的是
14.在某恒容的密闭容器中,可逆反应A(g)+B(g) xC(g)有如图所示的关系曲线,下列说法正确的是
A.温度:T1>T2 B.压强:p1>p2?
C.该正反应是吸热反应 D.x的值是1
13.下列离子方程式中正确的是
A.向 Ba(OH)2溶液中滴加稀H2SO4
Ba2++2OH-+2H++SO===BaSO4↓+2H2O
B.将含有2 n mol NaOH的溶液与含有n mol Ca(HCO3)2的溶液混合
OH-+Ca2++HCO===CaCO3↓+H2O
C.在标准状况下将少量Cl2通入FeBr2溶液中
3Cl2+2Fe2++4Br-===6Cl-+2Fe3++2Br2
D.将等体积、等物质的量浓度的Ba(OH)2溶液和NaHCO3溶液混合
Ba2++2OH-+2HCO===BaCO3↓+CO+H2O
12.等体积、等物质的量浓度的Na2SO4和Na2CO3溶液,两份溶液中离子总数相比
A.前者多 B.后者多
C.一样多 D.无法判断
11.某固体化合物A不导电,但熔化或溶于水都能完全电离。下列关于物质A的说法中,不正确的是
A.A为易溶性盐 B.A是强电解质
C.A是离子化合物 D.A为非电解质
10.最近,科学家在实验室里成功地在高压下将CO2转化为类似于SiO2的原子晶体。下列有关这种CO2晶体的叙述中错误的是
A.晶体中C、O原子个数比为2∶1
B.晶体中存在直线型CO2分子
C.该晶体熔点、沸点高,硬度大
D.晶体中C、O原子的最外电子层都满足8电子结构
9.在理论上不能用于设计原电池的化学反应是
A.HCl+NaOH===NaCl+H2O ΔH<0
B.2CH3O(l)+3O2(g)  2CO2(g)+4H2O(l) ΔH<0
2CO2(g)+4H2O(l) ΔH<0
C.4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH<0
D.2H2(g)+O2(g)===2H2O(l) ΔH<0
8.氟气是氧化性最强的非金属单质。在加热条件下,等物质的量的氟气与烧碱完全反应。生成NaF、H2O和另一种气体,该气体可能是
A.H2 B.HF
C.O2 D.OF2
7.实验室制备①氯化氢、②乙烯、③硝基苯、④硝化纤维、⑤乙酸乙酯、⑥硝酸时都用到浓H2SO4,其中利用其高沸点性质的是
A.只有① B.①④
C.①⑥ D.③⑤
6.在元素周期表短周期中的X和Y两种元素可组成化合物XY3,下列说法正确的是
A.XY3晶体一定是离子晶体
B.若Y的原子序数为m,X的原子序数一定是m±4
C.X和Y可属于同一周期,也可属于两个不同周期
D.X和Y一定不属于同一主族
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com