
题目列表(包括答案和解析)
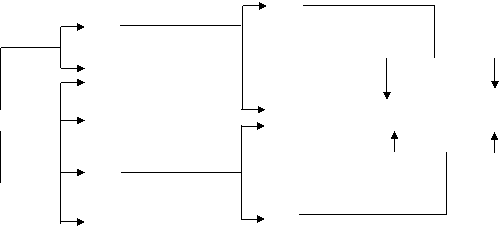
11.(9分)下图每一方框中的字母代表一种反应物或生成物:
|
|

|

|
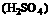 =1:1
=1:1

|
|
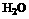
|
|
|
|
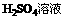
 n(B):n
n(B):n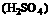 =1:2
=1:2
|
Y溶液
已知:常温下,C、D、F都是无色气体,其中C和D分子中的质子总数相等,C是一种可燃性气体,D能使湿润的红色石蕊试纸变蓝色,F能使澄清石灰水变浑浊;H是不溶于稀硝酸的白色沉淀。
(1)写出下列物质的化学式:C 、D 甲 、X 。
(2)写出NaOH与乙反应的有关化学方程式: 、
。
(3)写出G与Y反应后溶液为中性的离子方程式:
。
10.(10分)(1)工业上用MnO2和KOH为原料制取高锰酸钾,主要生产过程两步进行,第一步将MnO2和固体KOH粉碎,混合均匀,在空气中加热至熔化,并连续搅拌,以制取K2MnO4;第二步将K2MnO4的浓溶液电解,以制取KMnO4,回答下列问题:
①写出制取K2MnO4的化学反应方程式 ,连续搅拌的目的是 。
②电解K2MnO4的浓溶液时,两极发生的电极反应式是:阳极 ,
阴极 ,电解总的反应方程式是 。
(2)在淀粉-KI溶液中,滴入少量NaClO溶液,并加入少量硫酸,溶液立即变蓝,这
是因为 ,离子方程式是 。在上述蓝
色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失,这是因为
,离子方程式是 。以上实验条件下,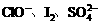 的氧化性由强到弱的顺序是
。
的氧化性由强到弱的顺序是
。
9.如下图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯中。在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加任何物质,发现(1)中NO2红棕色变深,(3)中NO2红棕色变浅,下列叙述不正确的是
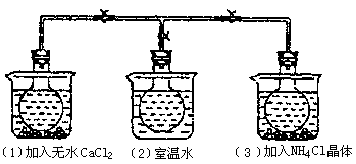
A.CaCl2溶于水时放出热量 B.烧瓶(1)中气体的压强增大
C.NH4Cl溶于水时放出热量 D.烧瓶(3)中气体的压强减小
8.下列说法正确的是
A.将pH=2的酸溶液稀释10倍溶液的pH值一定变为3
B.将pH=2的盐酸溶液和pH=4的盐酸溶液等体积混合后,溶液的pH值变为3
C.将pH=12的Ba(OH)2溶液稀释10倍,溶液的PH值变为13
D.将pH=a的盐酸与pH=b的NaOH溶液等体积混合后,若pH=7,则a+b=14
7.铜、镁合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mLN2O4气体(气体均为标况),在反应后的溶液中加入足量的NaOH溶液,生成沉淀的质量为
A.7.04g B.8.26g C.8.51g D.9.02g
6.SF6是一种无色气体,具有很强的稳定性,可用于灭火。SF6的分子结构如右图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为
A.6种 B.7种
C.10种 D.12种
5. 反应:2NH3(g)+CO2(g)
CO(NH2)2(s)+H2O(g)已达平衡。若增大压强,平衡移动,但混合气体的平均相对分子质量不变。下列说法正确的是
反应:2NH3(g)+CO2(g)
CO(NH2)2(s)+H2O(g)已达平衡。若增大压强,平衡移动,但混合气体的平均相对分子质量不变。下列说法正确的是
A.原混合气体的平均相对分子质量为30
B.原混合气体的平均相对分子质量为28
 C.起始时,NH3与CO2的体积比为13:14
C.起始时,NH3与CO2的体积比为13:14
D.起始时,NH3与CO2的体积比为14:15
4.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断不正确的是
A.原子晶体干冰有很高的熔点、沸点,有很大的硬度
B.原子晶体干冰易气化,可用作制冷材料
C.原子晶体干冰硬度大,可用作耐磨材料
D.每摩尔原子晶体干冰中含4mol C-O键
3.下列物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是①H2S+O2;②P+Cl2;③P2O5+H2O;④NaCl(固)+H2SO4(浓);⑤AlCl3+NaOH;⑥乙醇和浓硫酸;⑦苯和氯气;⑧碳酸钠和稀盐酸;⑨硫和氧气;⑩H2S+NaOH
A.全部都是 B.①②⑤⑧⑩
C.①②⑤⑦⑧⑩ D.①②④⑤⑦⑧⑨⑩
2.如图,标准状况下,向带有活塞的最大容积为120 L的密闭容器中充入a mol H2S和b mol SO2(a、b为正整数;a£5,b£5),则反应完全后,容器内气体可能达到的最大密度(g/L)是
A.14.40 B.8.00 C.5.60 D.2.86
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com