
题目列表(包括答案和解析)
28.将nmol木炭粉和1mol氧化亚铁在反应器中混和,隔绝空气加强热。
(1)可能发生反应有:
①FeO+C=Fe+CO↑ ②2FeO+C=2Fe+CO2↑
③FeO+CO=Fe+CO2↑ ④
(2)若n<1/4,充分反应后,反应器中的固体物质是 ,气体产物是 。
(3)若n>4,充分反应后,反应器中的固体物质是 ,气体产物是 。
(4)若反应的气体产物是混和物,n的取值范围是 。
(5)若反应的气体产物是混和物,且混和物中CO和CO2的物质的量相等,则n的值为 。
27.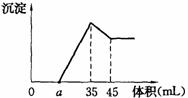 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL 浓度的H2SO4溶液中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀与加入NaOH溶液的体积的关系如右图所示,求:
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL 浓度的H2SO4溶液中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀与加入NaOH溶液的体积的关系如右图所示,求:
(1)H2SO4溶液的物质的量浓度;
(2)若a=2.3mL,计算各组分的质量;
(3)计算a值的取值范围。
26.在微热条件下,将11.2g铁粉恰好溶解在100mL10mol/L的浓硝酸中,若反应的气体产物为NO和NO2的混和物,且整个过程中不考虑硝酸的挥发、分解,也不考虑NO2的聚合,求气体产物中NO2与NO的物质的量之比。
25.现将11.2g铁粉完全溶解在500mL稀硝酸中,硝酸的还原产物是NO,反应结束后,再加入6.4g铜粉,试求下列情况下硝酸物质的量的浓度:
(1)铜粉恰好完全溶解且无气体放出
(2)铜粉恰好完全溶解一半且无气体放出
24.现有废液,其中含有CuCl2、FeCl2、HCl。某课外活动小组计划用它得到纯净的FeCl2晶体。为此,设计如下实验方案:
|
序号 |
A |
B |
C |
D |
E |
|
仪器及药品 |
 |
 |
 |
 |
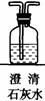 |
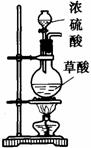
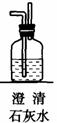
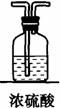
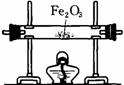
第一步:用上图中的仪器和药品组装一套实验装置制取干燥纯净的CO,用CO还原Fe2O3粉末制取还原铁粉。(制取CO的原理为:H2C2O4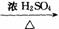 CO2↑+CO↑+H2O)
CO2↑+CO↑+H2O)
(1)如果所制气体流向从左向右时,上述组装的实验装置从左向右直接连接顺序(填仪器序号)是 → → → → 。
(2)正确的操作步骤中第一步应是: ;最后一步应是熄灭 处的酒精灯。
(3)装置B的作用是 ;装置E的作用是 。
第二步:将制得的还原铁粉放入原混合溶液中,制得纯净的FeCl2溶液。
(4)必须进行的操作是 。
第三步:得到纯净的FeCl2晶体。
(5)必须进行的操作是 。
23.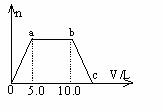 向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成的沉淀的物质的量(n)和通入CO2气体体积(V)的关系如右图,试回答:
向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成的沉淀的物质的量(n)和通入CO2气体体积(V)的关系如右图,试回答:
(1)a点之前的反应的离子方程式为:
________________________________________.
(2)a点到b点之间的反应离子方程式是:
________________________________________.
(3)c点的二氧化碳体积是 L
(4)混合稀溶液中Ba(OH)2和NaOH的物质的量之比为
22.在MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如下图所示,则:
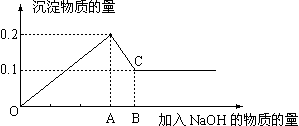
(1)图中C点表示当加入 molNaOH时,Al3+已经 ,Mg2+已经 。
(2)图中线段OA︰AB= 。
一定条件下,可逆反应A2+B2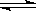 2C达到平衡后,c(A2)=0.5mol/L,c(B2)=0.1mol/L,c(C)=1.6mol/L。若A2、B2、C的起始浓度分别为amol/L、bmol/L、gmol/L。请确定:
2C达到平衡后,c(A2)=0.5mol/L,c(B2)=0.1mol/L,c(C)=1.6mol/L。若A2、B2、C的起始浓度分别为amol/L、bmol/L、gmol/L。请确定:
(1)a、b应满足的关系式__________________
(2)若反应从正反应方向开始进行,当g=__________是,a有最大值为_________
(3)若反应从逆反应方向开始进行,当b=__________是,a有最小值为_________
(4)综合⑵、⑶的结论,可知本题中a的取值范围为________________________。
21.已知X、Y均为短周期元素,X在空气中燃烧发出耀眼白光。气体G与氢气密度之比为8.5,B是一种化肥的重要组成部分,可由人体肝脏产生,也可由C分解而成。D是一种高分子化合物,能作为重金属盐中毒后的解毒剂。
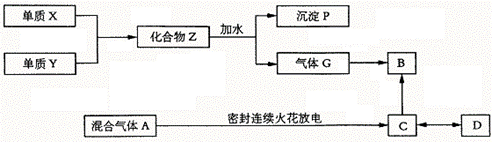
(1)写出X、Y、Z、P、G的化学式。
(2)写出B、C、D的名称。
(3)A中所含的主要气体成分是 ,这一实验最先由 设计完成。
(4)C分解成B是通过 作用。D是生物体内的 细胞器合成。
20.在一定条件下可实现下图所示的各物质之间的变化:
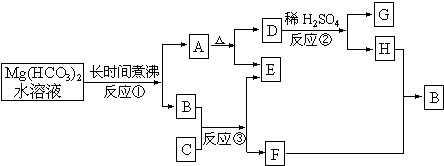
请填写下列空白:
(1)写出A、G的化学式:A 、G ;
(2)反应②中加入稀硫酸的作用是 ;
(3)写出反应③的化学方程式 ;
(4)反应①能生成A物质的原因是 。
19.今有四种固体投入水中分别产生E、F、G、M四种气体,这四种气体之间的反应如下:E+F→N;F+G→Q;Q+E→N+W;G+E→N+W;M+E→N+I,其中I是双原子分子中键 能最大的单质气体,则按产生气体E、F、G、M的顺序四种固体物质分别是
A Na2O2 Na CaC2 Mg3N2 B Na2O2 Li CaC2 (NH4)2S
C Na Na2O2 CaC2 (NH4)2S D Na Na2O2 CaC2 Mg3N2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com