
题目列表(包括答案和解析)
1、周期表前20号元素中,它们形成离子化合物时,原子数之比为1﹕2,且阴阳离子的电子层结构相同。写出这些化合物的化学式____________________________________________ 。
24.将30克铁粉(过量)与44mL浓硫酸在加热条件下充分反应,共收集到11.2L(标准状况)气体,其质量为19.6克.试计算:
(1)浓硫酸的物质的量浓度.
(2)反应后剩余铁粉的质量.
高三化学自主复习测试题一:基本概念
23.向碘化钾溶液中加入AgNO3溶液,直到完全反应为止,结果反应后溶液的质量恰好等于原碘化钾溶液的质量,求该硝酸银溶液的质量分数。
24.甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。回答下面问题:
(1)这四种溶液分别是甲:_________、乙:_________、丙:_________、丁:_________。
(2)写出丁与乙反应的离子方程式:________________________________________。
21.(1) 如果Fe3O4可写作FeO·Fe2O3或FeFe2O4,与此类似,Pb3O4则可写作___________或______________。
(2) 写出由化合反应一步制取FeCl2的化学反应方程式:
________________________________________________
(3)高锰酸钾和氢溴酸溶液可以发生下列反应:
KMnO4+ HBr→ Br2+ MnBr2+ KBr+ H2O ①配平上面化学方程式,
②其中还原剂是 ,若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量是 。
(4)①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液到中性,请写出发生反应的离子方程式:_____________________________________。
②在以上中性溶液中,继续滴加 Ba(OH)2溶液, 请写出此反应的离子方程式:_________________________。
20. 实验室有一包 KCl和 AlCl3的固体混合物,通过以下实验可确定 KCl和 AlCl3的质量之比,试根据实验方法和主要步骤,回答有关问题:
(1)调整托盘天平的零点时,若指针偏向右边,应将右边的螺丝向 旋动。
(2)某学生用已知质量为 y g的表面皿准确称取 W g样品,他在托盘天平的右盘上放上(W+y)g的砝码,在左盘的表面皿中放入样品,此时指针稍偏右边,该学生应怎样操作 ;
 (3)将样品置于烧杯中加适量水溶解,滴入过量的A溶液,烧坏中有沉淀物,则A溶液的名称是
;
(3)将样品置于烧杯中加适量水溶解,滴入过量的A溶液,烧坏中有沉淀物,则A溶液的名称是
;
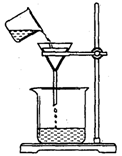
(4)过滤,某学生欲用右图装置操作,错误之处应怎样纠正?
答: ;
(5)甲学生用水多次洗涤过滤所得沉淀物,然后使其干燥,得到固体纯净物C,质量为W2g,C的名称是 ;
6)乙学生将过滤所得滤液跟甲学生洗涤沉淀所得液体混合,然后蒸干溶剂,再充分加热,最后得到纯净KCl固体W1g,则原混合物中KCl与AlCl3的质量之比的计算式为 。
19.某同学配置好两瓶Na2SO4溶液,一瓶为饱和溶液,另一瓶为 0.1 mol·L-1的非饱和溶液,还没来得及贴上标签就搞混了。区别这两种溶液最简单的方法是什么?
答: 。
18.还原2.4×10-3mol XO(OH)3+到X元素的低价态时,消耗0.2mol/L的Na2SO3溶液30mL,则X元素的低价态是( )
A.+1 B.-1 C.0 D.-2
第Ⅱ卷(48分)
17.某实验室用下列溶质配制一种混合溶液,已知溶液中 c(K+)=c(Cl-)=1/2c(Na+)=c(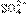 )
)
则其溶质可能是
A.NaCl,K2SO4 B.KCl,Na2SO4,NaCl
C.NaCl,Na2SO4,K2SO4 D.KCl,K2SO4,Na2SO4
16.下列几种方法制备O2:①KClO3 和MnO2共热;②Na2O2加水;③H2O2中加MnO2;④KMnO4受热分解。若要制相同质量的O2,则上述反应中相关物质转移的电子数之比为
A.3:2:2:4 B.1:1:1:1 C.2:1:1:2 D.1:2:1:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com