
题目列表(包括答案和解析)
4.下列实验操作或事故处理中,正确的做法是
A.银镜反应实验后附有银的试管,可用稀H2SO4清洗
B.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次
C.不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗
D.在250mL烧杯中,加入216mL水和24g NaOH固体,配制10% NaOH溶液
3. 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1moIN-N吸收167kJ热量,生成1molN≡N放出942kJ根据以上信息和数据,下列说法正确的是
A.N4属于一种新型的化合物 B.N4与N2互为同素异形体
C.N4沸点比P4(白磷)高 D.1mo1N4气体转变为N2将吸收882kJ热量
2.SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L,下列措施中能够减少SO2排放量的是 ①用天然气代替煤炭做民用燃料 ②使用水煤气或干馏煤气做燃料 ③硫酸厂使用V2O5作催化剂,加快SO2的转化速率 ④将块状煤粉碎,提高其燃烧效率 ⑤在煤中加入石灰后燃用 ⑥循环处理吸收塔放出的尾气
A.①②③④⑤ B.①③⑤⑥ C.①②⑤⑥ D.②③④⑥
1.《科学》评出2004年10大科技突破,其中“火星上‘找’到水的影子”名列第一。下列关于水的说法中错误的是
A.用膜分离的方法可以使海水淡化
B.高效催化剂可使水分解,同时释放能量
C.密度小于1g/cm3的溶液,浓度越大,密度越小
D.金属的电化腐蚀中,水参与了正极反应
33.(1)2CaO2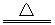 2CaO+O2↑ (2)80.0% (3)
2CaO+O2↑ (2)80.0% (3)
27.(6分)2I-+ClO-+2H+ == I2 + Cl-+H2O; SO32-+I2+H2O== SO42-+2I-+ 2H+;
ClO->I2>SO42-
(1)过氧化钠 (1分)
(2)肯定有NH4+、Al3+、Mg2+、SO42- (2分)
肯定没有Cu2+、Fe2+、HCO3- (2分)
可能有K+ (1分)
(3)①2Na2O2+2H2O=4NaOH+O2↑ ②Al(OH)3+OH-=AlO2-+2H2O (各1分)
(4)NH4+︰Mg2+︰Al3+=0.1︰0.2︰0.1=1︰2︰1(2分)
26.(8分)(1)1、5、8、1、5、4 (2)0.007 (3)19.6 (4)40%
21、(1)使纯碱和H2SO4反应产生的CO2全部排出 NaOH溶液 吸收空气中的CO2 偏大
(2)洗气瓶(图略)浓H2SO4吸水 偏大 (3)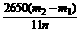 %
%
(4)防止空气中的水汽和CO2进入D被吸收
19.过氧化钙( CaO2)是一种完全无毒的氧化物,通常含有部分CaO,且带有数量不等的结晶水。为分析
某 过氧化钙样品的组成,进行了如下实验:①称取0.270 g样品,灼热使之完全分解,生成CaO、O2和
H2O,得到的O2在标准状况下体积为33.6 mL。②另取0.120 g样品,溶于稀盐酸,加热煮沸,使生成
的H2O2完全分解。然后将溶液中的Ca2+完全转化为CaC2O4沉淀,经过滤洗涤后,将沉淀溶于热的稀硫酸,
用0.02 00 mol/L KMnO4溶液滴定,共用去31.0 mL KMnO4溶液。化学方程式如下:
5CaC2O4+2KMnO4+8H2SO4=K2SO4+2MnSO4+5CaSO4+10CO2↑+8H2O
(1)写出CaO2受热分解的化学方程式。
(2)计算样品中CaO2的质量分数。
(3)计算样品中CaO2·xH2O的x值。
DACCCDBABDDD
18.本题共3小题。
(1)能源是人类社会发展进步的物质基础。在当代,能源同信息、材料一起构成了现代文明的三大支柱。为了降低汽车尾气对大气的污染,江苏有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。请写出表示甲醇燃烧热的热化学方程式
(2)在淀粉KI溶液中滴入少量NaClO溶液,并加入少量硫酸,溶液立即变为蓝色,其反应的离子方程式为 _________________ 。在上述蓝色溶液中滴入足量的Na2SO3溶液,蓝色立即消失,其反应的离子方程式为 ____________________ ,从以上实验可知,ClO-、I2、SO42-的氧化性由强到弱的顺序 ___________________________________。
(3)测定工业甲醇中CH3OH的质量分数可按下法:取0.1000g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL 0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点。
已知:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②此工业甲醇中CH3OH的质量分数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com