
جâؤ؟ءذ±ي(°üہ¨´ً°¸؛ح½âخِ)
8£®¼×،¢زز،¢±û،¢¶،¸÷تاNa2SO3،¢AgNO3،¢HCl،¢BaCl2ثؤضضخقة«بـز؛ضذµؤز»ضض£¬ثüأاء½ء½·´س¦؛َµؤدضدَبçدآ£؛
¼×+زز،ْ³ءµي،، ¼×+±û،ْ³ءµي،، زز+±û،ْ³ءµي،،
±ûت®¶،،ْ³ءµي،، زز+¶،،ْخقة«´ج¼¤ذشئّخ¶ئّجه£¬
شٍ¼×،¢زز،¢±û،¢¶،زہ´ختا(،،،،،، )
A،، Na2SO3،، HCl،، AgNO3،، BaCl2،،،،،،،،
B،، BaCl2،، Na2SO3،، HCl،، AgNO3
C،، BaCl2،، Na2SO3،، AgNO3،، HCl،،،،
D،، AgNO3،، HCl،، BaCl2،، Na2SO3
7£® شعتµرéتزہï؟ة°´ح¼ثùت¾µؤ×°ضأہ´¸ةشï،¢تص¼¯ئّجهR£¬¶àسàµؤئّجهR؟ةسأث®خüتص£¬شٍRتا،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،
،،،،
شعتµرéتزہï؟ة°´ح¼ثùت¾µؤ×°ضأہ´¸ةشï،¢تص¼¯ئّجهR£¬¶àسàµؤئّجهR؟ةسأث®خüتص£¬شٍRتا،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،
،،،،
A.HCl،،،،،،،،،،،، ،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،
B.Cl2،،،،،،،،،،،،
C.CO،،،،،،،،،،،،
D.NH3
6£®شعجه»دàح¬µؤء½¸ِأـ±صبفئ÷ضذ·ض±ً³نآْO2،¢O3ئّجه£¬µ±صâء½¸ِبفئ÷ؤعخآ¶ب؛حئّجهأـ¶بدàµبت±£¬دآءذثµ·¨صب·µؤتا
A£®ء½ضضئّجهµؤر¹ا؟دàµب،،،،،،،، ،،،،،،،،،، B£®O2±بO3ضتء؟ذ،
C£®ء½ضضئّجهµؤ·ض×ستؤ؟دàµب،،،، ،،،،،،،،،، D£®ء½ضضئّجهµؤرُش×ستؤ؟دàµب
5£®°¢·ü¼سµآآق³£تش¼خھ6.02،ء1023mol-1£¬دآءذذًتِضذصب·µؤتا
A£®31g °×ء×·ض×س(P4)ضذ؛¬سذP-P¼ü¸ِتخھ1.5،ء6.02،ء1023
B£®48gO2؛ح48gO3ثù؛¬·ض×ستخھ3،ء6.02،ء1023
C£®1.0L 1mol/L°±ث®ضذ£¬NH3،¤H2Oµؤ·ض×ستخھ6.02،ء1023
D£®20g ضطث®(D2O)ضذ؛¬سذµؤضذ×ستخھ8،ء6.02،ء1023
4£®زرضھ³ن·ضب¼ةصa gززب²ئّجهةْ³ة1molCO2ئّجه؛حز؛ج¬ث®£¬²¢·إ³ِببء؟b kJ£¬شٍززب²ب¼ةصµؤبب»¯ر§·½³جت½صب·µؤتا،،،، ،،،،،،،، (،،،، )
،،،، A£®2C2H2(g)+5O2(g)،، 4CO2(g)+2H2O(l)£»،÷H=£2b kJ/mol
،،،، B£®C2H2(g)+5/2O2(g)،، 2CO2(g)+H2O(l)£»،÷H=+2b kJ/mol
،،،، C£®2C2H2(g)+5O2(g)،، 4CO2(g)+2H2O(l)£»،÷H=£4b kJ/mol
،،،، D£®2C2H2(g)+5O2(g)،، 4CO2(g)+2H2O(l)£»،÷H=+b kJ/mol
3£®دآءذہë×س·½³جت½تéذ´²»صب·µؤتا (،،،، )
A،، دٍ´؟¼îبـز؛ضذ¼سبë´×ثلبـز؛،،،،
CO32£+2H+=CO2،ü+H2O
B£®شعآب»¯آءبـز؛ضذ¼سبë¹ء؟°±ث®،،،، Al3+ + 3NH3،¤H2O = Al(OH)3،+3NH4+،،،،،،،،،،
C£®شعج¼ثلاâؤئبـز؛ضذ¼سبëµبخïضتµؤء؟µؤاâرُ»¯±µبـز؛،،،،،،
HCO3£+OH£ + Ba2+ =،، BaCO3،+H2O
D£®شعءٍثلاâؤئبـز؛ضذ¼سبëµبخïضتµؤء؟µؤاâرُ»¯±µبـز؛،،،،،،،،،،،،
H+ + SO42£ + Ba2+ + OH£= BaSO4، + H2O
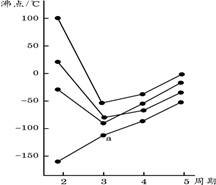
2£®سزح¼ضذأ؟جُصغدك±يت¾ضـئع±ي¢ôA-¢÷Aضذµؤؤ³ز»×هشھثطا⻯خïµؤ·ذµم±ن»¯£¬أ؟¸ِذ،؛عµم´ْ±يز»ضضا⻯خئنضذaµم´ْ±يµؤتا
A.H2S،،،،،، B.HCl،،،، C.PH3،،،،،،،،،،،، D.SiH4
1،¢2006ؤê3شآ5بص£¬خآ¼ز±¦شعت®½ىب«¹ْبث´َثؤ´خ»لزéةدثù×÷µؤ،°ص¸®¹¤×÷±¨¸و،±ضذض¸³ِ£؛،°×¥؛أ×تش´½عش¼£¬½¨ةè»·¾³سر؛أذحةç»ل،±£¬صâتاخز¹ْةç»ل¼°¾¼أ³¤ئع·¢ص¹µؤضطزھ±£ض¤،£ؤمبدخھدآءذذذخھضذسذم£سعصâز»±£ض¤µؤتا،،،،،،،،،، (،،،، )
A£®؟ھ·¢ج«رôؤـ،¢ث®ؤـ،¢·çؤـ،¢؟ةب¼±ùµبذآؤـش´،¢¼ُةظت¹سأأ؛،¢ت¯سحµب»¯ت¯ب¼ءد
B£®½«أ؛½ّذذئّ·¨´¦ہي£¬جل¸كأ؛µؤ×غ؛دہûسأذ§آت
C£®رذ¾؟²ةأ؛،¢²ةسحذآ¼¼تُ£¬ازجل¸ك²ْء؟زشآْ×م¹¤زµةْ²ْµؤ؟ىثظ·¢ص¹
 D£®تµدض×تش´µؤ،°3R،±ہûسأ¹غ£¬¼´£؛¼ُةظ×تش´دû؛ؤ(Reduce)،¢شِ¼س×تش´µؤضط¸´ت¹سأ(Reuse)،¢×تش´µؤر»·شظةْ(Recycle)
D£®تµدض×تش´µؤ،°3R،±ہûسأ¹غ£¬¼´£؛¼ُةظ×تش´دû؛ؤ(Reduce)،¢شِ¼س×تش´µؤضط¸´ت¹سأ(Reuse)،¢×تش´µؤر»·شظةْ(Recycle)
23£®(13·ض)زرضھAخھضذر§»¯ر§ضذµؤ³£¼û½ًتô£¬X،¢Yخھ³£¼û·ا½ًتô£¬A،¢X،¢Y¶¼خ»سعضـئع±يضذ¶جضـئع،£ئنضذA،¢Y³£خآدآخھ¹ججه£¬X،¢E،¢F،¢G،¢J³£خآدآخھئّجه£¬Cخھخقة«ز؛جه£¬Bتاز»ضضرخ£¬تـببز×·ض½â£¬·ض½â²ْخïخھE؛حHCl،£دضسأAسëت¯ؤ«×÷µç¼«£¬BCYµؤإ¨بـز؛×÷µç½âضت£¬¹¹³ةشµç³ط،£سذ¹طخïضتض®¼نµؤ×ھ»¯¹طدµبçدآح¼(²؟·ض·´س¦µؤجُ¼،¢ةْ³ةخï±»آشب¥)£؛
 ،،
،،
،،
،،
اëجîذ´دآءذ؟ص°×£؛
،، (1)½ًتôAخھ،،،،،،،،،، ،،£»²ظ×÷aتا½«Dبـز؛شعHClئّء÷ضذصô¸ة£¬شزٍتا،،،،،،،،،،،،،، ،،
،،،،،،،، ،،،،،،،،،،،،،،،،،،،،،،،،،£
،، (2)·´س¦¢عµؤ»¯ر§·½³جت½خھ£؛،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،، ،،£»
،،،،،،،، ·´س¦¢فµؤ»¯ر§·½³جت½خھ£؛،،،،،،،،،،،،،،،، ،،،،،،،،،،،،،،،،،،،،،،،،،،،£
،، (3)شµç³ط·´س¦¢ظضذ£¬ص¼«·´س¦ت½خھ£؛،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،، ،£
22£®(11·ض)ؤ³رذ¾؟ذشر§د°ذ،×éخھ²â¶¨ؤ³FeCl3رùئ·(؛¬ةظء؟FeCl2شسضت)ضذجْشھثطµؤضتء؟·ضت£¬ةè¼ئءثبçدآتµرé²½ضè£؛
¢ظ×¼ب·³ئء؟رùئ·ضتء؟a g£»
¢عدٍرùئ·ضذ¼سبë10mL 6mol،¤L-1µؤرخثل£¬رùئ·بـ½â؛َشظ¼سبëصôءَث®إن³ة100mLبـز؛;
¢غدٍةدتِبـز؛ضذ¼سبë3mLآبث®£¬½ء°èت¹ئن·´س¦حêب«£»
¢ـ¼سبë10%µؤ°±ث®ضء¹ء؟£¬³ن·ض½ء°è£¬ت¹³ءµيحêب«£»
¢ف¹آث£¬½«³ءµيد´µس؛َ¸ةش
¢ق½«³ءµيزئضءغلغِضذ£¬×ئةص،¢ہنب´،¢³ئضط£¬²¢·´¸´²ظ×÷¶à´خضء¹ججهحêب«·´س¦،£تش»ط´ًختجâ:
(1)ذ´³ِ²½ضè¢ـضذ²ْةْ³ءµيµؤہë×س·½³جت½£؛________________________،£
(2)ب·بد²½ضè¢ـ³ءµيزر¾حêب«µؤ·½·¨تا____________________________________،£
(3)د´µس³ءµيµؤ²ظ×÷·½·¨تا______________________________________________£»
بç؛خ¼ىرé³ءµيتا·ٌد´¾»£¬ئن·½·¨تا________________________________________،£
(4)شع²½ضè¢قضذ£¬إذ¶د¹ججه·´س¦حêب«µؤ·½·¨تا£؛،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،،
(5)بô؟صغلغِضتء؟خھb g£¬³ن·ض×ئةص¹ججهحêب«·´س¦؛َ£¬ت£سà¹ججه؛حغلغِµؤ×ـضتء؟خھ
c g£¬شٍرùئ·ضذجْشھثطµؤضتء؟·ضتتا______________________،ء100%
¹ْ¼تر§ذ£سإر، - ء·د°²لءذ±ي - تشجâءذ±ي
؛±±ت،»¥ءھحّخ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨ئ½ج¨ | حّةدسذ؛¦ذإد¢¾ظ±¨×¨اّ | µçذإص©ئ¾ظ±¨×¨اّ | ةوہْت·ذéخقض÷زهسذ؛¦ذإد¢¾ظ±¨×¨اّ | ةوئَاضب¨¾ظ±¨×¨اّ
خ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨µç»°£؛027-86699610 ¾ظ±¨ستدن£؛58377363@163.com