
题目列表(包括答案和解析)
25.(6分)(1)H 、O(2分); (2)HS- + OH- =S2-+ H2O(2分);
(3)正极(1分),H2 + 2OH--2e- == 2H2O(1分)
24.(6分)(1)②;(2)PCl3或CCl4、第3周期ⅥA族、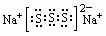 ;(3)KC8
;(3)KC8
23.(4分)(1)K2O·2UO3·V2O5·3H2O(2分) (2)H2C2O4(1分) 0.51(1分)
22.(6分)VIA(1分) ⅣA(1分)、随着相对分子质量增大,分子间作用力增大(2分)
它们分子间存在氢键,分子间作用力增大(2分)
21.(8分)A:NH3 B:HCN C:CO(NH2)2 D:BF3
第Ⅱ卷(非选择题,共60分)
30.(6分)某天然碱的组成为x Na2CO3·yNaHCO3· zH2O,将称取的4.56g样品于300℃加热分解至完全(300℃ Na2CO3不分解),得到残留固体3.71g,分解产生的气体通入足量饱和的澄清石灰水中,完全吸收后可得到0.500g沉淀。请计算:
(1)该样品中结晶水的质量分数;
(2)通过计算确定该天然碱的化学式。
高三第二次月考化学试卷评分标准
第Ⅰ卷(选择题,共40分)
29.(6分)钙是人体神经、肌肉、骨骼系统、细胞膜和毛细血管通透性的功能正常运作所必需的常量元素,维生素D参与钙和磷的代谢作用,促进其吸收并对骨质的形成和改善有重要的作用。某制药有限公司生产的“钙尔奇D600片剂”的部分文字说明如下:“本品每片含主要成分碳酸钙1.5 g(相当于钙元素600 mg),成人每天服用1片。”
(1)“1.5 g碳酸钙与600 mg的钙”的计量关系是如何得出来的,请列式表示;
(2)该公司的另一种产品,其主要成分与“钙尔奇D600”相同,仅仅是碳酸钙的含量不同。为测定该片剂中碳酸钙含量,某学生进行了如下的实验:取一片该片剂碾碎后放入足量的HCl中(假设该片剂的其余部分不与HCl 反应)过滤,取滤液加 (NH4)2C2O4,使Ca2+ 生成CaC2O4沉淀,沉淀过滤洗涤后溶解于强酸中,并稀释成1L溶液,取其20mL,然后用0.01 mol/L KMnO4 溶液滴定,反应中用去6 mL KMnO4溶液,发生的离子反应为:
2MnO4― + 5H2C2O4 + 6H+ == 2Mn2+ + 10CO2↑+ 8H2O
试通过计算回答该片剂中碳酸钙的含量,并仿照药品说明书的文本表达出来。
28.(6分)亚硝酸钠NaNO2可用做水泥施工的抗冻剂。它易溶于水,有咸味,既有氧化性,又有还原性。在酸性溶液中它能氧化碘离子、亚铁离子。它能将人体内血红蛋白里的亚铁离子氧化为三价铁离子而使人中毒,在建筑工地上多次发生把亚硝酸钠误作食盐食用,导致民工中毒的事件。亚硝酸钠和酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生如下反应:3HNO2 == 2NO↑+ HNO3 + H2O。
试从浓醋酸、氨水、纯碱、稀盐酸、碘化钾淀粉溶液中选择适当的物质作试剂,用两种简单的化学实验鉴别亚硝酸钠和氯化钠。
(1)方法一(只用一种试剂),试剂 ▲ ,现象 ▲ ;
(2)方法二,试剂 ▲ ,现象 ▲ ,写出反应的离子方程式是 ▲ 。
27.(6分)请设计实验用氯化钙固体和其他有关试剂(硝酸银价格昂贵不能使用),制取一定量纯净的硝酸钙固体。
(1)写出表示制取硝酸钙的化学方程式: ▲ , ▲ ;
(2)简述实验的操作步骤(不要求回答使用的仪器,但要求回答试剂的用量:少量、适量或过量) ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com