
题目列表(包括答案和解析)
23.(4分)1840年盖斯根据一系列实验事实得出规律,他指出:若是一个反应可以分几步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。已知热化学方程式:
C(S,金刚石) + O2(g) = CO2(g);△H = -395.41KJ/mol
C(S,石墨) + O2(g)= CO2(g);△H = -393.51KJ/mol
则金刚石转化为石墨的热化学方程式为 ▲ ,由热化学方程式看来更稳定的碳的同素异形体是 ▲ 。
22.(6分)在淀粉KI溶液中滴入少量NaClO溶液,并加入少量硫酸,溶液立即变为蓝色,其反应的离子方程式为 ▲ 。在上述蓝色溶液中滴入足量的Na2SO3溶液,蓝色立即消失,其反应的离子方程式为 ▲ ,从以上实验可知,ClO-、I2、SO42-的氧化性由强到弱的顺序是 ▲ 。
21.(8分)2gCu2S 和CuS 的混合物在酸性溶液中用400mL0.075mol /L KMnO 4溶液处理,发生反应如下:8MnO 4-+5 Cu2S+44H+=10Cu 2++5SO 2+8Mn 2++22H2O;
6MnO 4-+5 CuS+28H+=5 Cu 2++5SO 2+6Mn 2++14H2O。反应后煮沸溶液,赶尽SO2,剩余的KMnO 4恰好与350mL0.1mol/L(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
MnO 4-+ Fe2+ + H+= Mn2++ Fe3++ H2O;
(2)KMnO 4溶液与混合物反应后,剩余KMnO 4的物质的量为 ▲ mol;
(3)欲配制500mL0.1 mol /L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为 ▲ g;
(4)混合物中Cu2S的质量分数为 ▲ 。
20.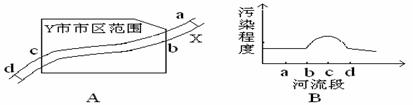 城市环境污染是当前突出的环境问题。如图A所示,X河流经某工业城市Y,其中a处在上游,附近有丰富的黄铁矿资源,d处在下游有多个企业以硫酸为原料。根据某月Y市环保局监测站对X河水质检测的结果,绘制成简图如图B所示。下列说法不正确的是
城市环境污染是当前突出的环境问题。如图A所示,X河流经某工业城市Y,其中a处在上游,附近有丰富的黄铁矿资源,d处在下游有多个企业以硫酸为原料。根据某月Y市环保局监测站对X河水质检测的结果,绘制成简图如图B所示。下列说法不正确的是
A.造成X河污染的主要污染源最可能分布在bc段
B.工业废水、生活污水、固体废弃物等可能是造成X河污染的污染源
C.d处污染程度减小,可能是某些污染物的离子间发生反应生成沉淀所致
D.该城市建造硫酸厂时,综合考虑诸多因素选址在b处最合理。
第Ⅱ卷(非选择题,共60分)
19.有关接触法制硫酸的叙述中,不正确的是
A.用硫铁矿代替硫,可减少环境污染
B.SO2进接触室前要净化,以免催化剂中毒
C.热交换的目的,一方面使即将参加反应的气体达到一定温度,另一方面降低SO3的温度
D.尾气经过处理后才能排放到空中
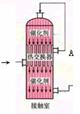
18.右图为接触室的示意图,从A处出来的气体为
A.SO2 B.SO3、O2 C.SO2、O2 D.SO2、SO3、O2
17.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放
 电电压。高铁电池的总反应为:
电电压。高铁电池的总反应为:
下列叙述不正确的是
A.放电时负极反应为:Zn-2e- +2OH- = Zn(OH)2
 B.充电时阳极反应为:Fe(OH)3 -3e- + 5OH- = FeO42- + 4H2O
B.充电时阳极反应为:Fe(OH)3 -3e- + 5OH- = FeO42- + 4H2O
C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
16.下列描述中,不符合生产实际的是
A.电解熔融的氧化铝制取金属铝,用铁作阳极 B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 D.在镀件上电镀锌,用锌作阳极
15.某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3∶1。用石墨作电极电解该混合溶液时,根据电极产物,可明显分为三个阶段。下列叙述不正确的是
A.阴极自始自终只析出H2 B.溶液pH不断增大,最后为7
C.电解最后阶段为电解水 D.阳极先析出C12,后析出O2
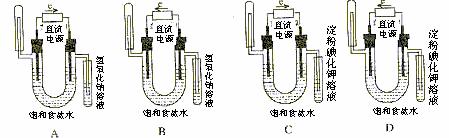
14.下图中验证氯化钠溶液(含酚酞)电解产物的装置是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com