
题目列表(包括答案和解析)
29.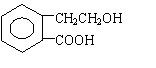 (12分)有机物A的结构简式为
,它可通过不同化学反应分别制得B、C、D和E四种的物质。
(12分)有机物A的结构简式为
,它可通过不同化学反应分别制得B、C、D和E四种的物质。
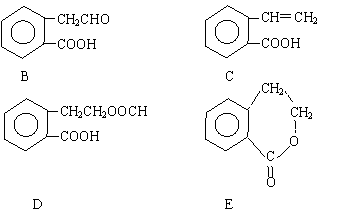
请回答下列问题:
(1)指出反应的类型:A→C:__________________。
(2)在A~E五种物质中,互为同分异构体的是 (填代号)。
(3)写出由A生成D的化学方程式 。
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是_________(填序号)。
(5)C能形成高聚物,该高聚物的结构简式为 。
28.(15分)甲、乙、丙、丁、戊分别是Na2SO4、Ba(NO3)2、HNO3、BaCl2、NaOH五种溶液中的一种,现利用X(一种钠盐)溶液鉴别它们,已知气体B的密度在同温同压下是氢气密度的22倍。试根据下图中的转化关系回答问题:

(1)下列物质的化学式分别为:
甲 、 乙 、丙 、
丁 、X ;
(2)戊的电子式为 ;
(3)白色沉淀A与乙反应的化学方程式为 。
27.(15分)已知A、B、C是第二周期的非金属元素,其原子序数依次增大,且它们之间可以形成AC和BC以及AC2和BC2分子,D元素是一种短周期元素,它与A、B、C可分别形成电子总数相等的三种分子.请填空:
(1) 写出A、B、C、D对应的元素符号:A.______、B.______、C.______、D._____.
(2) 写出工业生产中BD3与氧气反应的化学方程式:__________________________.
(3) 你认为B、C、D元素形成的化合物之间能否_____________(填:“能”或“不能”)发生下面的反应BC+BD3→DBC2+D2C,得出上面结论的理由是__________________
____________________________________________.
(4) Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g) 4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是_____________(用含a的代数式表示);
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是_____________(用含a的代数式表示);
Ⅱ.若维持温度不变,在一个与Ⅰ反应前的起始体积相同容积固定的密闭容器中发生Ⅰ中所述的化学反应,开始时仍向容器中充入AC和BC2各1mol,达平衡时生成AC2和B2共bmol,将b与Ⅰ中的a进行比较,则a_____b(填“>”、“<”、“=”或“不能确定”).
26.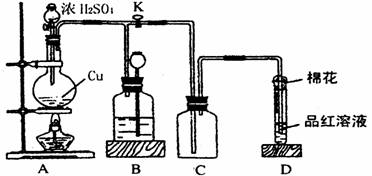 (18分)某化学兴趣小组为探究铜跟浓硫酸的反应,用下图所示装置进行有关实验。请回答:
(18分)某化学兴趣小组为探究铜跟浓硫酸的反应,用下图所示装置进行有关实验。请回答:
(1)装置A中发生的化学反应方程式为_____________________ 。
(2)装置D中试管口放置的棉花中应浸一种液体,这种液体是 ,其作用是 。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
_________________________________。B中应放置的液体是(填字母)____________。
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(4)实验过程中有时打开A装置中分液漏斗的活塞时,漏斗中的浓硫酸不能顺利滴入烧瓶中,可能的原因是 。
(5)实验中,取一定质量的铜片和一定体积18 mol · L – 1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是_____________
_______________________________________________________________。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________(填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
13.下列排列顺序错误的是 ( )
A.酸性}:H4SiO4<H3PO4<H2SO4<HClO4
B.碱性 KOH>Ca(OH)2>Mg(OH)2>Al(OH)3
C.原子半径F<O<S<Na
D.氢化物的稳定性SiH4>H2S>H2O>HF
12.pH=2的两种一元酸HA和HB分别与足量锌粉反应,所生成的H2体积V(HA)>V(HB)。
下列说法正确的是 ( )
A.酸的物质的量浓度c(HA)一定大于c(HB)
B.HB一定不是弱酸
C.若两种酸体积相同,则HB的酸性比HA酸性强
D.这两种酸的物质的量浓度一定相同而体积不同
11.在一定温度下,NO2(g)转化为N2O4(g)是一个放热反应。在一个密闭容器中达到平衡后,改变下列条件,下列说法中错误的是 ( )
A.加压使体积变小,将使正、逆反应速率均增大,平衡时颜色加深
B.保持体积不变,加入少量NO2(g),将使逆反应速率减小
C.保持体积不变,升高温度,再达到平衡时混合物的颜色加深
D.保持体积不变,加入少量N2O4(g),再达到平衡时NO2(g)的体积分数变小
10.八角茴香含有一种抗H5N1型禽流感病毒的重要成分--莽草酸,其分子结构如图。下列关于莽草酸的说法错误的是 ( )
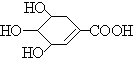 A.莽草酸分子式为C7H10O5
A.莽草酸分子式为C7H10O5
B.莽草酸能使溴水褪色
C.莽草酸遇FeCl3溶液不发生显色反应
D.1mol莽草酸可以与4molNaOH反应
9.通常条件下,下列各组物质不能用一种试剂通过化学反应区别的是 ( )
A.AgNO3 NaNO3 Na2CO3 B.Na2CO3 NaHCO3 K2CO3
C.MnO2 FeO CuO D.(NH4)2SO4 Na2SO4 NH4C1
8.下列说法或表示方法正确的是 ( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(石墨)→C(金刚石);△H= +1.91 kJ/mol,可知金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)==H2O(1);△H= -57.3 kJ/mol,若将含0.5 molH2SO4的浓硫酸与含l mol NaOH的稀溶液混合,放出的热量大于57.3 kJ
D.在101 kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)==2H2O(1);△H= +285.8 kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com