
题目列表(包括答案和解析)
18.如图,铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是
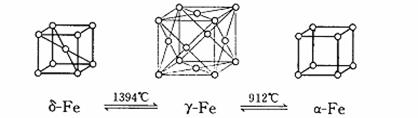
A.δ-Fe晶体中与每个铁原子距离相等且最近的铁原子有8个
B.α-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
C. 若δ-Fe晶胞边长为acm,α-Fe晶胞边长为bcm,则两种晶体密度比为2b3:a3
D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型相同
17、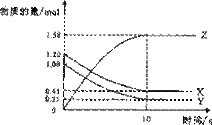 一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述不正确的是
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述不正确的是
A、从反应开始到10s时,用Z表示的反应速率为0.158mol/L·s
B、从反应开始到10s时,X的物质的量减少了0.79mol
C、从反应开始到10s时,Y的转化率为79.0%
D、反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
16. 锂电池用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯( 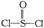 )中形成的,以下电池的总反应方程式为:8Li+3SOCl2=6LiCl+ Li2SO3+2S,下列叙述中正确的是
)中形成的,以下电池的总反应方程式为:8Li+3SOCl2=6LiCl+ Li2SO3+2S,下列叙述中正确的是
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的负极,石墨作电池的正极
C. 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供电子的物质的量与析出硫的物质的量之比为4 :1
15.为确定某溶液的离子组成,进行实验:①测定溶液的pH值,溶液显强碱性;
②取少量溶液加稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体;
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀;
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀;
根据以上实验,以下对原溶液的推测正确的是
A.一定有CO32-离子存在 B.不能确定是否存在HCO3-离子存在
C.一定有C1-离子存在 D.一定有SO32-离子存在
14.碳的第五种同素异形体很轻,像泡沫一样,被称为纳米泡沫。在纳米泡沫中,碳以七边形的方式结合,有一个未成对的电子;现代医疗中,可以用纳米泡沫来把肿瘤包裹起来,以红外线加热摧毁肿瘤,却不伤害外围组织。下列关于纳米泡沫的性质推断不正确的是
A.具有磁性 B.具有良好导热性 C.具有可燃性 D.能和盐酸反应
13、下列有关说法正确的是
A.H2SO4的酸性比HClO的酸性强,所以S的非金属性比Cl强
B.Mg(OH)2是中强碱,Al(OH)3是两性氢氧化物,所以Al的金属性比Mg强
C.H2O加热到1000℃开始分解,H2S加热到300℃开始分解,则O的非金属性比S强
D.用Na、Mg分别做与水反应的实验,可以比较它们的金属性强弱
12.下列离子方程式中,书写不正确的是:
A. 常温下,Cl2与NaOH溶液反应: Cl2 + 2OH- Cl-+ ClO-+ H2O
B. 澄清石灰水与少量小苏打溶液混合:Ca2+
+ OH-
+ HCO3- CaCO3↓
+ H2O
C. 稀H2SO4与Ba(OH)2溶液反应: Ba2++ OH-+ H+十SO42- BaSO4↓+ H2O
D. 氯化亚铁溶液中通入氯气: 2Fe2+ + Cl2
2Fe3+ + 2Cl-
11. X、Y、Z为短周期元素,这些元素原子的最外层电子数分别是1、4、6.则由这三种元素组成的化合物的化学式不可能是
A. XYZ B. X2YZ C. X2YZ2 D . X2YZ3
10. 用铝箔包住0.2mol金属钠,然后用针扎若干小孔,放入水中,完全反应后,用排水集气法收集到的气体(标准状况下)为 A. H2和O2的混合气体 B.= 2.24L H2 C. >2.24L H2 D.< 2.24L H2
9.某温度下,ClF(g)+F2(g)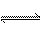 ClF3(g)
△H=-268kJ•mol-1,在密闭容器中达到平衡。下列说法正确的是
ClF3(g)
△H=-268kJ•mol-1,在密闭容器中达到平衡。下列说法正确的是
A.温度不变,增大体积,ClF3产率提高
B.温度不变,缩小体积,ClF转化率增大
C.体积不变,升高温度,平衡向正反应方向移动
D.体积不变,降低温度,ClF3的体积分数减小
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com