
题目列表(包括答案和解析)
31.(6分)下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。
(b)反应①②是化工生产中的重要反应。
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。
(e)化合物J由两种元素组成,其相对分子质量为32。

请按要求填空:
⑴反应③的化学方程式 。
⑵H的化学式 。
⑶L的溶液与化合物E反应的离子方程式 。
⑷化合物J的化学式 。
30.(12分)已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
I.若甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
a.甲+H2O 乙+丙 b.乙
乙+丙 b.乙 氧化物丁+H2O
氧化物丁+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则该金属在周期表中的位置是__________________。
②若甲为某短周期金属元素的氯化物,且氧化物丁既能与强酸又能与强碱溶液反应,则该金属的原子结构示意图 ____________________________________。
③将以上两种金属单质用导线连接,插入一个盛有NaOH溶液的烧杯中构成原电池,则负极发生的电极反应为 。
II.若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙 丙。则:
丙。则:
①甲的结构式为 。
②写出上述反应的化学方程式 。
③向NaOH溶液中通入气体甲,由于气体甲通入量不同,所得到的溶液中溶质的组成也不同,试推断其反应后的溶液中溶质有可能的组成,请分别列出
。
4写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生完全反应的总离子方程式 。
29. (9分)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式: 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
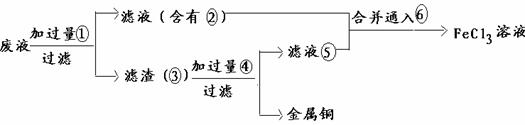
(4)请写出上述实验中3的化学式:
(5)配制硫酸亚铁溶液时,常在其中加入
(6)要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为 。
1加入足量氯水2加入足量NaOH溶液3加入少量KSCN溶液
A、13 B、32 C、31 D、123
(7)写出向25的混合液中通入6的离子方程式 。
28. (9分)下表是元素周期表中短周期元素部分,表中字母分别代表一种元素:
|
a |
|
b |
|||||
|
|
|
|
d |
e |
f |
|
|
|
c |
|
|
g |
|
|
h |
|
(1)上述 元素(填字母代号)可以形成硬度最大的单质。
(2)“神舟”六号飞船内需要有一种化合物来吸收宇航员呼出的 CO2,你认为该物质应该是由上表中的 和 元素(填字母代号)组成的,写出该化合物与CO2反应的化学方程式并用双线桥法表示电子转移情况 。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子的结构式是 。
 (3)表中元素g的氢化物热稳定性比元素e的氢化物的热稳定性
(填“强”或“弱”)。
(3)表中元素g的氢化物热稳定性比元素e的氢化物的热稳定性
(填“强”或“弱”)。
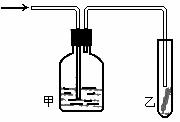
(4)将潮湿的由h元素构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是
①浓硫酸 ②NaOH溶液 ③KI溶液 ④饱和食盐水
27.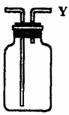 (3分) 现有下图所示装置,正放在桌面上,可分别实现下列实验目标,其中适用于从Y口进入的是(填字母)
(3分) 现有下图所示装置,正放在桌面上,可分别实现下列实验目标,其中适用于从Y口进入的是(填字母)
A.瓶内盛一定量液体干燥剂,用于干燥气体
B.瓶内盛一定量液体试剂,用于除去气体的杂质
C.瓶内盛一定量水,用于制得可溶于水的气体的饱和溶液
D.瓶内盛满水,用于测量难溶性气体的体积
E.一般用于向上排气法收集某些气体
F.一般用于向下排气法收集某些气体
26.(11分)喷泉实验是中学化学的一个重要性质实验,也是一种自然现象。其产生的原因是存在压强差。试根据附图,回答下列问题:
(1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
 A.HCl和H2O
B.NH3和H2O C.NH3和苯 D.CO2和烧碱溶液
A.HCl和H2O
B.NH3和H2O C.NH3和苯 D.CO2和烧碱溶液
(2)图B的锥形瓶中分别加入足量的下列物质,反应后能产生喷泉现象的是
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液C.大理石与稀硫酸 D.碳铵与稀硝酸
(3)若图B的锥形瓶内是无水酒精,水槽内是冷水,则向水槽中加入足量的下列哪些物质也会产生喷泉现象?
A.浓硫酸 B.生石灰 C.氢氧化钡晶体与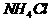 固体 D.氢氧化钠固体
固体 D.氢氧化钠固体
(4)城市中常见的人造喷泉及火山喷发的原理与上述 装置的原理相似。(5)如果只提供如图C的装置,引发喷泉的方法是
。
(6)写出实验室制取氨气的化学方程式: ,氨分子的结构式为 ,其空间构型为 。
25. 50 mL 0.2 mol/L AlCl3溶液中加入2 mol/L NaOH溶液a mL后,再滴加1 mol/L盐酸。滴加盐酸的体积(横坐标)与生成沉淀的质量(纵坐标)如图示的关系,则加NaOH溶液的体积为
( )
50 mL 0.2 mol/L AlCl3溶液中加入2 mol/L NaOH溶液a mL后,再滴加1 mol/L盐酸。滴加盐酸的体积(横坐标)与生成沉淀的质量(纵坐标)如图示的关系,则加NaOH溶液的体积为
( )
A.10 mL B.25 mL
C.50 mL D.60 mL
高密二中2006--2007学年度上学期十月份质量检测考试
高三化学试题
第Ⅱ卷(非选择题,共50分)
① 凡元素符号、化学式有错及化学专用词语出现错别字的,有关内容不得分。
② 各种化学方程式没配平的,均不得分。
3 答题时,若只答出含义而未答出要点的,有关内容不得分;没有用化学专用词语答题者,有关内容不得分。
24.如图,B为常见金属或非金属单质,有下列转化关系:
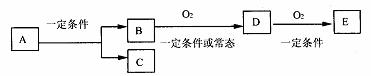
若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是 ( )
A.AlCl3 B.H2O2 C.KCl D.NaCl
23.铝、铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低。已知反应:BeCl2 + Na2BeO2 + 2H2O == 2NaCl + 2Be(OH)2↓能完全进行,则下列推断正确的是 ( )
A.Na2BeO2溶液的 pH > 7,将其蒸干并灼烧后得到的残留物为BeO
B.BeCl2溶液的pH < 7,将其蒸干并灼烧后得到的残留物可能是BeO
C.Be(OH)2能溶于盐酸,不能溶于NaOH溶液
D.BeCl2水溶液的导电性强,故BeCl2是离子化合物
22.某未知盐溶液中可能存在X、Y两种离子,欲用Z试剂来检验盐溶液中是否存在X离子,Y离子不会干扰的是( )
|
试剂Z |
离子X |
离子Y |
|
A.NH3·H2O |
Al3+ |
Mg2+ |
|
B.AgNO3 |
Cl- |
 |
|
C.Na2S |
Cu2+ |
Fe2+ |
|
D.Ba(NO3)2 |
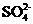 |
Cl- |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com