
题目列表(包括答案和解析)
10.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
A.滴加石蕊试液显红色的溶液:Fe3+ 、NH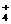 、Cl- 、SCN-
、Cl- 、SCN-
B.pH值为1的溶液:Cu2+、Na+ 、Al3+、NO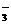
C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO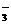 、Br-、Ba2+
、Br-、Ba2+
D.所含溶质为Na2SO4的溶液:K+ 、CO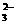 、NO
、NO 、 Mg2+
、 Mg2+
9.在25℃时,将两个惰性电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,阴极上逸出a mol气体,同时有w g Na2SO4 ·10 H2O晶体析出,若温度不变,则剩余溶液中溶质的质量分数为 ( )
A.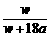 × 100% B.
× 100% B.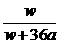 × 100%
× 100%
C.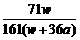 × 100% D.
× 100% D. × 100%
× 100%
8.用惰性电极电解100mL浓度为0.05mol/L的CuSO4溶液,通电一段时间,Cu2+恰好反应完全,若溶液体积仍为100mL,此时溶液的pH为 ( )
A.1 B.2 C.12 D.13
7.下列离子反应方程式正确的是 ( )
A.铜和硫酸锌溶液:Cu + Zn2+= Cu2++ Zn
B.澄清的石灰水中加入少量NaHCO3溶液:Ca2++2OH-+2HCO3- = CaCO3↓+2H2O+CO32-
C.少量的盐酸逐滴滴入碳酸钠溶液:CO32-+2H+=CO2↑+H2O
D.溴化亚铁溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl-
6.最近我国某近代物理研究所取得重大科研成果,研制出首批氧-18气体(18O2),氧-18是一种稳定的氧的同位素,称为重氧。下列有关说法正确的是 ( )
A.1.8g氧-18气体(18O2)的物质的量是0.1mol
B.0.1mol重氧水H218O所含的中子数为6.02×1023
C.0.2mol氧-18气体(18O2)的体积约为4.48L
D.氧-18气体的摩尔质量是36g
5.根据磷元素的原子结构示意图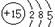 ,做出如下推理,其中与事实不符的是 ( )
,做出如下推理,其中与事实不符的是 ( )
A.磷元素位于元素周期表的第三周期、第VA族
B.磷原子不如氮原子和硫原子的得电子能力强
C.磷单质不如氮气和硫单质活泼
D.磷的氢化物(PH3)受热时不如氮的氢化物(NH3)和硫的氢化物(H2S)稳定
4.下列各物质中,所有原子都满足最外层为8电子结构的是 ( )
A.BeCl2 B.PCl3 C.PCl5 D.NH3
3.FeCl3溶液、Fe(OH)3 胶体共同具备的性质是 ( )
A.加入饱和MgSO4溶液都发生聚沉
B.分散质的粒子都不能通过半透膜
C.都比较稳定,密封保存一段时间都不会产生沉淀
D.加入硫酸先产生沉淀,后沉淀溶解
2.从硫元素的化合价态上判断,下列物质中的硫元素不能表现氧化性的是 ( )
A.Na2S B. S C. SO2 D. H2SO4
1.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是 ( )
A.化学不再是纯实验科学 B.化学不再需要实验
C.化学不做实验,就什么都不知道 D.未来化学的方向还是经验化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com