
题目列表(包括答案和解析)
4、下列离子中,最易结合质子的是
A、Cl- B、CH3CH2O - C、OH - D、C6H5O –
3、我国纳米专家发明的“WXP复合纳米材料”的主要化学成分是氨基二氯代戊二醛的含硅衍生物,它能保持长期杀菌作用,“WXP复合纳米材料”有望用于制造纸币。试推断以直链戊二醛(OHCCH2CH2CH2CHO)为母体的氨基二氯代戊二醛的可能结构有
A、6种 B、7种 C、8种 D、10种
2、 由下列各组的三种元素构成的化合物中,既有离子晶体,又有分子晶体的是
A、H、O、C B、Na、S、O C、H、N、O D、H、S、O
1、下列有关共价化合物的说法中,一定正确的是
①具有较低的熔、沸点 ②不是电解质 ③固体时是分子晶体 ④都由分子构成 ⑤液态时不导电
A、①③④ B、②④⑤ C、①②③④⑤ D、只有⑤
21.答案:(10分,其中(1)(2)每空2分,(3)(4)每空3分)
(1)NaCl (2)A中必含有NaCl
(3)0.04+ (4)2.56 g
24.(10分)白色粉末A由Na2S、Na2SO3、Na2S2O3、Na2SO4、NaCl等物质中的三种混合而成,取一定量A样品投入100 mL、2.2 mol·L-1盐酸中,充分反应后过滤,最终得到100 mL pH为0的溶液。将此溶液蒸干,只得到8.19 g纯净B。
(1)B的化学式为_______________________________。
(2)请通过计算推断A中是否有NaCl?____________________________________。
(3)若反应中还生成V L(标准状况)气体,且气体不会使品红溶液褪色,则取出的A样品中含有Na2S___________________________mol(用含V的代数式表示)。
(4)A中组成的物质的量比不同时,所产生的沉淀的量也不同,上述A样品与盐酸反应可生成沉淀的质量最大值是_____________ g。
23.(8分)采矿工业废液中的氰化物(含CN-)具有很强的毒性,对环境的污染比较严重,工业上通常要进行处理,将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一)或无毒物质。
(1)工业上用过氧化氢处理含CN-的废水,其反应方程式为(已配平):KCN+H2O2+H2O=A+NH3↑。则生成物A的化学式为 ,反应中被氧化的元素为 (填写元素符号)。
(2)工业上用氯氧化法处理含CN-的废水,某厂废水中含KCN,其浓度为650mg •L-1。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2 → KOCN+2KCl+H2O。如果投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:
KOCN+ KOH+ Cl2 - CO2 + N2 + KCl + H2O
(3)若用液氯处理上述废水,使KCN完全转化为无毒物质,则理论上71克的液氯可处理上述废水 L。
答案:(10分,每空2分,配平2分)(1)KHCO3,C(2)2、4、3、2、1、6、2(3)40
22. (10分)如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH溶液后倒立于KOH溶液的水槽中。切断K1,闭合K2、K3通直流电,回答下列问题:
(10分)如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH溶液后倒立于KOH溶液的水槽中。切断K1,闭合K2、K3通直流电,回答下列问题:
(1)判断电源的正、负极:a为________极,b为________极。
(2)在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,可能出现的现象________。
(3)写出电极反应式:A极________,C极______________。
(4)若A极产生气体的体积在标准状况下为xL,则C极上产物的质量大约为______________g。
(5)若电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,合闭K1,则电流表的指针是否移动(填“是”或“否”) ________。若电流表指针不移动说明理由,若指针移动也说明理由。
答案:(1)负极:2H2+4OH--4e-=4H2O, 正极:O2+2H2O +4e-=4OH-
2H2+O2=2H2O (2)①负、正 ②紫色向D方向移动,两极有气体产生 ③4OH--4e-= O2↑+2H2O,4H++4e-=2H2↑ ④5x/28g ⑤是 组成氢氧燃料电池
23.(1)B2H6(g)+3O2(g)=B2O3(s)+3H2O(l);△H=-2165kJ/mol 1016.5kJ
(2)①b Fe2++(2a-b)Br-+aCl2 = b Fe3++(a-)Br2+2 aCl-
②2 Fe2++4Br-+3Cl2 = 2Fe3+ +2Br2+6Cl-
21.(8分)(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为
;又知H2O(l)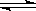 H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是 kJ。
H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是 kJ。
(2)将a mol Cl2通入含 b mol FeBr2的溶液中,若0< ≤时,反应的离子方程式为2Fe2+ +Cl2 = 2Fe3+ +2 Cl-,写出另外两个可能发生反应的离子方程式。
①当 < < 时 。
②当 ≥时 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com