
题目列表(包括答案和解析)
6.无色混合气体甲,可能含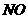 、
、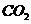 、
、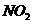 、
、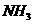 、
、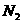 中的几种,将100mL甲气体依次经过下图实验的处理,结果得到酸性溶液且最终无剩余气体。则甲气体的组成为
中的几种,将100mL甲气体依次经过下图实验的处理,结果得到酸性溶液且最终无剩余气体。则甲气体的组成为
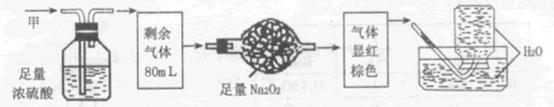
A.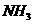 、
、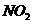 、
、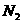 B.
B.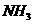 、
、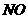 、
、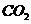
C.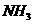 、
、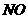 、
、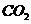 、
、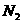 D.
D.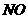 、
、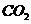 、
、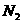
5.已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
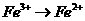 ;
;
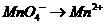 ;
;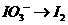 ;
;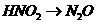 。
。
如果分别用这些物质氧化KI,得到等物质的量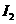 ,消耗最少的时
,消耗最少的时
A.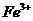 B.
B.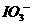 C.
C.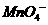 D.
D.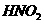
4.下列各组离子在酸性溶液中能大量共存的是
A.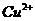
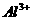
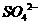
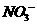 B.
B.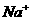
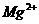
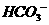

C.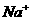
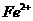

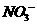 D.
D.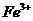
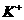


3.下列离子方程式正确的是
A.钠与水反应: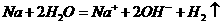
B.用醋酸中和 溶液:
溶液: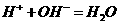
C.向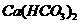 溶液中加澄清石灰水:
溶液中加澄清石灰水: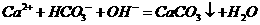
D.向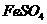 溶液中滴加
溶液中滴加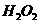 :
: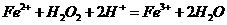
2.原计划实现全球卫星通讯需发射77颗卫星,这一数学与铱(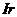 )元素的核电核数恰好相等,因此成为“铱星计划”。已知铱的一种核素的质量数为191,则其核内的种子数是
)元素的核电核数恰好相等,因此成为“铱星计划”。已知铱的一种核素的质量数为191,则其核内的种子数是
A.77 B.114 C.191 D.268
1.在盛放浓硫酸的试剂瓶标签上印有下列警示标记中的

27.(7分)取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸体积之间的关系如下图所示,试回答下列问题:

(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式)
,各种溶质的物质的量之比为 ;加盐酸后产生CO2体积的最大值为 mL。
(2)曲线B表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式)
;加盐酸后产生CO2体积最大值 mL。
(3)通过计算求出原NaOH溶液的物质的量浓度。
高三化学上学期期中考试评估卷
26.(6分)6.4 g Cu与过量硝酸(a mol / L,30mL)充分反应。硝酸的还原产物只有NO2、NO。反应后溶液中含H+为0.1mol。
(1)此时溶液中所含NO3-为 mol。
(2)求生成的气体中NO2和NO的物质的量各为多少(用含有a的式子表示)?
25.(8分)已知a、I、e为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
|
粒子代码 |
a |
I |
e |
|
原子核数 |
单核 |
四核 |
双核 |
|
粒子的电荷数 |
一个单位正电荷 |
0 |
一个单位负电荷 |
物质A由a、e构成,B、C、D、K都是单质,反应①-⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
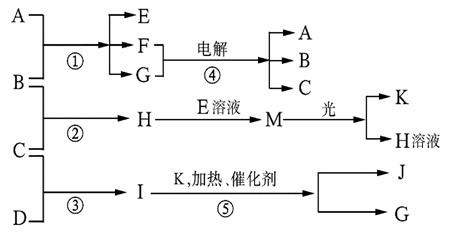
请填写下列空白:
(1)写出下列物质的化学式:B 、J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。
②反应① 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为:
24.(9分)已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Z二种元素的元素符号:X 、Z
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为:
(3)由X、Y、Z所形成的常见离子化合物是 .它与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是:
(4)在由X、Y、Z、W四种元素形成的常见单质或化合物中,不能形成的晶体类型是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com