
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
14. AЁЂMЮЊСНжждЊЫи,вбжЊAЮЛгкЖЬжмЦк,ЧвA2-гыM+ЕФЕчзгЪ§жЎВюЮЊ8,дђЯТСаЫЕЗЈжае§ШЗЕФЪЧЃК
A. A КЭ M ЕФдзгађЪ§жЎВюЮЊ 8
B. A КЭ M дзгЕФЕчзгзмЪ§жЎКЭПЩФмЪЧ 11
C. A КЭ M дзгЕФзюЭтВуЕчзгЪ§жЎКЭЮЊ 8
D. A КЭ M дзгЕФзюЭтВуЕчзгЪ§жЎВюЮЊ 5
13. ЯђНКЬхжаМгШыЕчНтжЪ,ФмЪЙНКЬхФ§ОлЁЃЪЙвЛЖЈСПЕФНКЬхдквЛЖЈЪБМфФкПЊЪМФ§ОлЫљашЕчНтжЪЕФХЈЖШ(mol/L)ГЦзї"ОлГСжЕ"ЁЃЕчНтжЪЕФОлГСжЕдНаЁ,дђБэЪОЦфФ§ОлФмСІдНДѓ , ЪЕбщжЄУї,Ф§ОлФмСІжївЊШЁОігкНКСЃДјЯрЗДЕчКЩЕФРызгЫљДјЕФЕчКЩЪ§,ЕчКЩЪ§дНДѓ, Ф§ОлФмСІдНДѓ,дђЯђFe(OH)3НКЬхжаМгШыЯТСаЕчНтжЪЪБ,Цф"ОлГСжЕ"зюаЁЕФЮЊЃК
A. NaClЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B. FeCl3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C. K2SO4ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D. Na3PO4
12ЃЎЯТСаИїзщЮяжЪМфЗДгІПЩФмАќРЈЖрВНЗДгІ , ЦфзмЕФРызгЗНГЬЪНе§ШЗЕФЪЧ
A. NaC1O (aq) жаЭЈШыЩйСП CO2ЃКЁЁ C1O- + CO2 + H20 = HClO +HC03-
ЁЁЁЁ B. FeCl2дкПеЦјжаБЛбѕЛЏ:ЁЁЁЁЁЁ ЁЁЁЁ4Fe2++O2+2H20=4Fe3++40H- ЁЁ
ЁЁЁЁ C. A1Cl3(aq)жаЭЖШыЙ§СПNa:ЁЁЁЁЁЁ A13++4Na+2H20 = A102- + 4Na++ 2H2 Ёќ
ЁЁЁЁ D. FeBr2(aq)жаЭЈШыЩйСПC12:ЁЁЁЁЁЁ 2Fe2++4Br-+3C12= 2Fe3++2Br2+6C1-
11ЃЎФГЮоЩЋШмвКгыNH4HC03зїгУФмВњЩњЦјЬх,ДЫШмвКжаПЩФмДѓСПЙВДцЕФРызгзщЪЧ
AЃЎC1-ЁЂ Mg2+ ЁЂH+ ЁЂ Zn2+ ЁЂS042-
BЃЎNa+ ЁЂ Ba2+ ЁЂ N03-ЁЂ OH- ЁЂ SO42-
CЃЎMnO4-ЁЂK+ ЁЂCl- ЁЁH+ ЁЁS042- ЁЁ
DЃЎK+ ЁЁN03-ЁЂS042- ЁЂOH- ЁЁNa+
10.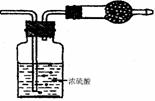 ФГЮоЩЋЦјЬхПЩФмгЩ O2
ЁЂ CO2 ЁЂ HClЁЂNH3
ЁЂNO ЁЂ Br2 ЁЁжаЕФвЛжжЛђМИжжзщГЩ , ЭЈЙ§ЭМжаЯДЦјЦПКѓЦјЬхЬхЛ§МѕЩй , ЭЈЙ§ИЩдяЙмКѓЦјЬхГЪКьзиЩЋ , дђЯТСаЭЦЖЯе§ШЗЕФЪЧ:
ФГЮоЩЋЦјЬхПЩФмгЩ O2
ЁЂ CO2 ЁЂ HClЁЂNH3
ЁЂNO ЁЂ Br2 ЁЁжаЕФвЛжжЛђМИжжзщГЩ , ЭЈЙ§ЭМжаЯДЦјЦПКѓЦјЬхЬхЛ§МѕЩй , ЭЈЙ§ИЩдяЙмКѓЦјЬхГЪКьзиЩЋ , дђЯТСаЭЦЖЯе§ШЗЕФЪЧ:
AЃЎИЩдяЙмФкЙЬЬхЮЊМюЪЏЛв
BЃЎдЦјЬхжавЛЖЈга NO КЭ O2
CЃЎдЦјЬхжавЛЖЈгаNH3 ЁЂNO ЁЂCO2
DЃЎдЦјЬхжавЛЖЈУЛга HC1ЁЂ Br2
9ЃЎ ЩшNAДњБэАЂЗ№МгЕТТоГЃЪ§ЕФЪ§жЕ , ЯТСаЫЕЗЈжае§ШЗЕФЪЧ:
ЂйГЃЮТГЃбЙЯТ, 17g МзЛљ (Ѓ14CH3) ЫљКЌЕФжазгЪ§11NA
ЂкГЃЮТГЃбЙЯТЃЌ22.4L NOЦјЬхЕФЗжзгЪ§аЁгкNA
Ђл 64gЕФЭЗЂЩњбѕЛЏЛЙдЗДгІ , вЛЖЈЪЇШЅ2NAИіЕчзг
ЂмГЃЮТГЃбЙЯТ , 100mL 0.5mol/L ЕФввЫсШмвКжа , ввЫсЕФЗжзгЪ§ФПаЁгк0.05NA
ЂнБъПіЪБ , 22.4L ЖўТШМзЭщЫљКЌгаЕФдзгЪ§ЮЊ5NA
ЂоГЃЮТГЃбЙЯТ, 1mol ТШЦјКЌгаЕФЕчзгЖдЪ§ЮЊNA
ЁЁЁЁ A. ЂйЂк ЁЁЁЁЁЁЁЁЁЁЁЁ B. ЂлЂм ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.ЂкЂмЁЁЁЁЁЁЁЁЁЁЁЁ D.ЂнЂо
8ЃЎ 100ЁцЪБЃЌНЋ0.1molN2O4жУгк1LУмБеЕФЩеЦПжаЃЌШЛКѓНЋЩеЦПЗХШы100ЁцЕФКуЮТВлжаЃЌЩеЦПФкЕФЦјЬхж№НЅБфЮЊКьзиЩЋЃКN2O4(g)
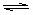 2NO2 (g)ЁЃЯТСаНсТлВЛФмЫЕУїЩЯЪіЗДгІдкИУЬѕМўЯТвбОДяЕНЦНКтзДЬЌЕФЪЧЁЁ
2NO2 (g)ЁЃЯТСаНсТлВЛФмЫЕУїЩЯЪіЗДгІдкИУЬѕМўЯТвбОДяЕНЦНКтзДЬЌЕФЪЧЁЁ
ЂйЩеЦПФкЦјЬхЕФбеЩЋВЛдйМгЩюЃЛЁЁЁЁЁЁ ЂкN2O4 ЕФЯћКФЫйТЪгыNO2ЕФЩњГЩЫйТЪжЎБШЮЊ1ЁУ2ЃЛЁЁЁЁ ЂлNO2ЕФЩњГЩЫйТЪгыNO2ЯћКФЫйТЪЯрЕШЃЛЁЁЁЁ ЂмNO2ЕФЮяжЪЕФСПХЈЖШВЛБфЃЛЁЁ ЂнЩеЦПФкЦјЬхЕФжЪСПВЛдйБфЛЏЃЛЁЁ ЂоЩеЦПФкЦјЬхЕФбЙЧПВЛдйБфЛЏЃЛЁЁ ЂпЩеЦПФкЦјЬхЕФУмЖШВЛдйБфЛЏЃЛЁЁ ЂрЩеЦПФкЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПВЛдйБфЛЏ
ЁЁ AЃЎЂкЂнЂпЁЁЁЁЁЁЁЁЁЁ BЃЎЂйЂлЂмЂоЂрЁЁЁЁЁЁЁЁЁЁ CЃЎжЛгаЂлЁЁЁЁЁЁЁЁЁЁ DЃЎжЛгаЂн
7. ЁЁЯТСаИїбЁЯюЫљЪіЕФСНИіСП , ЧАепвЛЖЈДѓгкКѓепЕФЪЧ:
Ђй F2 КЭ Br2 ЕФЗаЕу
ЂкДПЫЎдк 25 Ёц КЭ 80 Ёц ЪБЕФ pH жЕ
ЂлЭЌЮТЯТЗжБ№дк1OOgЫЎжазюЖрФмШмНтЕФЮоЫЎ CuSO5КЭ CuSO5ЁЄ 5H2OЕФжЪСП
Ђм 25 Ёц ЪБ ,ЕШЬхЛ§ЕФ pH жЕЖМЕШгк3ЕФбЮЫсКЭAlCl3ШмвКжа ,вбЕчРыЕФЫЎЗжзгЪ§
ЂндкNH3+NOЁњ N2ЪЎH20 ЗДгІжа , БЛбѕЛЏКЭБЛЛЙдЕФN дзгЪ§
ЂоФЭЛ№ВФСЯ MgO КЭ CaO ЕФШлЕу
Ђп H-КЭH+РызгАыОЖ
ЂрН№ИеЪЏОЇЬхКЭЪЏФЋОЇЬхжа , УПИізюаЁЬМЛЗРяЫљКЌЕФЪЕМЪЬМдзгЪ§
ЁЁЁЁ AЃЎЂйЂкЂоЁЁЁЁЁЁЁЁ BЃЎЂйЂкЂлЂнЁЁЁЁЁЁЁЁ CЃЎЂнЂоЂп ЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂкЂоЂп
6ЃЎ ЙигкЙЄвЕЩњВњЕФЯТСаа№ЪіжаЃЌВЛе§ШЗЕФЪЧ
ЁЁ ЁЁ AЃЎЙЄвЕЩњВњСђЫсЪБЃЌЪЙгУШШНЛЛЛЦїПЩвдГфЗжРћгУЗДгІжаЫљЗХГіЕФШШСП
ЁЁ BЃЎЙЄвЕЩЯКЯГЩАБУЛгаВЩгУИќДѓЕФбЙЧПЪЧДгЩшБИКЭЖЏСІвЊЧѓЗНУцПМТЧЕФ
ЁЁ CЃЎЙЄвЕЩЯгУРызгНЛЛЛФЄЗЈЕчНтБЅКЭЪГбЮЫЎжЦЩеМю
ЁЁ DЃЎЙЄвЕЩЯВЩгУЕчНтШлШкТШЛЏТСЕФЗНЗЈжЦШЁН№ЪєТС
5. ЁЁ(NH4) 2PtCl6 ОЇЬхЪмШШЗжНт , ЩњГЩЕЊЦјЁЂТШЛЏЧтЁЂТШЛЏяЇКЭН№ЪєВЌЁЃдкДЫЗжНтЗДгІжа , бѕЛЏВњЮягыЛЙдВњЮяЕФЮяжЪЕФСПжЎБШЪЧ:
ЁЁЁЁ A.1: 2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.1: 3 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.2: 3 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.3: 2
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com