
题目列表(包括答案和解析)
7.K35ClO3晶体与H37Cl溶液反应生成氯气、氯化钾和水,此反应生成的氯气的相对分子质量为
A.73.3 B.73 C.74 D.70.6
6.实验室用白磷(P4)和四碘化二磷(P2I4)与水共同反应来制备碘化鏻(PH4I)。同时还生成磷酸,下面叙述正确的是
A.方程式中P2I4和PH4I的系数比为1:4 B.水在反应中为氧化剂
C.生成的磷酸是还原产物 D.反应过程中无电子得失和偏移
5.已知H2O(g)=H2O(l);△H1=-Q1 kJ/mol C2H5OH(g)=C2H5OH(l);△H2=-Q2 kJ/mol C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H3=-Q3 kJ/mol
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为
A.Q1+Q2+Q3 B.0.5(Q1+Q2+Q3) C.1.5Q1+0.5Q2+0.5Q3
D.1.5Q1-0.5Q2+0.5Q3
4.化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol
 化学键时释放(或吸收)出的能量。已知白磷和P4O6的
化学键时释放(或吸收)出的能量。已知白磷和P4O6的
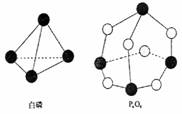
分子结构如右图所示,现提供以下化学键的键能(kJ·mol-1)
P-P:198 , P-O:360 , O2分子:498 。则反应
P4(白磷)+3O2→P4O6的反应热△H为
A.-1638kJ/mol B.+1638kJ/mol
C.-126kJ/mol D.+126kJ/mol
3.下列反应中,Na2O2既不是氧化剂又不是还原剂的是
A.2Na2O2+2H2O=4NaOH+O2↑ B.2Na2O2+2CO2=2Na2CO3+O2↑
C.Na2O2+H2SO4=Na2SO4+H2O2 D.3Na2O2(熔融)+Fe2O3=2Na2FeO4+Na2O
2.要配制下列含有较多量不同阴、阳离子的四种溶液,其中能配制成功的是
A.K+、Al3+、Cl-、CO32- B.H +、Zn2+、S2O32-、Cl-
C.H +、SO32-、S2-、Cl- D.Mg2+、SO42-、NH4+、Cl-
1.从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是
A.2NaBr+Cl2=2NaCl+Br2 B.AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl
C.3S+6KOH=2K2S+K2SO3+3H2O D.NH4Cl+NaNO2=NaCl+N2↑+2H2O
0.2505g样品扩大一倍来算(即用0.5010g)推算出:
反应消耗AgNO3:n(AgNO3)=0.1000mol·L-1x40.00mL=0.004000mol
即发生上述反应的Cl-为:n(Cl-) =0.004000mol
则有 y:z=(0.006000mol-0.004000 mol): 0.004000mol=1:2
同时还有:1:x:(y+z)= 0.002000: 0.01000: 0.006000=1:5:3
解得:x=5 y=1 z=2
带入[Co(NH3)xCly]Clz中,求得Co化合价为:+3 假设成立
该钴化合物的化学式为:[Co(NH3)5Cl]Cl2
答:⑴[Co(NH3)xCly]Clz中氮元素的质量分数为27.94%
⑵该钴化合物的化学式为:[Co(NH3)5Cl]Cl2
0.5010g样品中Cl的总质量为:
m(Cl)=0.5010g-0.002000molx59g·mol -1-0.01000molx17g ·mol -1=0.2130g
n(Cl)=0.006000mol
又有:[Co(NH3)xCly]Clz+zAgNO3==[Co(NH3)xCly](NO3)z+zAgCl↓
20.00mLB溶液中过量的HCl:n(HCl)=0.003000mol ,
100mLB溶液中过量的HCl:n(HCl)=0.01500mol那么与NH3反应的n(HCl)=0.01000mol
故0.5010g样品中 n(NH3)=0.01000mol n(N)=0.01000mol
[Co(NH3)xCly]Clz中氮元素的质量分数
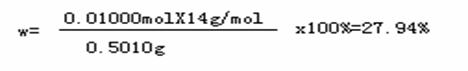
⑵ I2+2Na2S2O3==2NaI+Na2S4O6
因反应用去0.1000mol·L-1Na2S2O3溶液20.00mL,推算出:n(I2)=0.001000mol
Co与Fe同一族,Com+具有强氧化性,故设m=3
则有:2Co3++2I-==2Co2++I2 n(Co3+)=0.002000mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com