
题目列表(包括答案和解析)
22.(16分)某无色溶液中可能存在的离子如下: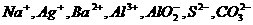
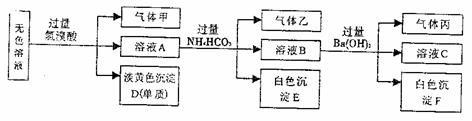
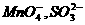 。取10mL该溶液进行实验,有关实验过程、现象及产物如下图所示:
。取10mL该溶液进行实验,有关实验过程、现象及产物如下图所示:
回答下列问题:
(1)沉淀D是(填名称) ,生成该沉淀的离子方程式为:
;
生成气体乙的离子方程式为: ;
生成沉淀F的离子方程式为: ;
(2)若测知气体甲为两种成分,则气体和原溶液中溶质的可能组成为(将结果填入下表中。)
|
可能情况 |
(1) |
(2) |
|
气体可能 组成 |
|
|
|
溶质可能组成 (填化学式) |
|
|
(3)若测知气体甲的成分只有一种时,则原溶液中一定存在的离子有 ,可能存在的离子有 。
|
21.(12分)某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了下图所示装置。打开分液漏斗D中活塞,缓慢加入稀盐酸至过量,与固体M充分反应。待反应停止后,B中有黑色沉淀析出,C中量气装置右边液面上升,调节量气装置使左右液面相平后,测得进入C中的气体为V mL(已换算成标准状况)。
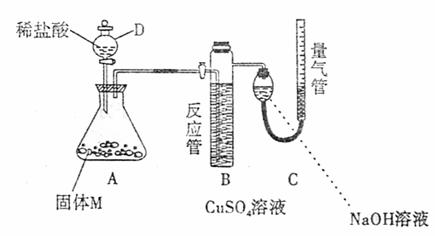
根据上述实验事实,回答下列问题:
(1)加入药品和实验开始前必须进行的操作是 。
(2)固体M中一定有的物质是 (写化学式)。
(3)写出A中发生反应的化学方程式(只写一个):
。
(4)写出B中析出黑色沉淀时发生反应的离子方程式 。
(5)根据题给条件,固体M中一种物质的质量可以确定,应为 g(用代数式表示)。
(6)稀盐酸与固体M反应后还残留淡黄色固体,该固体可能是 (写化学式),要分离该固体,在实验操作中,除烧杯、玻璃棒外,还需要的玻璃仪器是 。
(7)反应完成后,取A中溶液少许加入试管中,要确定固体M中是否含有Fe3+,需加入的试剂为: 。
A.KSCN溶液 B.NaOH溶液 C.氨水
20.(14分)简要回答下列问题:
(1)春夏季下雨时常伴有“电闪雷鸣”现象,因“闪电”而发生的化学反应有(举两例,用化学方程式表示):
①
②
(2)酸雨的pH小于5.6,放置一段时间后pH还会减少。其原因是(用化学方程式表示):
(3)铁的纯度越高越不易生锈;钢铁表面上若附着有电解质更易生锈。铁锈的化学成分是:Fe2O3·nH2O。请写出钢铁生锈时有关反应的化学方程式(包括电极反应及其总反应):
电极反应式:
总反应式:
其它反应:
19.下列各组有机物,不论以何种比例混合,只要二者物质的量之和不变,那么,完全燃烧时所消耗氧气的物质的量相等,且所生成的物质的量也相等的是 ( )
A.甲烷和甲酸甲酯 B.乙烷和乙醇
C.苯和苯酚 D.乙炔和苯
第Ⅱ卷(非选择题,共62分)
18.下列热化学式中△H的绝对值能表示可燃物燃烧热的是 ( )
A.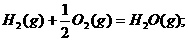 △H=-241.8KJ·mol-1
△H=-241.8KJ·mol-1
B.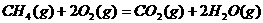 ;△H=-802.3KJ·mol-1
;△H=-802.3KJ·mol-1
C.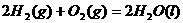 ;
△H=-571.6KJ·mol-1
;
△H=-571.6KJ·mol-1
D.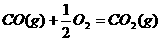 ;
△H=-283KJ·mol-1
;
△H=-283KJ·mol-1
17.过氧化氢俗称双氧水,它是一种液体,易分解,常作氧化剂、漂白剂,为贮存、运输、使用的方便,YC工业上常将H2O2转化为固体的过碳酸钠(化学式为:2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是( )
A.MnO2 B.H2S C.NaHCO3 D.稀HCl
16.下列离子方程式中正确的是 ( )
A.向NaHCO3溶液中滴加少量澄清的石灰水:
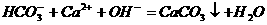
|
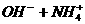 ======
======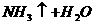
 C.NaHS溶液呈碱性:
C.NaHS溶液呈碱性: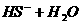
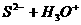
D.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性
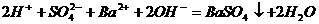
14.将等物质的量的Mg和Al的粉末混合均匀,分成四等份,分别加入到下列四种过量的溶液中,充分反应后,放出氢气量最多的是 ( )
A.3mol/LHCl溶液 B.4mol/L HNO3溶液
C.8mol/LNaOH溶液 D.18mol/L H2SO4溶液
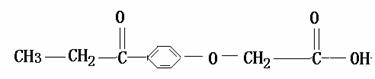 15.利尿酸在奥运会上被禁用,其结构简式为:
15.利尿酸在奥运会上被禁用,其结构简式为:
下列叙述正确的是 ( )
A.利尿酸分子内处于同一平面的原子数不超过10个
B.利尿酸能使溴水褪色
C.1mol利尿酸最多可与6mol H2发生加成反应
D.利尿酸与新制Cu(OH)2悬浊液反应有红色沉淀生成
13.下列叙述中正确的是 ( )
A.离子化合物中可能含有非极性共价键
B.共价化合物中可能含有离子键
C.晶体中不一定都存在化学键
D.结构类似的共价化合物,相对分子质量越大,其熔沸点一定越高
12.某有机物在酸性条件下发生水解反应时,生成两种不同有机物,且这两种有机物的相对分子质量相等。则水解前的这种有机物是 ( )
A.甲酸甲酯 B.乙酸异丙酯 C.麦芽糖 D.葡萄糖
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com