
题目列表(包括答案和解析)
2. 下列各组中的物质,互为同位素的是 ( )A.白磷与红磷 B.苯与甲苯 C.重氢与超重氢 D.2-甲基丙烷与丁烷
1. 科学家发现宇宙中有一种新型的氢粒子,它由3个氢原子核(只含质子)和2个电子构成,这对解释宇宙的演化提供了新的参考依据。下列符号能正确表示该新型粒子的是 ( )A.H3 B.3H+ C.H3+ D.H3+
24.(本题10分) 在t℃时,向盛有500 g水的烧杯中加入3.7 g Ca(OH)2粉末,充分搅拌。已知t℃时,Ca(OH)2的溶解度是0.185 g。并假设在溶解和反应过程中溶液的体积温度基本保持不变,所得溶液的密度约为1.00g/cm3。试计算下列问题(计算结果保留2位小数)。
(1)求烧杯中所得的石灰水中OH-离子的物质的量浓度。
(2)若采用向上述烧杯中通入CO2气体的方法,使溶液中的Ca2+离子浓度等于0.01 mol·L-1,则需要向烧杯中通入标准状况下CO2 的体积是多少?
23.(本题10分)在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量/mg |
255 |
385 |
459 |
|
气体体积/mL |
280 |
336 |
336 |
(1)乙组实验中,盐酸 (填“过量”、“适量”或“不足量”),
理由是 。
(2)要计算盐酸的物质的量浓度,题中可做计算依据的数据是 。
(3)合金中Mg、Al的物质的量之比为 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,则所加NaOH溶液的体积是 。
22.(本题9分) A、B、C、D四种元素都是短周期元素。A元素的离子焰色反应时火焰呈黄色。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL 2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构最外层电子数是次外层电子数的三倍。根据上述条件,回答:
(1)C元素在元素周期表中的位置是 ,它的最高价氧化物的化学式为 。
(2)C与B元素形成化合物的晶体类型是______________。
(3)A与D形成稳定化合物的电子式为______________,判断该化合物在空气是否变质的简易方法是 。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为 。
21.(本题7分)A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3和AgNO3中的一种。已知:
①A与B反应有气体生成 ②B与C反应有沉淀生成
③C与D反应有沉淀生成 ④D与E反应有沉淀生成
⑤A与E反应有气体生成 ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是 。
(2)A是 ,B是 ,C是 ,D是 ,E是 。
(3)A与E反应的离子方程式是 。
20.(本题9分)已知:2Fe + 3Br2 = 2FeBr3,Fe2+的还原性大于Br-现有16.8g铁和0.3molBr2反应后加入适量水后,通入amolCl2。
(1).当a≤0.15时,反应离子方程式为
(2).当Fe2+与Br-同时被氧化时,a的取值范围为
(3).当a=0.3时,反应后氧化产物与还原产物的物质的量之比为
19.(本题9分)
⑴下列仪器中,根据物质的沸点不同分离物质时需要的是 (填编号)。
 ①容量瓶 ②普通漏斗 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥滴定管 ⑦燃烧匙 ⑧温度计 ⑨干燥管
①容量瓶 ②普通漏斗 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥滴定管 ⑦燃烧匙 ⑧温度计 ⑨干燥管
⑵右图分别是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是 。
A.①是量筒,读数为2.5mL
B.②是量筒,读数为2.5mL




 C.③是滴定管,读数为3.5mL
C.③是滴定管,读数为3.5mL
D.①是温度计,读数为2.5℃
⑶ 实验室里不同化学试剂的保存方法不尽相同。下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内(多选倒扣分):
① NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦氯水 ⑧浓硝酸
|
A |
B |
C |
D |
E |
 |
 水 水 |
 |
 |
 |
|
( ) |
( ) |
( ) |
( ) |
( ) |
18.某结晶水合物化学式为R·nH2O,其式量为M。25℃时,将ag该晶体溶于bgH2O中恰好形成Vml饱和溶液。下列表示式正确的是 ( )
A.25℃时R的溶解度为: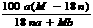 g
g
B.饱和溶液溶质的质量分数为: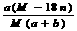 %
%
C.饱和溶液物质的量浓度为: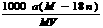 mol·L-1
mol·L-1
D.饱和溶液的密度为: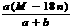 g·mL-1
g·mL-1
第二卷 (非选择题 共54分)
17.若某氖原子质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是 ( )
A.氖元素的相对原子质量一定是12a/b B.该氖原子的摩尔质量是aNAg/mol
C.Wg该氖原子的物质的量一定是 mol D.Wg该氖原子所含质子数是10W/a
mol D.Wg该氖原子所含质子数是10W/a
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com