
题目列表(包括答案和解析)
28.(14分)环保检测部门测定某气体样品中含一氧化碳的含量,其方法和实验步骤如下:
① 将2.000L的气体样品通过盛有I2O5固体的加热管,发生的反应为:
5CO + I2O5
 5CO2
+ I2。
5CO2
+ I2。
② 将所产生的碘升华,并加入30.00mL 0.0050 mol·L-1的硫代硫酸钠溶液,发生的反应为:I2 + 2S2O32- = 2I-+ S4O62-
③ 将②中溶液取出 ,加入1.000mL 0.0100 mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化。
,加入1.000mL 0.0100 mol·L-1的碘水,正好将所取溶液中过量的Na2S2O3全部氧化。
试计算1L该气体样品中有多少毫克(mg)的CO?
27. (12分) 莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
(1)A的分子式是 。
(2)A与溴的四氯化碳溶液反应的化学方程式是
(有机物用结构简式表示)
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是
(4)A在浓硫酸作用下加热可得到B(B的结构简式为HO- -COOH),其反应类型是
。
-COOH),其反应类型是
。
(5)B的同分异构体中既含有酚羟基又含有酯基的共有 种,写出其中一种同分异构体的结构简式 。
26.(8分)在化学上常用两种模型来表示分子结构,一种是球棍模型,另一种是比例模型。比例模型是用不同颜色球的体积比来表示分子中各种原子的体积。
(1)右图是一种常见有机物的比例模型,该模型图可代表一种( )
 A.饱和一元醇 B.饱和一元醛
A.饱和一元醇 B.饱和一元醛
C.二元酸 D.羟基酸
(2)该物质可发生的反应有( )
A.与H2加成 B.银镜反应
C.消去反应 D.与乙醇酯化
(3)根据(2)中选择,写出该物质发生反应的化学方程式
25.(11分)写出下列反应的离子方程式。
(1)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程都可用“Ba2++SO42-==BaSO4↓”来表示,请写出有关反应的化学方程式(3个)_________________。
(2)溴化碘的分子式为IBr,它跟水反应的化学方程式为H2O+IBr==HBr+HIO,若将其改写成离子方程式应为_________________。
(3)在淀粉KI溶液中加入适量稀硫酸,再滴加少量NaClO溶液,溶液即变蓝色,写出该反应的离子方程式__________________。在上述蓝色溶液中滴加足量的Na2SO3溶液,蓝色逐渐消失,写出该反应的离子方程式__________________。从以上实验可知ClO-,I2,SO32-的氧化性由强到弱的顺序是_________________________。
24. (10分)下图是部分元素的单质及其化合物的转化关系图(有关反应的条件及部分反应物或生成物已略去);
已知:C、D、F均为单质,其中C、D在常温、常压下是气体;反应②是化工生产中的重要反应,生成物E具有漂白性;J、K均为不溶于水的沉淀,其中J为红褐色。

请回答下列问题:
(1)A的电子式:_______________;
(2)反应②的离子方程式是___________________________________;
(3)反应③的化学方程式是____________________________________;
(4)实验室由H制备少量K的方法:是用胶头滴管吸取B溶液,将滴管尖端插入盛有新制H溶液试管底部,慢慢挤出B溶液即可,观察到的现象为:
________________________________________________________;
(5)当有1.12L(标准状况)D生成时,反应①中转移的电子数为___________;
23.(8分)卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX’型卤素互化物与卤素单质结构相似、性质相近。试回答下列问题:
 ⑴卤素互化物BrCl能发生下列反应
⑴卤素互化物BrCl能发生下列反应
H2O+BrCl===HBrO+HCl
KBr+BrCl===KCl+Br2
①写出KI与IBr反应的化学方程式______________。
②写出苯与(C6H6)与ICl发生取代反应生成一卤代物的化学方程式____________________________。
⑵右图是部分卤素单质和XX’型卤素互化物的沸点与其相对分子质量的关系图。它们的沸点随着相对分子质量的增大而升高,其原因是______________。
⑶试推测ICl的沸点所处的最小范围是介于 的沸点和 的沸点之间。
21. (8分)某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如右图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为完全正确(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项
(8分)某研究性学习小组在整理实验室化学试剂时,发现一盛有无色溶液的试剂瓶,标签破损,如右图。某同学根据中学化学知识,对该试剂可能是什么物质的溶液进行了如下猜想和验证,选择你认为完全正确(包括猜想物质的化学式、检验需要的试剂、操作、现象及结论)的选项
(多选倒扣分)。
|
序号 |
猜想物质的化学式 |
检验需要的试剂 |
操作、现象及结论 |
|
A |
Na2SO4 |
稀盐酸、氯化钡溶液 |
取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4。 |
|
B |
Na2CO3 |
稀盐酸、澄清的石灰水、品红溶液 |
取少量该溶液于试管中,滴入稀盐酸,如果产生的气体不能使品红溶液褪色而能使澄清的石灰水变浑浊,则原溶液是 Na2CO3。 |
|
C |
Na2SO3 |
稀盐酸、澄清的石灰水 |
取少量该溶液于试管中,滴入稀盐酸,如果产生无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2SO3。 |
|
D |
Na2SiO3 |
过量稀盐酸 |
取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀溶解,则原溶液是Na2SiO3溶液。 |
|
E |
Na2S2O3 |
稀盐酸 |
取少量该溶液于试管中,滴入稀盐酸,如果溶液变浑浊(或产生淡黄色沉淀),并产生无色有剌激性气味的气体,则原溶液是Na2S2O3溶液。 |
除上述五种可能之外,写出你认为还有可能物质的化学式(1种): 。22. (4分)下面是某研究性学习小组对蜡烛及其燃烧的研究报告,请你完成该实验报告:
|
探究步骤 |
实验现象 |
结论或产生这一现象的原因 |
|
①将一小块蜡烛放入水中 |
|
结论:
|
|
②燃着时 |
有明亮火焰 |
|
|
③刚吹灭时 |
|
原因: |
20.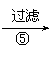

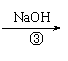

 (8分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(8分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐 滤液


精盐
 (1)判断BaCl2已过量的方法是____________________________。
(1)判断BaCl2已过量的方法是____________________________。
(2)第④步中,相关的离子方程式是_______________________。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,
其原因是_______________ ______________。
(4)为检验精盐纯度,需配制150 mL.0.2 mol/L NaCl(精盐)溶液,
右图是该同学转移溶液的示意图,图中的错误是_____________________________________________________。 100 mL容量瓶
19.NO和CO都是汽车尾气里有害物质,它们缓慢的起反应生成N2和CO2,对此反应,下列叙述正确的是
A.使用催化剂增大CO转化率 B.改变压强对反应速率无影响
C.降低压强能增大NO转化率 D.升高温度能加大反应速率
第Ⅱ卷(非选择题,共83分)
18.据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体
C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+
D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com