
题目列表(包括答案和解析)
9.将溶质质量分数为3p%的X溶液与p%的X溶液等体积混合,其混合溶液中溶质质量分数小于2p%,则X可能是下列物质的
A.H2SO4 B.NaCl C.C2H5OH D.NaOH
8.下列条件下,两瓶气体所含原子数一定相等的是
A.同质量、不同密度的N2和CO B.同温度、同体积的H2和N2
C.同体积、同密度的C2H4和C2H6 D.同压强、同体积的N2O和CO2
7.设NA代表阿伏加德罗常数,下列说法正确的是
A.5.6 g铁与足量盐酸反应转移的电子数为0.3NA
B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA
C.标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2NA
D.20 g重水(D2O)中含有的电子数为10NA
6.下列离子方程式中正确的是
A.CH3COOH溶液与NaOH溶液反应:H++OH-=H2O
B.Na2CO3溶液中通入少量CO2:CO32-+CO2+H2O=2HCO3-
C.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H+十SO42-=BaSO4↓+H2O
D.Ca(HCO3)2与过量Ca(OH)2溶液反应:
Ca2++HCO3-+2OH-=CaCO3↓+CO32-+2H2O
5.一定能在下列溶液中大量共存的离子组是
A.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl-
B.c(H+)=1×10-13mol·L-1的溶液:Na+、Ca2+、SO42-、CO32-
C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
D.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-
4.钛(Ti)被称为继铁、铝之后的第三金属,以TiO2制取Ti的主要反应有:
①TiO2+2C+2Cl2 TiCl4+2CO ②TiCl4+2Mg
TiCl4+2CO ②TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
下列叙述正确的是
A.反应①是置换反应 B.反应②是复分解反应
C.反应①中TiO2是氧化剂 D.反应②中金属镁是还原剂
3.下列说法正确的是
A.在101 kPa时,1 mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热
B.酸和碱发生中和反应生成1 mol水,这时的反应热叫中和热
C.燃烧热和中和热都属于反应热
D.在稀溶液中,1 mol CH3COOH和1 mol NaOH完全中和时放出的热量为57.3 kJ
2.下列叙述正确的是
A.直径介于1 nm-100 nm之间的微粒称为胶体
B.电泳现象可证明胶体属电解质溶液
C.利用丁达尔效应可以区别溶液与胶体
D.胶体粒子很小,可以透过半透膜
1.下列变化,一定都有新物质生成的是
A.炭化、风化、硝化、老化、钝化、油脂硬化
B.蒸馏、分馏、电解、电镀、电化学腐蚀、水解、分解
C.化合、混合、水合、氧化、酯化、皂化
D.空气液化制O2、脱水、渗析、盐析、凝聚
20、(13分)取0.04molKMnO4固体加热一段时间后,收集到a mol单质气体,此时KMnO4的分解率为x,在反应后的残留固体中加入100mL36.5%、1.18g/cm3的浓盐酸地(过量)并加热,充分反应后又收集到bmol单质气体(假定气体全部逸出),锰元素(Mn)全部以Mn2+存在于反应后的溶液中。
分解产物与浓盐酸在加热时涉及下列反应:
①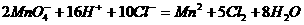
②□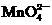 +□Cl-+□H+=□Mn2++□Cl2+□H2O
+□Cl-+□H+=□Mn2++□Cl2+□H2O
③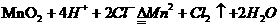
(1)试配平反应②的离子方程式,将化学计量数填入上述对应的方框内(如果是1,也必须填写)。
(2)a+b=_______(用含x的代数式表示)
(3)当x=_______时(a+b)取最小值,且最小值为___________。
(4)当a+b=0.09mol时,0.04molKMnO4按上述操作反应后,将所得溶液稀释至1L。该稀释后的溶液中c(H+)=________mol·L-1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com