
题目列表(包括答案和解析)
8.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.6.2克白磷分子中含P-P键为0.05NA
B.1 L pH = 1的水溶液中水合氢离子数为0.1 NA
C.6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA
D.标准状况下,2.24 L氧单质所含原子数一定为0.2 NA
7.下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是( )
|
|
(I) |
(II) |
|
A |
少量SO2通入Ba(OH)2溶液 |
过量SO2通入少量Ba(OH)2溶液 |
|
B |
少量浓氨水滴入Al2(SO4)3溶液 |
少量Al2(SO4)3溶液滴入浓氨水 |
|
C |
0.1mol Cl2通入含0.2mol FeBr2的溶液 |
0.3 molCl2通入0.2molFeBr2溶液中 |
|
D |
过量BaCl2溶液与少量Na2SO4溶液相混合 |
少量Ba(NO3)2溶液与过量MgSO4溶液相混合 |
6.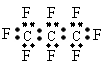 最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”-全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是( )
最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”-全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是( )
A、分子中三个碳原子可能处于同一直线上 B、全氟冰烷的电子式为:
C、相同压强下,沸点:C3F8<C3H8
D、全氟冰烷分子中既有极性键又有非极性键
5.
2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的
 烯烃复分解催化剂。工业上冶炼钼的化学原理为①2MoS2 + 7O2 2MoO3 + 4SO2;
烯烃复分解催化剂。工业上冶炼钼的化学原理为①2MoS2 + 7O2 2MoO3 + 4SO2;
②MoO3 + 2NH3·H2O = (NH4)2MoO4 + H2O; ③(NH4)2MoO4 + 2HCl = H2MoO4↓+ 2NH4Cl;
 ④H2MoO4 MoO3
+ H2O;⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是( )
④H2MoO4 MoO3
+ H2O;⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是( )
A、MoS2煅烧产生的尾气可直接排空
B、MoO3是金属氧化物,也是碱性氧化物
C、H2MoO4是一种强酸
D、利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
3.下列有关叙述正确的是( )
A.“神舟六号”飞船返回舱的表层采用高温时自动烧蚀的耐高温、抗氧化的新型无机非金属材料带走热量从而保证内部温度不致过高。
 B.“加碘食盐” “含氟牙膏”“富硒营养品” “高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子。
B.“加碘食盐” “含氟牙膏”“富硒营养品” “高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子。
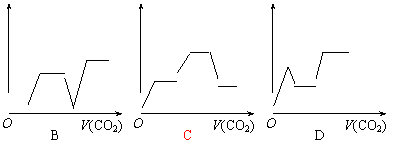
C.右图是反应物和生成物的能量变化示意图,则其可能发生的反应的热化学方程式可表示为:
2 A(g)+ B(g) = 2 C(g);△H= - Q kJ/mol(Q>0)
D.化工厂爆炸时可用湿布捂住鼻孔、眼睛等并躲在下风的低洼处
|
|
|
|
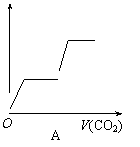
2.奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维
下列说法正确的是( )
A、羊毛与聚酯纤维的化学成分相同 B、聚酯纤维和羊毛一定条件下均能水解
C、该聚酯纤维单体为对苯二甲酸和乙醇 D、由单体合成聚酯纤维的反应属加聚反应
1.俄罗斯杜布纳核研究所和美国劳伦斯利弗莫尔实验室的科学家在2004年2月的美国《物理评论C》杂志上发表文章宣布, 他们新合成了元素周期表上的第115号和第113号元素。科学家在利用回旋加速器进行的实验中,用具有20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为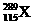 。下列有关叙述正确的是( )
。下列有关叙述正确的是( )
A.115号元素衰变成113号元素是化学变化 B.核素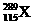 中中子数与质子数之差为174
中中子数与质子数之差为174
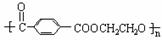 C.113号元素最高正价应为+3 D.115号与113号元素的原子质量比为115:113
C.113号元素最高正价应为+3 D.115号与113号元素的原子质量比为115:113
22.(10分)
2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1mol/L (NH4)2Fe(SO4)2溶液完全反应。
 (1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
MnO4-+ Fe2++ H+= Mn2++ Fe3++ H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为 mol。
(3)欲配制500mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为 g。
(4)混合物中Cu2S的质量分数为 。
21. (4分)
(4分)
(1)右图为某市售盐酸试剂瓶标签上的部分数据。该盐酸的物质的量浓度为 mol·L-1。
(2)将标准状况下的NH3(g)溶于水中,得到密度为ρ g·cm-3的氨水a g,物质的量浓度为c mol·L-1,则
溶于水中NH3(g)的体积是 L。
20.(8分)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40-50 ℃时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 (填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式
。
(3)CuH溶解在稀盐酸中生成的气体是 (填化学式)。
(4)如果把CuH溶解在足量的稀硝酸中只生成NO气体,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com