
题目列表(包括答案和解析)
18. (8分)标准状况下,甲、乙、丙各取20mL相同浓度的盐酸,然后分别加入组成完全相同的镁铝合金粉末,得到下表有关数据。请填写相应空白项。
|
|
甲 |
乙 |
丙 |
|
金 属/g |
0.250 |
0.300 |
0.450 |
|
生成气体 /mL |
280 |
313.6 |
313.6 |
|
盐酸的浓度/mol/L |
1)
( ) |
||
|
镁铝的物质的量之比 |
2)
( ) |
17. (6分)下图是元素周期表的一部分,表中所列字母分别代表某一化学元素:
|
a |
|
|
|
b |
||||||||||||||
|
|
c |
|
|
d |
e |
|
|
|||||||||||
|
f |
|
g |
|
|
h |
|
i |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
j |
|
|
1) 由a、d、e三种元素形成的化合物中,能促进水的电离的化合物是 (填一种物质的化学式)
2) 将等物质的量的f、g的单质投入足量水中,反应后逐滴加入1mol/L的盐酸溶液,到100mL时能产生最大沉淀。则在该过程中一共放出 L气体(标况)
16.
 反应4NH3+5O2 4NO+6H2O在2升的密闭容器中进行,半分钟后,NO的物质的量由1.2mol增加到3.6mol,则此反应的平均速率
反应4NH3+5O2 4NO+6H2O在2升的密闭容器中进行,半分钟后,NO的物质的量由1.2mol增加到3.6mol,则此反应的平均速率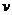 x(表示反应物的消耗速率或生成物的生成速率)为( )
x(表示反应物的消耗速率或生成物的生成速率)为( )
A.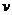 (O2)=0.05摩/(升·秒) B.
(O2)=0.05摩/(升·秒) B.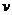 (NO)=0.06摩/(升·秒)
(NO)=0.06摩/(升·秒)
C.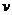 (H2O)=0.07摩/(升·秒)
D.
(H2O)=0.07摩/(升·秒)
D.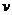 (NH3)=0.08摩/(升·秒)
(NH3)=0.08摩/(升·秒)
|
题序 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
答案 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

第II卷(共52分)
15. 19.2毫克铜跟适量的浓硝酸反应,铜全部作用后共收集到气体8.96毫升(标准状况),反应消耗的HNO3的物质的量可能是( )×10-3摩尔.(不考虑NO2与N2O4之间的转化)
A.0.8 B.0.9 C.1.0 D.1.2
14. 某温度下,将C12通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3三者的混合液,已知反应时被还原的氯元素与被氧化的氯元素的物质的量之比为7:2,则溶液ClO-与ClO3-的浓度之比为( )
A.1:1 B.2:1 C.3:5 D.5:3
13. 在50g浓度为c mol/L、密度为ρg/cm3 的氨水中加入一定量的水稀释成0.5c mol/L,则加入水的体积为( )
A.小于50mL B.等于50mL C.大于50mL D.等于50/ρmL
12. 已知①25℃、101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②25℃、101kPa下,碳的燃烧热是393.5kJ/mol。
今有120g碳不完全燃烧,所得混合气体对氧气的相对密度为1。则这个反应同时放出的热量是( )
A.1105kJ B.1812.5kJ C.2520kJ D.3935kJ
11. 用18 mol/L H2SO4溶液和铜片加热制得1mol SO2。下列说法不正确的是( )
A.反应中,被还原的硫酸为1mol
B.用111mL浓硫酸跟足量的铜反应能达到目的
C.用64g Cu与足量的浓硫酸反应能达到目的
D.反应中浓硫酸既表现出酸性,又表现出强氧化性
10.
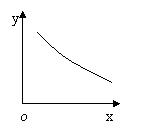 在一定条件下,向固定容积的密闭容器中充入一定量的B和C,发生反应: B(g)+ 2C(g)
在一定条件下,向固定容积的密闭容器中充入一定量的B和C,发生反应: B(g)+ 2C(g) 2A(g);ΔH<0, 达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是( )
2A(g);ΔH<0, 达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是( )
A.当X表示温度时,Y表示C的物质的量
B.当X表示压强时,Y表示A的产率
C.当X表示反应时间时,Y表示混合气体的密度
D.当X表示C的物质的量时,Y表示B的物质的量
9. 某无色混合气体可能由CH4、NH3、H2、CO、NO2、CO2和HCl中的某几种气体组成。在恒温恒压条件下,将混合气体通过浓H2SO4时,总体积基本不变;通过澄清石灰水,未见浑浊,但气体体积减少;再通过碱石灰后将剩余气体导出,它能在O2中能够点燃,燃烧产物不能使CuSO4粉末变色。则原混合气体( )
A.一定存在HCl和CO B.一定没有CH4、NH3、H2、NO2和CO2
C.一定存在HCl、CO和CO2 D.上述A、B、C判断均不合理
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com