
题目列表(包括答案和解析)
23.(8分,每小题2分)
⑴C
⑵NO2(g)+CO(g)=CO2(g)+NO(g);
ΔH=-234 kJ/mol
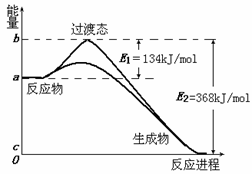
⑶(见右上图)
⑷434
21(6分)(1)BD(3分,选1个得1分,错选得0分)
 (2)反应不能自发进行 1051K
(2)反应不能自发进行 1051K
22.(1)g(2)a b d g(3)a b d(每空2分)
27、(10分)
⑴该平衡混合物中CO2的体积分数为 33.3% (2分)
⑵则反应向 逆反应方向(1分) ,CO2的体积分数可能是下列各值中的 D(2分)
⑶下列说法中正确的是 ( ①⑤(2分) )
 高三化学第一次阶段考试题
高三化学第一次阶段考试题
25.(11分)
(1)镉在元素周期表中第 5 周期,第 ⅡB 族。(各1分,共2分)
(2)写出步骤①反应的离子方程式 Cd+2H+=Cd2++H2↑,Zn+2H+=Zn2++H2↑(各1分,共2分)
(3)步骤②所加入的金属的名称是 锌(2分) ,如何处理“溶液”?
回收炼锌(1分) 。(共3分)
(4)镉在 阴 极析出,该电极材料是 镉板 (各1分,共2分)
(5)写出硫化钠沉淀镉离子的离子方程 Cd2++S2-=CdS↓ (1分) 。
26(11分)
(1)热化学方程式是N2H4(1)+O2(g)=N2(g)+2H2O;△H=-624kJ/mol(2分)
(2)①锌片上发生的电极反应是Cu2++2e-=Cu(2分)
②标准状况下的空气 112 L
(3)该反应的离子方程式是 ClO-+2NH3=N2H4+Cl-+H2O(2分) 。
(4)1阴极的电极反应式为 N2+6H++6e-==2NH3 (2分) 。
24、 (18分)
(1)的化学方程式为___2Cl-2e- = Cl2↑____________;溶液的pH_升高________
(2)反应的离子方程式为 _ Ca2++CO32-=CaCO3 ↓;Mg2++2OH-=Mg(OH)2↓ Fe3++3OH-=Fe(OH)3↓ (3)该钡试剂可以是 _ a、c ___ _
(4)加入试剂的合理顺序为 b 、c ______(选填a、b、c)。
(5),通过___蒸发____、冷却、过滤__________(填写操作名称)除去NaCl。
(6)由图示可知用离子交换膜法电解制碱工艺中___ NaCl (或淡盐水)____产品可循环使用。
(7)电解后NaOH的物质的量浓度为___7.14_______mo1·L-1。
23、(8分)
⑴其中属于有效碰撞的是 C (选填“A”、“B”或“C”);
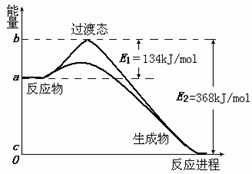 ⑵ 请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)ΔH=-234 kJ/mol ;
⑵ 请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)ΔH=-234 kJ/mol ;
⑶
⑷则上表中X= 434 。

22.(6分)(每空2分)
(1) 开始时液面在a mL处,继续添加液体至液面在b mL处,则所加液体体积为(a-b)mL的是__ g ______________。
(2) 仪器上标明了使用温度的是__ a b d g ___________。
(3) 用8.2 mL的浓盐酸配制一定物质的量浓度的稀盐酸,不可缺少的仪器是__ a b d
______________。
21、(6分)(1)操作以及结论不合理的是_ BD(3分,选1个得1分,错选得0分) ___
(2)判断反应CaCO3(s) ===CaO(s)+CO2(s)的自发方向 反应不能自发进行;发生自发反应时所需要的最低温度 1051K (已知:△H=178.2kJ·mol-1;△S=196.6 kJ·mol-1)
27、(10分)
⑴该平衡混合物中CO2的体积分数为
⑵则反应向 ,CO2的体积分数可能是下列各值中的 (填编号)
⑶下列说法中正确的是 ( )
28(10分)
⑴具有的优点是_______ ________(填一项)。NOx会导致酸雨、_ _等
⑵需要测量并记录的数据是______________。
⑶消耗的物质的量较多的可能是_______________(填字母),原因是___________ ___________________
高三化学第一次月考试题
班级 : 姓名 : 座号 : 分数:
第I卷(70分)
25.(11分)
(1)镉在元素周期表中第 周期,第 族。
(2)写出步骤①反应的离子方程式 。
(3)步骤②所加入的金属的名称是 ,如何处理“溶液1”? 。
(4)步骤④用“溶液2”作电解液,镉在 极析出,该电极材料是
(5)写出硫化钠沉淀镉离子的离子方程 。
26(11分)
(1)热化学方程式是
(2)①锌片上发生的电极反应是
②标准状况下的空气 L
(3)该反应的离子方程式是 。
(4)1阴极的电极反应式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com