
题目列表(包括答案和解析)
9.( )最新科技报道,美国夏威夷联合中心的科学家发现了新型氢粒子,这种新粒子是由3个氢原子核(只有质子)和2个电子构成,对于这种粒子,下列说法正确的是
A.这种粒子含有3个质子 B.它的组成可以表示为H3
C.这种粒子含有3个中子 D.是氢的一种新的同位素
7.( )某金属硝酸盐在受热分解时生成了金属氧化物、二氧化氮与氧气,且产物中NO2与O2的体积比为6∶1(同温同压下测得),则该硝酸盐分解时金属化合价的变化情况是
A.升高 B.降低 C.不变 D.不能确定
( )8.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羧基硫(COS),已知羧基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法正确的是
A.羰基硫的属于非极性分子 B.羰基硫的电子式为:
C.羰基硫沸点比CO2低 D.羰基硫分子中三个原子处于同一直线上
6.( )一些烃的燃烧热(kJ/mol)如下表,下列表达正确的是
|
化合物 |
燃烧热/kJ/mol |
化合物 |
燃烧热/kJ/mol |
|
甲烷 |
891.0 |
正丁烷 |
2878.0 |
|
乙烷 |
1560.8 |
异丁烷 |
2869.6 |
|
丙烷 |
2221.5 |
2-甲基丁烷 |
3531.3 |
|
乙烯 |
1411.0 |
乙炔 |
1300.0 |
A.热稳定性:正丁烷>异丁烷
B.乙烷燃烧的热化学方程式为:
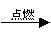 C2H6(g)+ O2(g) 2CO2(g)+3H2O(l) ;ΔH=-1560.8 kJ/mol
C2H6(g)+ O2(g) 2CO2(g)+3H2O(l) ;ΔH=-1560.8 kJ/mol
C.等物质的量的乙烯和乙炔完全燃烧,乙烯放出的热量多,故用氧烯焰来切割或焊接金属
D.相同质量的烃,碳的质量分数越大,燃烧放出的热量越多
5.( )可以鉴别甘油、乙醛、乙酸和甲酸四种无色水溶液的试剂是
A.新制Cu(OH)2悬浊液 B.FeCl3溶液
C.KMnO4溶液 D.浓溴水
4.( )下列离子方程式不正确的是
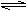 A.碳酸钠溶液呈碱性:CO32-+H2O HCO3-+OH-
A.碳酸钠溶液呈碱性:CO32-+H2O HCO3-+OH-
B.将少量二氧化碳气体通入次氯酸钠溶液:SO2+2ClO-+H2O=SO32-+2HClO
C.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4+
D.氯气通入澄清石灰水中:Cl2+2OH-=Cl-+ClO-+H2O
3.( )下列各组离子在相应的条件下一定能大量共存的是
A.在碱性溶液中:CO32-、K+、C1-、Na+
B.与铝粉反应放出氢气的无色溶液中:NO3-、Mg2+、Na+、SO42-
C.在c(H+)/c(OH-)==1×1013的溶液中:NH4+、Ca2+、C1-、K+
D.在中性溶液中:Fe3+、C1-、NO3-、A13+
2.( )用硫酸酸化的三氧化铬(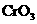 ),遇酒精后,其颜色由红变为蓝绿色,用这种现象可测得司机是否酒后驾车.反应如下:
),遇酒精后,其颜色由红变为蓝绿色,用这种现象可测得司机是否酒后驾车.反应如下:
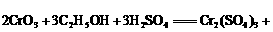
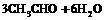 ,在此反应中,还原剂和氧化剂的物质的量之比是
,在此反应中,还原剂和氧化剂的物质的量之比是
A.2∶3 B.3∶2 C.1∶1 D.3∶1
1.( )氯化碘(ICl)的性质类似卤素,有很强的化学活动性。ICl跟Zn、H2O的反应:①2ICl+2Zn=ZnCl2+ZnI2 ②ICl+H2O=HCl+HIO 下列叙述中正确的是
A.在反应①中,ZnI2既是氧化产物又是还原产物
B.在反应①中,ZnCl2既是氧化产物又是还原产物
C.在反应②中,ICl既是氧化剂又是还原剂
D.在反应②中,ICl既不是氧化剂,又不是还原剂
25.(12分)Na2S2O3·5H2O(俗称海波)是照相业常用的一种定影剂。工业上制得的Na2S2O3·5H2O晶体中可能含有少量的Na2SO3和Na2SO4杂质。为了测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液30.00mL,充分反应后滤出硫,微热滤液使生成的SO2全部逸出。(Na2S2O3+H2SO4 = Na2SO4+SO2↑+S↓+H2O)测得有关实验数据如下(标准状况):
|
|
第一份 |
第二份 |
第三份 |
|
样品的质量/g |
7.540 |
15.08 |
35.00 |
|
二氧化硫的体积/L |
0.672 |
1.344 |
2.688 |
|
硫的质量/g |
0.8000 |
1.600 |
3.200 |
(摩尔质量:Na2S2O3·5H2O 248g/mol;Na2SO3 126g/mol;Na2SO4 142g/mol)
(1)计算所用硫酸溶液的物质的量浓度。
(2)分析以上实验数据,该样品中 (填写选项字母)
A.仅含有Na2S2O3·5H2O
B.含有Na2S2O3·5H2O和Na2SO3,无Na2SO4
C.含有Na2S2O3·5H2O、Na2SO3和Na2SO4
(3)若将30.16g该样品和一定量的上述硫酸溶液混合微热。试讨论:当加入硫酸的体积(aL)在不同取值范围时,生成的SO2体积(bL)的值(可用含a的关系式表示)。
24.(6分)在40mL0.10mol/LBaCl2溶液中,加入过量0.10mol/LH2SO4溶液,使沉淀完全。将反应后的混合物过滤,取滤液的一半,在滤液中加入25mL0.22mol/LNaOH溶液至恰好呈中性。试计算加入H2SO4溶液的体积
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com