
题目列表(包括答案和解析)
5.能说明Al的金属活动性比Cu强的事实是
A.以铝为阳极、铜为阴极电解硫酸铜溶液时,阳极铝溶解
B. 与氯气反应时,铝失去3个电子,而铜失去2个电子
C.常温下将铝和铜用导线连接放入到稀盐酸溶液中,铝为负极
D.常温下,铝在浓硝酸中钝化而铜不发生钝化
4.密度为0.91g/mL的氨水,质量分数为25%(即质量分数0.25),该氨水用等体积的水稀释后,所得溶液的质量分数
A.等于12.5% B.大于12.5% C.小于12.5% D.无法确定
3.下列说法正确的是
A.离子晶体中可能含有共价键,但不一定含有金属元素
B.分子晶体中一定含有共价键
C.非极性分子中一定存在非极性键
D.组成结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高
2.下列各种晶体熔化时只需克服分子间作用力的是
A.干冰 B.NaCl C.SiO2 D.C6H5ONa
1.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象
A.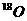
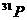
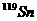
B.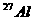
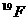
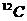
C.元素周期表中VA族所有元素的原子
D.元素周期表中第一周期所有元素的原子
15.(10分)丁烷在一定条件下可以按两种方式裂化:C4H10→C2H6+C2H4;C4H10→CH4+C3H6,现对发生裂化反应后的裂化气(不含丁烷)进行研究。
⑴探究裂化气的热值: 已知:
|
气体 |
CH4 |
C2H6 |
C2H4 |
C3H6 |
|
燃烧热(kJ/mol) |
Q1 |
Q2 |
Q3 |
Q4 |
①若44.8L(标准状况)裂化气充分燃烧放出热量QkJ,则Q的取值范围介于:
~ (用Q1、Q2、Q3、Q4表示,下同)。
②若将44.8L气体(标准状况)缓缓通过盛有足量溴的四氯化碳溶液中,发现洗气瓶增重33.6g,则44.8L(标准状况)气体完全燃烧放出的热量Q= kJ。
⑵测量与H2加成反应后气体总体积与氢气的体积分数关系:
另取裂化气与H2混合得5L混合气体,已知其中H2的体积分数ψ(H2)=X,在一定条件下使其充分反应,反应后气体的体积为VL。请列出V与X的函数关系式。
14.(8分)已知醇、醛在一定条件下能发生缩合反应,示例如下:
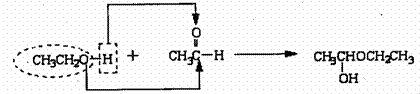
已知:
①1827年人们就发现有机物A,它的分子式为C13H18O7,与一分子水作用,水解生成B和C;
②B能发生银镜反应,B也可由淀粉水解得到,B的分子式为C6H12O6;
③C遇氯化铁溶液能发生显色反应,1molC与足量钠反应可生成1molH2;
④C在适当的条件下用适当氧化剂演化,可得D,D的分子式为C7H6O3,相对分子质量D比C大14;
⑤D有两个取代基,但不是间位,它与Br2在催化剂作用下发生一溴取代,产物有四种,D能与碳酸氢钠溶液反应;
⑥D与乙酸酐[(CH3CO)2O]反应,可得到常见药物E和乙酸,E能与碳酸氢钠反应放出二氧化碳。
试回答下列问题:
⑴写出结构简式:C E
⑵写出与D互为同分异构体,含有苯环且含有酯结构的结构简式: (只需写一种);
⑶B通常以六元环状结构存在,写出B的环状结构简式: 。
13.(10分)氰(CN)2的结构简式为N≡C-C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素。(CN)2和水反应可生成HCN和HCNO;(CN)2的氧化性比Br2弱,比I2强。
(1)下列有关反应的化学方程式不正确的是 (填选项标号)。
A.(CN)2和NaOH溶液反应:(CN)2+2NaOH====NaCN+NaCNO+H2O
B.MnO2和HCN反应:MnO2+4HCN △ Mn(CN)2+(CN)2↑+2H2O
C.向KCN溶液中加入碘水:I2+2KCN====2KI+(CN)2
D.在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2NaBr====2NaCl+Br2
(2)HCN的电子式为 。
(3)处理含CN-(其中C为+2价)的工业废水常用ClO-氧化,生成的CNO-(其中C为+4价)元素,反应的离子方程式如下:
aCN-+bClO-+2cOH-====dCNO-+eN2↑+fCO32-+bCl-+cH2O
上述化学方程式可能的配平系数有多组,请回答:
①方程式中e : f的值为 (填选项标号)。
A.1 B.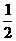 C.2 D.不能确定
C.2 D.不能确定
②若d=e=1, 则b= 。
12.(8分)根据初中化学知识,硫酸铜溶液与氢氧化钠溶液反应可得到蓝色沉淀,进一步将沉淀加热可生成黑色物质。小明做了这个实验:他在试管中倒入2mLCuSO4溶液,再加入一定量的氢氧化钠溶液,结果得到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热直至沸腾,观察不到有黑色CuO产生的现象。这是为什么呢?小明通过查找资料得知,该浅绿色沉淀物可能是溶解度极小的碱式硫酸铜,其化学式为Cu(OH)6SO4。
(1)请帮小明写出生成浅绿色沉淀的有关反应的化学方程式
(2)请帮小明设计-个实验,证明该浅绿色沉淀中含有硫酸根离子
________________________________________
__________________________________________________________________________。
11. (14分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
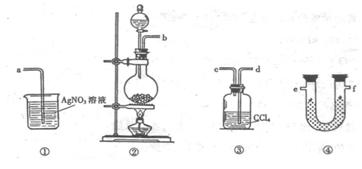
 ⑴请根据甲同学的意图,连接相应的装置,接口顺序:
⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接 , 接 , 接a。
⑵U形管中所盛试剂的化学式为 。
⑶装置③中CCl4的作用是 。
⑷乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在 之间(填装置序号)。瓶中可以放入 。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成 ,如果观察到
______________________________的现象,则证明制Cl2时有HCl挥发出来。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com