
题目列表(包括答案和解析)
23.(16分)某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:
一是发生氧化还原反应:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;
二是发生双水解反应:2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3。
为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
[实验Ⅰ]学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,作者设计这个实验的目的是
. 。
[实验Ⅱ]取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色“液体”是 ;向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是
. ;
将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,另一份加入BaCl2稀溶液,有少量白色沉淀生成。产生血红色现象的离子方程式是
. 。
[实验Ⅲ]换用稀释的FeCl3和Na2SO3溶液重复实验,Ⅱ、Ⅲ产生的现象完全相同。由上述实验得出的结论是 ;
若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是
. 。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①________________________________________________________________;
②________________________________________________________________。
21.(4分)下列实验操作或对实验事实的叙述正确
的是 (填序号)
① 为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液
② 向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
③ 使用胶头滴管的任何实验都不允许将滴管插入液面以下
④ 为了获得胆矾晶体,可将CuSO4溶液蒸干、灼烧到质量不再发生变化时为止
⑤ 不慎将苯酚沾到皮肤上,立即用酒精清洗;
⑥ 用石英坩埚高温熔融NaOH和Na2CO3的固体混合物
⑦ 配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入浓硝酸中,并不断搅拌;
⑧ 用洁净的玻璃棒蘸取稀H2SO4,点在pH试纸中部以测定此溶液的pH
22.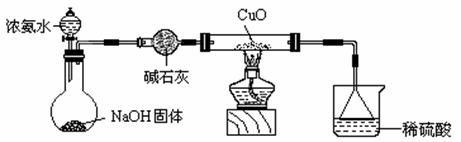 (10分) 利用如图所示的装置和其他必要的仪器用品,完成下列实验。
(10分) 利用如图所示的装置和其他必要的仪器用品,完成下列实验。
(1)证明氨气具有还原性。已知在加热条件下发生:2NH3+3CuO = N2+3Cu+3H2O。
① 碱石灰的作用是 稀硫酸的作用是 。
② 浓氨水与固体NaOH接触,为什么会逸出大量氨气?
。
③ 证明NH3具有还原性的实验现象是
。
(2)用吸收了足量氨气的硫酸溶液可以制取少量硫酸亚铁铵晶体。
已知:硫酸亚铁铵是淡蓝绿色晶体,在空气中性质比较稳定。硫酸亚铁铵在水中的溶解度小于硫酸铵和硫酸亚铁。制备硫酸亚铁铵的化学方程式为:
(NH4)2SO4+FeSO4+6H2O = (NH4)2Fe(SO4)2•6H2O。
在烧杯中的溶液里加入稀H2SO4调节溶液至酸性,加入适量的硫酸亚铁浓溶液后搅拌。为分离出硫酸亚铁铵晶体,还需要进行的实验操作是:(只要求填操作名称)
。
20. 将Mg、Cu组成的混合物26.4g投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入过量的4mol·L-1的NaOH溶液300mL,金属离子完全沉淀。则形成沉淀的质量是
A.43.2g B. 46.8g C. 53.6g D. 63.8g
顺德区2006学年第一学期高三年级期中考试
化学试卷
第Ⅱ部分 非选择题(共80分)
19.为提纯下列物质(括号内为杂质),所选用的除杂试剂与主要分离方法都正确的是
|
|
不纯物质 |
除杂试剂 |
分离方法 |
|
A |
苯(甲苯) |
KMnO4(酸化),NaOH溶液 |
分液 |
|
B |
NH4Cl溶液(FeCl3) |
NaOH溶液 |
过滤 |
|
C |
乙酸乙酯(乙酸) |
饱和Na2CO3溶液 |
分液 |
|
D |
苯(苯酚) |
浓Br2水 |
过滤 |
18.下列各选项所述的两个量:①HBr和HF的沸点; ②纯水在25℃和80℃时的pH值;③ 同温下分别在100g水中最多能溶解的无水CuSO4和CuSO4·5H2O的质量;④ 25℃时,等体积的pH值都等于3的盐酸和AlCl3溶液中,由水电离产生的H+浓度;⑤ 在NH3+NO→N2+H2O反应中,被氧化和被还原的N原子数 ;⑥ 耐火材料MgO和生石灰CaO的熔点;⑦ H-和H+离子半径。其中前者一定大于后者的是
A. ①②⑥⑦ B. ①②③⑤ C. ②⑥⑦ D. ⑤⑥⑦
17.下列关于晶体的说法一定正确的是
A.第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同
B.晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子
C.离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键
D.C60晶体(其结构模型如上图)中每个C60分子周围与它距离最近且等距离的C60分子有12个
16.在pH为4-5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法正确的是
A.加入纯Cu将Fe2+还原
 B.向溶液中加入(NH4)2S使Fe2+沉淀
B.向溶液中加入(NH4)2S使Fe2+沉淀
C.直接加水加热使杂质离子水解除去
D.在溶液中通入Cl2,再加入CuO粉末调节pH为4-5
15.在10mL2 mol·L-1的稀硝酸溶液中,加入1.92g铜粉,充分反应后,再向其中加入1 mol·L-1的硫酸溶液10mL,假设每步反应均充分进行,则最终溶液中c(Cu2+)为
A.1.50 mol·L-1 B.0.375 mol·L-1 C.0.50 mol·L-1 D.0.75 mol·L-1
14.下列反应的离子方程式正确的是
①硫酸铜溶液与氢氧化钡溶液反应: Ba2++ SO42_= BaSO4↓
②将金属钠加入水中 2Na + 2H2O = 2Na+ + 2OH - + H2 ↑
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
④氟气与水反应: F2+H2O=H+ +F -+ HFO
⑤小苏打溶液中加入少量的石灰水:Ca2+ +2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
⑥次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
⑦钠与硫酸铜溶液反应:Cu2++2Na =2Na+ +Cu
⑧氯气与水反应Cl2 + H2O = 2H+ + Cl - + ClO-
⑨纯碱溶液中滴加少量盐酸CO32- + H+ = HCO3-
A.①②⑤⑨ B.②③⑤⑨ C.④⑤⑥⑦ D.②③⑧⑨
13.青石棉(cricidolite)是一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,其化学式为Na2Fe5Si8O22(OH)2。青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法不正确的是
A.青石棉是一种复杂的硅酸盐
B.青石棉中含有一定量的石英晶体
C.青石棉的化学组成可表示为:Na2O·3FeO·Fe2O3·8SiO2·H2O
D.1mol青石棉能使1molHNO3被还原
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com