
题目列表(包括答案和解析)
30.下面所列的是中学化学实验室中几种常见的玻璃仪器:
①温度计 ②容量瓶 ③滴定管 ④烧杯 ⑤圆底烧瓶 ⑥量筒 ⑦玻璃棒
(1)在仪器上具体标明使用温度的是(不考虑温度计) (填写编号);可作反
应容器并可加热的是 (填写编号)
(2)需要用到温度计的实验是 (填写编号)
①用乙醇制取乙烯 ②石油分馏 ③浓硫酸稀释 ④测定硝酸钾的溶解度
(3)玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流。下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是(填字母代号)_________________。
A. 一定溶质质量分数溶液的配制
B. 用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
C. 用普通漏斗组成的过滤装置进行过滤实验
D. 用浓氨水和浓盐酸进行氨和氯化氢反应的实验
E. 用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验
F. 硫酸铜晶体里结晶水含量测定的实验
G.将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体
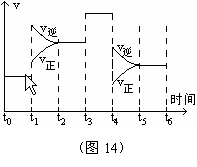
29、一密闭容器中发生下列反应N2+3H2 2NH3;ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图。回答下列问题:
2NH3;ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图。回答下列问题:
(1)处于平衡状态的时间段是_ _ A t0~t1 B,t2~t3 C,t3~t4 D,t5~t6
(2)t1、t3、t4时刻,体系中分别是什么条件发生了什么变化?
t1时刻 、t3时刻 、t4时刻
(3)下列时间段中,氨的百分含量最高的是( )
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
28.有机物A(C10H20O2)具有兰花香味,可用做香皂、洗发香波的芳香赋予剂。已知:
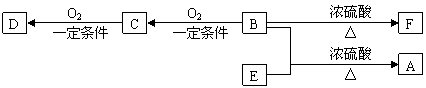 ①B分子中没有支链。
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯原子取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是 、 。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式: 、 。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2-甲基-1-丙醇和甲酸在一定条件下制取E。该反应的化学方程式是
27. X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: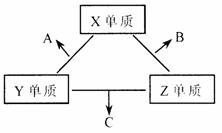
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10。 请回答下列问题:
(1)X元素在周期表中的位置是_________周期_________族。
(2)分析同主族元素性质的递变规律,发现B、C物质的沸点反常,这是因为它们的分子之间存在_________。
(3)①C的电子式是________________,C分子的结构呈________形。
②C在一定条件下反应生成A的化学方程式是__________________________。
③X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐。该盐的水溶液pH________7(填“大于”、“于小”、“等于” ),其原因是(写出离子方程式)__________________________。
(4)已知Y单质与Z单质生成C的反应是可逆反应,△H < 0。将等物质的量的Y、Z两种单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法正确的有_________。
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,Y、Z两种单质在混合气体中的物质的量之比为1
3]已知、的空间构型均为四面体,NH4+的结构式为 \s\up10(∣←N-,\s\up10(∣H(→表示
共用电子对由N原子单方面提供)。 请画出的结构式_____________________。
26. 同族元素的同类物质的结构、性质既有相似性,也有特殊性。回答下列问题:
⑴ 已知酸性FCH2COOH>CH3COOH,试推断:
①BrCH2COOH、②ClCH2COOH、③FCH2COOH的酸性由强到弱的顺序(填序号)_________________。
⑵ 已知AgCl可溶于稀氨水形成银氨溶液、AgBr可溶于浓氨水形成银氨溶液、AgI不溶于浓氨水,它们都不溶于水。试推断:
上述三种银盐在水中溶解度由大到小的顺序__________ ______________。
25. 下图中A、B、C分别是某课外活动小组设计的制取氨气并进行喷泉实验的三组装置示意图,制取NH3选用试剂如图所示,回答下列问题:

(1)用A图所示的装置可制备干燥的NH3:
①反应的化学方程式为:__________。装置中收集NH3的试管口放置棉花团的作用是:_________。
②干燥管中干燥剂能否改用无水CaCl2___________,理由是_________________________.
(2)用B图所示的装置可快速制取较大量NH3拟作喷泉实验。根据B图所示的装置及试剂回答下列问题:
①用化学方程式表示:浓氨水滴人CaO中有大量NH3逸出的过程:____________________.
②检验NH3是否收集满的实验方法是:________________________________。
(3)用C图所示的装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是__________,该实验的原理是:_____________________。
若测得C装置烧瓶中NH3的质量是相同状况下相同体积H2质量的10倍,则喷泉实验完毕后,烧瓶中水可上升至烧瓶容积的___________(填“几分之几”)。
24. 甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
(1) 写化学式:丙_________,E________。
(2)X的电子式为____________________。
(3) 写出A与H2O反应的化学反应方程式:___________________________________ 。
(4) 写出B与G溶液反应生成F的离子方程式: 。
(5) 在上图的反应中,不属于氧化还原反应的是(填序号)____________________。
23. 下列实验操作能达到实验目的的是__________________(填代号)。
A.向沸水中滴入少量浓FeCl3溶液,煮沸至呈红褐色,制取Fe(OH)3胶体
B.向盛有稀HNO3的试管中加入铜片,稍稍加热,观察生成的NO气体
C.将pH试纸湿润后用于鉴别NH3和HCl两种刺激性气体
D.用滴管吸取NaOH溶液滴入久置的FeSO4溶液中,制取Fe(OH)2
E.将充有NO2气体的密闭玻璃球放入热水中,验证温度对化学平衡的影响
22.有人建议将氢元素排在元素周期表的ⅦA族。下列事实能支持这一观点的是:①H原子得到一个电子实现最外电子层稳定结构;②氢分子的结构式为H-H;③与碱金属元素形成离子化合物M+[∶H]-;④分子中原子间的化学键都属于非极性键 ( )
A.只有①②③ B.只有①③④ C.只有②③④ D.有①②③④
第Ⅱ卷(非选择题,共56分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com