
题目列表(包括答案和解析)
4.下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是:
A.氯化镁、氢氧化钠 B.硫酸钠、氢氧化钡
C.氯化铝、氨水 D.溴化亚铁、氯水
2.下列事实不能用勒夏特列原理解释的是:
A.氨水应密闭保存,放置于低温处
B.在硫酸亚铁溶液中,加入铁粉以防止氧化变质
C.生产硝酸的过程中使用过量空气以提高氨气的利用率
D.实验室常用排饱和食盐水的方法收集氯气
3 下列可用氢键来解释的是:
A.浓的氢氟酸溶液中存在HF2-和H2F3- B.SiH4沸点比CH4高
C.水和乙醇分别与金属钠反应,前者比后者剧烈
D.H2O比H2S稳定,前者1000oC以上才分解,后者300 oC分解
1.六氟化硫分子呈正八面体,难以水解,在高电压下仍有良好的绝缘性,在电器行业有着广泛用途,但逸散到空气中会引起强温室效应。下列有关SF6的推测正确的是 :
A.SF6易燃烧生成二氧化硫 B.SF6中各原子均达到八电子稳定结构
C.高温条件下,SF6微弱水解生成H2SO4和HF D.SF6是极性分子
28、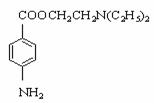 (11分)普鲁卡因为白色、细微的针状晶体,易溶于水;其针剂常用于临床局部麻醉剂。普鲁卡因的结构简式为:
(11分)普鲁卡因为白色、细微的针状晶体,易溶于水;其针剂常用于临床局部麻醉剂。普鲁卡因的结构简式为:
已知: ①将环氧乙烷(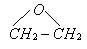 )通到二乙胺
)通到二乙胺 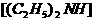 的醇溶液中可制备二乙胺基乙醇
的醇溶液中可制备二乙胺基乙醇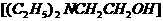
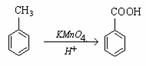
②烷基苯的支链可以氧化成羧基,如
③硝基苯在铁和盐酸的作用下,能被还原成苯胺(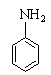 )
)
利用这些反应,可按以下步骤从甲苯得到普鲁卡因,其转变关系如下(X、Y分别为加入的试剂):

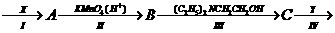 普鲁卡因
普鲁卡因
请填写下列空白:
(1)普鲁卡因在一定条件下水解的化学方程式____________ __________;
(2)写出下列物质的结构简式
A______ _____;B____ _______;C________ ___。
(3)所加试剂X、Y分别为
X______________________;Y______________________。
(4)各反应的类型是
I___________;II___________;III___________;IV___________。
27、(8分)已知:苯和卤代烃在催化剂作用下可以生成烷基苯和卤化氢。根据以下转化关系(生成物中所有无机物均已略去),回答下列问题:
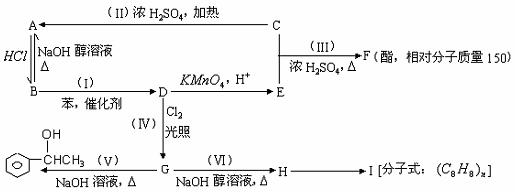
(1)在(I)-(Ⅵ)6个反应中,属于取代反应的是(填反应编号) 。
(2)写出物质的结构简式:F ,I 。
(3)写出B转化为D的化学方程式: 。
26、(13分)下图A-J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A-E和F-J中分别含有同一种元素。反应E→A+O2的条件未标出。
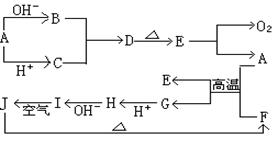
请填写下列空白:
(1)化合物H中的阳离子_______;D的化学式___________。
(2)A生成B反应的离子方程式是______________________________________。
(3)A和F的混合物叫做___________,发生反应的化学方程式是:
_________________________________________________________________。
(4)I→J反应的化学方程式是___________________________________________。
该反应过程中发生的现象是______________________________________。
25、(Ⅰ)(6分)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
(2)若上述关系中③是正确的,则溶液中溶质的化学式是 。
若上述关系中④是正确的,则溶液中溶质的化学式是 。
(3)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“大小”、“小于”、或“等于”,下同) c(NH3·H2O),混合前盐酸中c(H+)
和氨水中c(OH-)的关系c(H+) c(OH-)。
(Ⅱ)(5分)在密闭容器中,通入AmolN2和BmolH2,在一定条件下达到平衡,容器中还剩余CmolN2,
(1)生成NH3的物质的量为 ; (2)平衡时H2的转化率为 ;
(3)若把容器体积减小一半,则正反应速率 ,逆反应速率 ,
N2转化率 。(填“变大”、“变小”、“不变”)
24、 (6分)据著名网站-网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构。
(1)下列有关O4的说法正确的是
A、O4分子内存在极性共价键 B、合成O4的反应可看作核聚变反应,即不属于化学变化
C、O4与O3、O2都是氧的同素异形体 D、O4将来可用作更强有力的火箭推进的氧化剂
(2)含O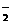 、O
、O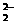 甚至O
甚至O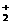 的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:

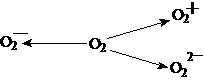
上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式: 。
(4)化合物O2[PtF6]中含有O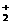 ,则O2[PtF6]属于____________化合物,有一种常见的含有钾元素和O
,则O2[PtF6]属于____________化合物,有一种常见的含有钾元素和O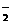 的氧化物可用作宇宙飞船中氧气来源,写出该反应的化学方程式:
的氧化物可用作宇宙飞船中氧气来源,写出该反应的化学方程式:
____________________________________________________________
23、(14分)某化学研究性学习小组讨论Fe3+和SO32-之间发生怎样的反应,提出了两种可能:
一是发生氧化还原反应:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;
二是发生双水解反应:2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3。
为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
[实验Ⅰ]学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,设计这个实验的目的是 。
[实验Ⅱ]取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色“液体”是 。向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是 。将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生血红色现象的离子方程式是 。
[实验Ⅲ]换用稀释的FeCl3和Na2SO3溶液重复实验,Ⅱ、Ⅲ产生的现象完全相同。由上述实验得出的结论是 。
若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是 。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
①________________________________________________________________;
②________________________________________________________________。
22、(10分)一般测定样品成分含量的实验应重复二至三次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙两位同学分别设计了如下实验方案:
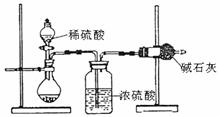 Ⅰ.甲同学的方案如右图所示:
Ⅰ.甲同学的方案如右图所示:
(1)根据甲同学的实验装置图分析,在每次实验过程
中所进行的称量操作至少要进行4次。
(2)甲同学重复测定了三次,得到碳酸钠的质量分数的数
据存在较大的偏差,你认为原因可能是 (填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收
D.加入稀硫酸的量不足,则可能造成误差
Ⅱ.乙同学的方案是:称取样品m g,并溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称量得固体n g
(1)混合物中碳酸钠的质量分数为(用m、n表示) 。
(2)洗涤沉淀的操作要点是 。
(3)Ca2+、Ba2+都可以使CO32-沉淀完全,但乙同学使用氯化钡溶液而不用氯化钙溶液
的原因是 ;测定CO32-的量,若使用氢氧化钡溶液而不用氢氧化钙溶液,结果将具有更高的精确度,原因
是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com