
题目列表(包括答案和解析)
24.(12分)物质A是化合物,B、C、D、K都是单质,反应②-⑤都是常见的工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
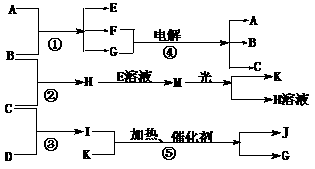
请填写下列空白:
(1)写出下列物质的化学式:B ; C ; D ;
K ;G ;J 。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M 。 ②I溶于G 。
(3)在通常状况下,若1 g C气体在B气体中燃烧生成H气体时放出92.3 kJ热量,则2 mol H气体完全分解生成C气体和B气体的热化学方程式为
23. (11分)据著名网站-网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构。
(1)下列有关O4的说法正确的是
A、O4分子内存在极性共价键
B、合成O4的反应可看作核聚变反应,即不属于化学变化
C、O4与O3、O2都是氧的同素异形体
D、O4将来可用作更强有力的火箭推进的氧化剂
 (2)含O
(2)含O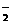 、O
、O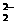 甚至O
甚至O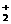 的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
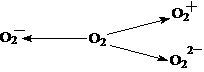
上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式: 。
(4)化合物O2[PtF6]中含有O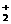 ,则O2[PtF6]属于____________化合物,有一种常见的含有O
,则O2[PtF6]属于____________化合物,有一种常见的含有O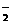 的氧化物可用作宇宙飞船中氧气来源,写出该反应的化学方程式:
的氧化物可用作宇宙飞船中氧气来源,写出该反应的化学方程式:
____________________________________________________________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
 用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KClO3质量 |
其它物质质量 |
待测数据 |
|
④ |
1.2 g |
无其他物质 |
|
|
⑤ |
1.2 g |
CuO 0.5 g |
|
|
⑥ |
1.2 g |
MnO2 0.5 g |
|
回答下列问题:
⑶上述实验中的“待测数据”指_____________;
⑷本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管;
⑸若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,__________________________________
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a._______________________________;b.CuO的化学性质有没有改变。
(一)制取氧化铜
①称取2 gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。回答下列问题:
⑴上述实验步骤中需要使用玻璃棒的是_______________(填实验序号),步骤①、③中研磨固体所用仪器的名称是___________________;
⑵步骤③中洗涤沉淀的操作是_____________________________________________
21.(8分)近年来,我国储氢纳米碳管研究获重大进展,电弧法合成的碳纳米管,常伴有大量物质--碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应的化学方程式为:
C+ K2Cr2O7
+ H2SO4(稀) CO2↑+ K2SO4 + Cr2 (SO4 ) 3+
.
CO2↑+ K2SO4 + Cr2 (SO4 ) 3+
.
(1)完成并配平上述反应的化学方程式。(2)此反应的氧化剂是 ,氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 (填选项编号)
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生11g气体物质,则转移电子的数目为 。
22.(14分)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
20.在一定量饱和的澄清石灰水中,加入5.60克CaO后充分搅拌,静置恢复到原来的温度,发现石灰水下部有白色不溶物形成,则下列叙述正确的是:
A.白色不溶物为CaO,其质量为5.60克
B.白色不溶物为Ca(OH)2,其质量为7.40克
C.石灰水的浓度和质量均不会变化
D.石灰水的质量将会减少,石灰水的pH不会发生变化
19.羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00mL0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65mL 0.020mol/L的KMnO4酸性溶液完全作用(已知:FeSO4+ KMnO4+ H2SO4= Fe2(SO4)3+ K2SO4+ MnSO4+ H2O(未配平),则在上述反应中,羟胺的氧化产物是:
A.N2 B.N2O C.NO D.NO2
18.在容积不变的密闭容器中存在如下反应: 2SO2(g)+O2(g) 2SO3(g)
△H<0
2SO3(g)
△H<0
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
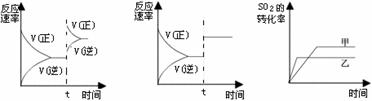
I II III
A.图I研究的是t时刻增大O2的浓度对反应速率的影响
B.图II研究的是t时刻加入催化剂后对反应速率的影响
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且甲的温度较低
17.已知热化学方程式2SO2(g)+
O2(g)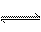 2
SO3(g) △H= -Q kJ/mol(Q>0),则下列说法正确的是:
2
SO3(g) △H= -Q kJ/mol(Q>0),则下列说法正确的是:
A.2molSO2(g)和1mol O2(g)所具有的内能小于2 molSO3(g)所具有的内能
B.将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QKJ的热量
C.升高温度,平衡向逆反应移动,上述热化学方程式中的Q值减小
D.如将一定量SO2(g)和 O2(g)置于某密闭容器中充分反应后放热QKJ,则此过程中有2molSO2(g)被氧化
16.在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量浓度之比为:4:2:1,现加入适量的铁粉,使溶液中的三种离子的物质的量浓度之比为:1:3:9,则投入的铁粉与原溶液中Cu2+的物质的量之比为:
A、5:4 B、4:5 C、3:5 D、5:6
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com