
题目列表(包括答案和解析)
4.类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( )
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②Fe3O4可写成FeO·Fe2O3;Pb3O4也可写成PbO·Pb2O3
③铝和硫直接化合可以得到Al2S3;铁和硫直接化合也可以得到 Fe2S3
④不能用电解熔融的AlCl3来制取金属铝;也不能用电解熔融的MgCl2来制取金属镁
A.①③④ B.②③ C②③④ D.①②③④
3.在含有I-离子且滴加酚酞显红色的溶液中,能大量共存的离子组是
A.SO42-、NO3-、Fe2+、Al3+ B.Na+、Ba2+、Cl-、AlO2-
C.Cl-、Na+、K+ 、ClO- D.NH4+、K+、Cl- 、SO32-
2.下列图象是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的图象是
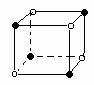
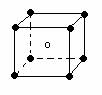
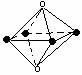
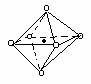
⑴ ⑵ ⑶ ⑷
A、图⑴和图⑶ B、图⑵和图⑶ C、图⑴和图⑷ D、只有图⑴
1.下列说法正确的是
A.铅笔芯的主要成分是金属铅
B.CO气体有毒,在生有炉火的居室中多放几盆水,可吸收CO
C.液氯罐中的液氯泄漏时,可将其移入水塘中,并向水塘中加入生石灰
D.夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风
29.(12分)将Mg粉放入盛有CO2和O2混合气的密闭容器中充分燃烧。
(1)若Mg粉的质量为6.0 g,反应后容器内O2有剩余,则在反应后容器内的固体
物质中一定含有______________,该固体物质的质量为________________; (2)若Mg的质量为a g,混合气体的体积为b L,反应后容器内O2有剩余,则在b L
混合气中,V (O2)的取值范围是_____________________________________;
(3)若Mg粉的质量仍为a g,燃烧后Mg粉和气体均无剩余,则反应后容器内固体物质的质量的最大值是______________________________________________。
(气体体积均已折算成标准状况下的数据)
28.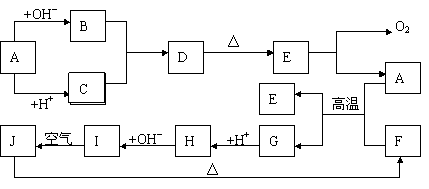 (14分)下图中A-J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A-E和F-J中分别含有同一种元素,框图中有的生成物被略去,反应E→A+O2的条件未标出。请填写下列空白:
(14分)下图中A-J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质。已知A-E和F-J中分别含有同一种元素,框图中有的生成物被略去,反应E→A+O2的条件未标出。请填写下列空白:
(1)化合物H中的阳离子是 ___________;D的化学式是 _________________。 (2)A生成B反应的离子方程式是 __________________________________________。 (3)B和C反应的离子方程式是 ____________________________________________。 (4)A和F反应的化学方程式是 ____________________________________________。 (5)I→J反应的化学方程式是 _____________________________________,
该反应过程中发生的实验现象是 _________________________________ 。
27.(18分)我国著名化学家侯德榜先生发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉中内外。“侯氏制碱法”的基本做法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱。它的反应原理可用下列化学方程式表示:
|
某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下一套实验装置
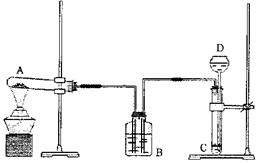
实验室可选药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化铵、氯化钠
(1)选用最合适的试剂的名称A ;D
(2)本实验具体操作过程中,应先通 气体,再通 气体;
原因是
(3)指出该装置的至少两处错误
(4)在改进装置后,该同学进行了实验,实验所用的饱和NaCl溶液中含溶质58.5g,实验最后得到无水碳酸钠26g,则其产率为 ;该同学针对其实验结果,认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是
(5)在“侯氏制碱法”的工业生产中,原料的利用率高,大大降低了成本。请问本实验中哪些物质可重复利用?
26. (16分)材料科学是近年来化学研究的热点之一。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性,它是以中学化学中的常见物质为原料来生产的,如下虚线框外为其生产过程;线框内的其他转化是为探究C的组成而设,G、H均为难溶于水的白色固体;图中C、M、K均含A元素,C物质遇水强烈水解,能生成一种白色胶状物质F和E的酸雾,其余物质均为中学化学常见物质。请回答下列问题:
(16分)材料科学是近年来化学研究的热点之一。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性,它是以中学化学中的常见物质为原料来生产的,如下虚线框外为其生产过程;线框内的其他转化是为探究C的组成而设,G、H均为难溶于水的白色固体;图中C、M、K均含A元素,C物质遇水强烈水解,能生成一种白色胶状物质F和E的酸雾,其余物质均为中学化学常见物质。请回答下列问题:
(1)指出K可能所属的晶体类型__________。
(2)写出化学式:单质B________,化合物F__________。
(3)写出上述反应的离子反应方程式:
⑤__________________________________________________________________________
⑥__________________________________________________________________________
(4)写出反应④的化学反应方程式 .
13.某无色溶液可能由Na2CO3、MgCl2、NaHCO3、BaCl2中的一种或几种混合而成,向溶液中加入烧碱溶液出现白色沉淀,加入稀硫酸也出现白色沉淀并放出气体。据此分析,下述组合判断中正确的是
①肯定有BaCl2 ②肯定有MgCl2 ③肯定有NaHCO3 ④肯定有NaHCO3或Na2CO3
⑤肯定没有MgCl2
A.①②③ B.①③ C.②④ D.①③⑤
12.2.1g Mg、Al混合物投入足量盐酸中产生2240mLH2(标准状况),然后加入1mol/LNaOH溶液充分反应后,过滤、洗涤、干燥后固体的质量不可能为
A.3.0g B.3.5g C.5.5 D.5.6g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com