
题目列表(包括答案和解析)
22.(8分)某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了NaNO3.Cu(NO3)2.AgNO3。(加热及夹持装置未画出)
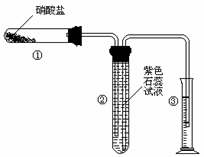
(1)甲同学加热的是NaNO3。加热过程发现:装置②中产生气泡,部分石蕊试液被压至装置③中;用带火星的木条检验②中的气体,木条复燃;分析装置①中剩余的固体得知,剩余固体中含有N元素,且显+3价。请写出NaNO3受热分解的化学方程式: 。
(2)乙同学加热的是Cu(NO3)2。加热过程发现:装置②中也有气泡产生,但在上升的过程中消失。石蕊试液逐渐变为红色,液体几乎不被压至装置③中。装置①中的固体逐渐变为黑色。请写出Cu(NO3)2受热分解的化学方程式: ;
(3)丙同学加热的是AgNO3。加热过程发现:装置②中也有气泡产生,但在上升的过程中气泡部分消失,英才剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:
 (Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,
(Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,
 (Ⅱ)2AgNO3 2Ag+2NO2↑+O2↑。请你分析,可能正确的是哪一个并说明
(Ⅱ)2AgNO3 2Ag+2NO2↑+O2↑。请你分析,可能正确的是哪一个并说明
由: ;
请你设计一个简单的实验证明你的结论是正确的: ;
(4)由上述3个实验的结果,请你推测:硝酸盐受热分解的产物可能与
有关。
20.(8分)通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
键能/ KJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低Y(填>或<=SiC______ Si; SiCl4 ______ SiO2
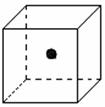 (2)右图立方体中心的“●”表示硅晶体中的一个原子,
(2)右图立方体中心的“●”表示硅晶体中的一个原子,
请在立方体的顶点用“●”表示出与之紧邻的硅原子。
(3)工业上高纯硅可通过下列反应制取:
 SiCl4 (g)
+ 2H2(g) Si(s) +
4HCl(g)
SiCl4 (g)
+ 2H2(g) Si(s) +
4HCl(g)
该反应的反应热△H = ___________ KJ/mol
 21.(8分)根据反应框图填空,已知反应①-⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120。
21.(8分)根据反应框图填空,已知反应①-⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120。
(1)写出A、B的化学式
A__________________ B____________________
(2)写出下列化学反应方程式或离子方程式:
反应③的化学方程式_________________________________________________
反应⑤的离子方程式_________________________________________________
(3)写出反应①所使用设备的名称_________________________________
19.(8分)已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、盐酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因___________________________________________________________________。
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池?__________,若能,请写出电极反应式,负极__________________,正极_________________。(若不能,后面两空不填)
(3)若电池反应为:Cu + 2H+ = Cu2+ + H2↑,该池属于原电池还是电解池?__________,请写出各电极的电极材料和电解质溶液_________________________________。
18.(8分)为防止碘缺乏病,Y通常在食盐中加入KIO3。
(1)用淀粉碘化钾溶液和稀硫酸可定性检验出食盐中的IO3-,表示该反应的离子方程式是________________________________________,若要确认食盐中还含有K+,方法是______________________________________________________________。
(2)工业上以石墨和铁为电极电解KI溶液制取KIO3。电解时,石墨作_________(填“阳极”或“阴极”),石墨电极上的电极反应式是____________________________,电解过程中铁电极附近溶液pH__________(填“变大”、“变小”或“不变”)。
17.(6分) 在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,有关反应的离子方程式是__________________;在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失,有关反应的离子方程式是__________________________。从以上事实可知,ClO-、I2.SO42-的氧化性由弱到强的顺序是___________________。
16.用6.02×1023表示阿伏加德罗常数(NA)的值,下列说法中正确的是 ( )
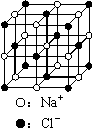 A.在SiO2晶体中,若含有1mol Si原子,则含Si-O
A.在SiO2晶体中,若含有1mol Si原子,则含Si-O
键数为2NA
B.6.8 g熔融的KHSO4中含有6.02×1022个阳离子
C.23.4 g NaCl晶体中含有6.02×1022个右图所示的结构单元
D.用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中,
胶粒数等于0.1 NA
15.下列反应的离子方程式正确的是 ( )
①往硝酸银溶液中滴加少量氨水:Ag++2NH3==[Ag(NH3)2]+
②将金属钠加入水中 2Na + 2H2O = 2Na+ + 2OH - + H2 ↑
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
④氟气与水反应: F2+H2O=H+ +F -+ HFO
⑤小苏打溶液中加入少量的石灰水:Ca2+ +2OH-+2HCO3-=CaCO3↓+CO32- +2H2O
⑥次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
⑦钠与硫酸铜溶液反应:Cu2++2Na =2Na+ +Cu
⑧氯气与水反应Cl2 + H2O = 2H+ + Cl - + ClO-
⑨纯碱溶液中滴加少量盐酸CO32- + H+ = HCO3-
A.①②⑤⑨ B.②③⑤⑨ C.④⑤⑥⑦ D.②③⑧⑨
14.下列物质的保存方法正确的是 ( )
①少量金属钠保存在冷水中
②浓硝酸盛放在无色试剂瓶中
③少量金属钾保存在煤油中
④氢氧化钠溶液盛放在带有橡胶塞的试剂瓶中
⑤氯水存放在带玻璃塞的无色细口瓶中
⑥碳酸钠固体保存在带橡胶塞的细口瓶中
⑦氢氟酸保存在塑料瓶中
A.②③④⑦ B.③④⑥⑦ C.③④⑦ D.①③④⑦
13.根据下表下列叙述中正确的是: ( )
|
序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
|
|
FeCl3 |
|
② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
|
③ |
KClO3 |
HCl(浓) |
|
Cl2 |
Cl2 |
|
④ |
KMnO4 |
HCl(浓) |
|
Cl2 |
MnCl2 |
A.表中第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.氧化性比较: KMnO4>Cl2>Fe3+>Br2>Fe2+
C.还原性比较: H2O2>Mn2+>Cl-
D.④的离子方程式配平后,H+的化学计量数为16
11.有两只串联的电解池,甲池盛有CuSO4溶液,乙池盛有一定量某硝酸盐的稀溶液,用惰性电极电解,当甲池的阴极上析出1.6gCu时,乙池的阴极上析出0.45g固体,则乙池的溶质可能是 ( )
A.NH4NO3 B.Al(NO3)3 C.Cu(NO3)2 D.Mg(NO3)2
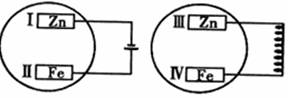 12.把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示,该图为平面透视图),经过一段时间后,首先观察到溶液变红的区域是 ( )
12.把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示,该图为平面透视图),经过一段时间后,首先观察到溶液变红的区域是 ( )
A.Ⅰ和Ⅱ附近 B.Ⅰ和Ⅳ附近 C.Ⅱ和Ⅲ附近 D.Ⅱ和Ⅳ附近
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com