
题目列表(包括答案和解析)
26.将等物质的量的A、B、C、D四种物质混合,发生如下反应:a A + b B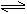 c C + d D,已知C是固体,当反应进行一段时间后,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol,此时反应达到化学平衡.
c C + d D,已知C是固体,当反应进行一段时间后,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol,此时反应达到化学平衡.
⑴ 化学方程式中各物质的化学计量数是:
a= 、b= 、c= 、d= .
⑵ 如果只改变压强,反应速率发生变化,但平衡不发生移动,则反应中各物质的聚集状态分别是A 、B 、D .
⑶ 如果只升高温度,反应一段时间后,测知A、B、C、D的物质的量相等.则该反应的正反应是 (填“吸热”或“放热”)反应.
25、下列事实中不能用勒夏特列原理解释的是( )
A.往H2S水溶液中加碱有利于S2-的增加
B.高压有利于合成氨的反应
C.500℃左右比室温更有利于合成氨的反应
D.制取乙酸乙酯实验中及时蒸馏出乙酸乙酯有利于提高反应物的转化率
24. 在容积固定的4L密闭容器中,进行可逆反应:
X(g)+2Y(g)
在容积固定的4L密闭容器中,进行可逆反应:
X(g)+2Y(g)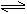 2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率V(正)、V(逆)与时间t的关系如右图所示.则图中阴影部分面积表示( )
2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率V(正)、V(逆)与时间t的关系如右图所示.则图中阴影部分面积表示( )
A.X的物质的量的减少 B.X的浓度的减少
C.Y的物质的量的减少 D.Z的浓度的增加
23.可逆反应 A(s) + mB(g) 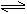 nC(g) 达到平衡时,温度和压强对该反应的影响如图所示.图中压强P1>P2,X轴表示温度,Y轴表示平衡混合气体中B的体积分数.据此可判断( )
nC(g) 达到平衡时,温度和压强对该反应的影响如图所示.图中压强P1>P2,X轴表示温度,Y轴表示平衡混合气体中B的体积分数.据此可判断( )
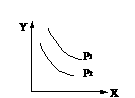 A.上述反应是放热反应,且m+1<n
A.上述反应是放热反应,且m+1<n
B.上述反应是放热反应,且m<n
C.上述反应是吸热反应,且m+1>n
D.上述反应是吸热反应,且m<n
22.在密闭容器中反应aX(g)+bY(g)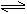 cZ(g)+dW(g)达到平衡时,X的浓度为0.5mol/L,若将容器的容积扩大到原来的2倍,当达新平衡时X的浓度降为0.3mol/L.下列叙述中不正确的是( )
cZ(g)+dW(g)达到平衡时,X的浓度为0.5mol/L,若将容器的容积扩大到原来的2倍,当达新平衡时X的浓度降为0.3mol/L.下列叙述中不正确的是( )
A.平衡向逆反应方向移动 B.a+b>c+d
C.Z的体积分数增加 D.Y的转化率下降
21.已知298K时,2SO2(g)+O2(g)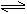 2SO3(g),ΔH=-197kJ/mol .在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量为Q1;向另一个体积相同的密闭容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出的热量为Q2,则下列关系正确的是( )
2SO3(g),ΔH=-197kJ/mol .在相同的温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量为Q1;向另一个体积相同的密闭容器中通入1molSO2、0.5molO2和1molSO3,达到平衡时放出的热量为Q2,则下列关系正确的是( )
A.Q2<Q1<197 kKJ B.Q2=Q1=197KJ C.Q1<Q2<197KJ D.Q1=Q2<197KJ
19. 可逆反应2X(g)+Y(g)
可逆反应2X(g)+Y(g)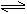 2Z(g)在不同温度(T)和不同压强(P)条件下产物Z的物质的量n(Z)与反应时间t的关系如图所示,则下列判断中正确的是
2Z(g)在不同温度(T)和不同压强(P)条件下产物Z的物质的量n(Z)与反应时间t的关系如图所示,则下列判断中正确的是
A.T1<T2,P1<P2 B.T1<T2,P1>P2
C.T1>T2,P1>P2 D.T1>T2,P1<P2
|
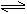 2Z(g),ΔH<0. 在不同温度(T)、不同压强(P1>P2)条件下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为( )
2Z(g),ΔH<0. 在不同温度(T)、不同压强(P1>P2)条件下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为( )18.将4 mol A 气体和 2 mol B 气体在2 L的容器中混合并在一定条件下发生如下反应:
2A(g) + B(g)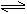 2C(g).若经2 s 后测得生成物C 的浓度为0.6 mol/L,现有下列几种说法:
2C(g).若经2 s 后测得生成物C 的浓度为0.6 mol/L,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol/(L·s)
②用物质B表示的反应的平均速率为0.6 mol(L·s)
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol/L
其中正确的是( )
A.①③ B.②③ C.①④ D.③④
17.一真空密闭容器中盛有1mol PCl5,加热到200℃时发生如下反应PCl5(g)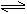 PCl3(g)+Cl2(g),达到平衡时,PCl5所占体积分数为a %.在相同温度下,若在同一容器中,最初投入的是2mol PCl5,反应达到平衡时PCl5所占体积分数为b %.则a和b的正确关系是( )
PCl3(g)+Cl2(g),达到平衡时,PCl5所占体积分数为a %.在相同温度下,若在同一容器中,最初投入的是2mol PCl5,反应达到平衡时PCl5所占体积分数为b %.则a和b的正确关系是( )
A.a>b B.a<b C.a=b D.无法比较
16.达到化学平衡时,两容器内NO2转化为N2O4的转化率是( )
A.α(A)>α(B) B.α(A)<α(B) C.α(A)=α(B) D.无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com