
题目列表(包括答案和解析)
6. 下列有关说法正确的是 ( )
A.溴乙烷水解后的碱性溶液不能用稀硝酸酸化,因为稀硝酸会把Br-氧化,再加入AgNO3溶液则不会产生浅黄色沉淀
B.为提高高锰酸钾溶液的氧化能力,用盐酸将KMnO4溶液酸化
C.证明CH3CH2CH=CHCH2CHO分子中有碳碳不饱和键的方法:向其中加酸性高锰酸钾溶液,高锰酸钾溶液褪色
D.检验溶液中是否含有SO42-时,在无其它阳离子干扰时,所加的BaCl2溶液用盐酸酸化。
5.下列各组物质,可用一种试剂加以区别的是( )
①四种黑色固体:FeO、Fe、CuO、C
②四种白色粉末:(NH4)2SO4、NH4CI、Na2SO4、NaCI
③四种无色溶液:乙醛、乙酸、甲酸、乙醇
④四种有机物:苯、四氯化碳、无水乙醇
A.只有①② B.只有③④ C.只有①②④ D.全部
4.有关化学用语正确的是( )
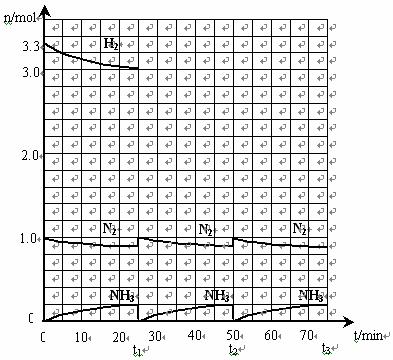
A.丁烯的最简式C4H8 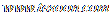 B.丙醇的结构简式C3H8O
B.丙醇的结构简式C3H8O
C.四氯化碳的电子式::Cl:C:Cl: D.乙炔的分子式是:C2H2
3.下列过程中属于化学变化的是( )
①白色的硫酸铜粉末久置于空气中变成蓝色 ②同素异形体之间的互变
③福尔马林用来浸制标本 ④同分异构体之间的互变
⑤蜂蚁螫咬处涂稀氨水或小苏打溶液可以减轻痛苦 ⑥氯化钠溶液通电后导电
A.只有①②④⑤ B.①②③④⑤⑥ C.只有③④⑤ D.只有①④⑤
2.消毒剂在日常生活、医疗、卫生、防疫中有重要作用,下列消毒剂的使用不正确是( )
A.过氧乙酸、漂白精是常用的消毒液
B.食品加工、消毒防腐常使用福尔马林
C.因患禽流感而被隔离的地区,常用生石灰处理
D.医疗上常用75%的酒精进行消毒
1.石油是一种重要能源,人类正面临着石油短缺,油价上涨的困惑。以下解决能源问题的方法不当的是 ( )
A.大量使用木材作燃料 B.推广使用乙醇汽油
C.开发风能 D.开发太阳能
25、(8分)某资料说铁锈的成分为Fe2O3·H2O和FeCO3的混合物。根据此记载,某实验兴趣小组设计下列实验来验证其中是否含有碳酸亚铁。
①取一高度腐蚀的干燥铁钉,称其质量为10.04g,在氮气保护下,充分加热,冷却后称得质量为8.92g。
②将①得到的残渣投入到5.00mol/L的硫酸中,不断添加硫酸直至残渣完全溶解时,恰好用去硫酸31.00mL。整个过程无气体放出。试回答下列问题:
⑴铁锈中是否含有碳酸亚铁?理由是?
⑵锈蚀的铁钉中含Fe2O3·H2O多少克?
24、(8分)将3.20g Cu溶于B mol/L过量的硝酸溶液30.0 mL中,假设硝酸的还原产物只有NO2和NO,反应结束后,将所剩溶液加水稀释至1000 mL,测得c(NO3-)=0.200 mol/L。
(1)试求稀释后溶液的pH。
(2)生成的气体中NO2和NO的物质的量(可以含有B的代数式表示)。
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:
2NO2+2NaOH=NaNO3+NaNO2+H2O,NO+NO+2NaOH=2NaNO+H2O
若生成的混合气体能被NaOH溶液完全吸收,试讨论B的取值范围。
23、(10分) 在实验室中进行合成氨工业的模拟实验,当反应进行一段时间,并建立相应的平衡以后,及时分离出氨并补充与起始原料比相同的氮气和氢气,以实现连续的生产过程,在1L的密封容器中,在一定条件下发生如下反应。
N2(g)+3H2(g) 2NH3(g);ΔH<0
2NH3(g);ΔH<0
 请根据图示回答下列问题:
请根据图示回答下列问题:
⑴反应起始时,氮气与氢气的物质的量之比n(N2)∶n(H2)=_____∶_____。在15分钟时合成氨反应第一次达到平衡,其中以H2的浓度变化所表示的平均化学反应速率为________。
⑵在t1时,曲线发生变化的原因是________、_________。请计算氢气在t1起点时的坐标(______,______)以及在t2平衡时的坐标(____,____)。并在图中画出在t1-t2之间氢气的物质的量变化曲线。
⑶为达到图示中t2的平衡状态,在t1-t2之间需要采取的措施是______。
a.扩大容器的体积 b.升高温度 c.降低温度 d.缩小容器的体积
⑷经历十次上述的循环过程,计算在t11达到平衡时,N2和H2的物质的量之比n(N2)∶n(H2)=____∶____,整个过程中N2和H2的总转化率之比a(N2)∶a(H2)=____∶____。
⑸根据以上计算结果,请你建议合成氨反应的最佳原料比是:n(N2):n(H2)=______。
22、(8分)我国是最早记载丹砂的药用价值和炼制方法的,为了使人们重视丹砂,1982年我国发行面值为10分的丹砂邮票。汞单质和化合物在工业生产和科学研究上有其广泛用途。丹砂炼汞的反应包括以下两个反应:反应Ⅰ HgS +O2 Hg +SO2
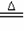
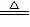
反应Ⅱ 4HgS +4CaO 4Hg +3CaS + CaSO4
请试完成下列问题:
(1)HgS与氧气反应,氧化剂是 。
(2)请标出反应Ⅱ中电子转移的方向和数目。
(3)得到的汞中含有铜等杂质,工业上常用5%的硝酸洗涤,写出除去少量铜杂质反应的离子方程式: 。
(4)已知Hg(NO3)2溶液中加入Hg,存在如下平衡:Hg + Hg2+
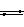 Hg22+ ,提高Hg22+浓度的方法是:
。
Hg22+ ,提高Hg22+浓度的方法是:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com