
题目列表(包括答案和解析)
21.CO不仅是家用煤气的主要成分,也是重要的化工原料。美国近年来报导了一种低温低压催化工艺,把某些简单的有机物经“羰化”反应后可以最后产生一类具有优良性能的装饰性高分子涂料、粘合剂等。如下图所示:
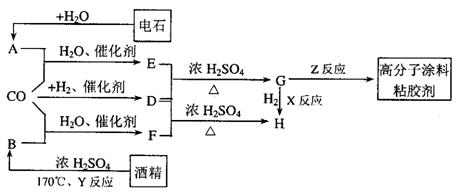
图中G(RCOOR)的一种同分异构体是E的相邻同系物;而H的一种同分异构体则是F的相邻同系物。已知D由CO和H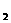 按物质的理之比为1∶2完全反应而成,其氧化产物可发生银镜反应:H是含有4个碳原子的化合物。试写出:
按物质的理之比为1∶2完全反应而成,其氧化产物可发生银镜反应:H是含有4个碳原子的化合物。试写出:
(1)结构简式:E_____________、G_________________、R’基____________。
(2)G的两个同类别分异构体的结构简式(不带R字母)________________________及__________________________________。
(3)反应类型:X_______________、Y_________________、Z_____________________。
(4)写出下列转化的化学方程式:
 ①A+CO+H
①A+CO+H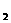
 E;②F+D
H。
E;②F+D
H。
①______________________________________________________________。
②______________________________________________________________。
20.(11分)
A、B、C、D、E、F六种物质在一定条件下有如所听示的相互转化关系,所有反应物和生成均已给出。
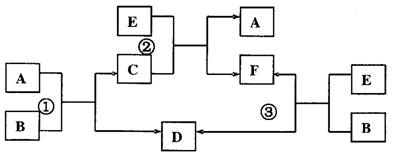
(1)若反应①、②、③均为溶液中的置换反应,A、D、E为常见金属单质,则A、D、E的还原性由强到弱的顺序为____________________。请写出满足以上要求的离子方程式:
反应①________________________________________________________________。
反应②________________________________________________________________。
(2)若反应①、②、③均为复分解反应。请写出满足要求的化学方程式:
反应①________________________________________________________________。
反应②________________________________________________________________。
(3)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应①的化学方程式是_____________________________________________________。
19.(9分)
A、B、C、D都是短期元素,原子半径:D>C>A>B。已知:A、B同周期, A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍。试回答:
(1)写出元素的名称:A____________________、C_______________________。
(2)写出由B、D组成的两种化合物的电子式分别为:_____________、______________。
(3)C的固态氧化物属于______________晶体。写出表示C的氧化物的一种重要的工业用途___________________________________________________。
(4)A、C的最高价氧化物对应水化物中酸性较强的是_______________(写水化物的分子式)
(5)写出C的氧化物与D的最高价氧化物对应水化物反应的离子方程式:____________
18.(8分)
某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置己略去,粗黑线表示乳胶管。请填写下列空白:
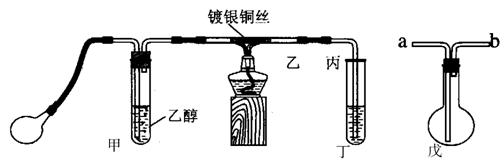
(1)甲装置常常浸在温度为70-80的水浴中,目的是________________________
(2)实验时,先加热玻璃管乙中的镀银钢丝,约1分钟后鼓入空气,此时铜可丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
(3)乙醇的催化氧化反应是______反应(填“放热”或“吸热”),该反应的化学方程式为______________________________________________
(4)控制鼓气速度的方法是_____________________________________________,若鼓气速度过快则会_________________________________________________________,若鼓气速度过慢则会______________________________________________________
(5)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接_____________、______________接丙。
17.(6分)
(1)指出下列实验仪器和用品(已洗涤干净)使用时的第一步操作:
①红色石蕊试纸检验氨气的性质__________________________________________;
②滴定管(中和滴定)_____________________________________________________
(2)下列有关实验的叙述中,不正确的有:_____________________(填序号)
①蒸干AlCl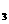 溶液可得纯净的无水氯化铝;
溶液可得纯净的无水氯化铝;
②在苯酚溶液中滴入少量稀溴水溶液中立即出现白色沉淀。
③无法用分液漏斗将甘油和水的混合液体分离;
④用酸式滴定管量取20.00mL高锰酸钾酸性溶液;
⑤为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比;
⑥苯与溴水在铁粉的催化作用下制备溴苯:
16.以Fe为阳极,石墨棒为阴极,对足量的Na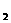 SO
SO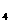 溶液进行电解,一段时间后得到1mol Fe(OH)
溶液进行电解,一段时间后得到1mol Fe(OH) 沉淀,此间共消耗水的物质的量为:
沉淀,此间共消耗水的物质的量为:
A.1.5mol B.2mol C.2.5mol D.3mol
15.下列关于晶体的说法一定正确的是:
A.金属晶体的熔点都比离子晶体的熔点低
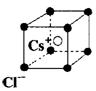
B.氯化铯晶体中每个Cs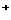 周围与其距离最近的Cs
周围与其距离最近的Cs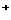 有6个(晶体结构如右图)
有6个(晶体结构如右图)
C.石墨晶体中每个碳原子与4个碳原子以共价键相结合
D.晶体中一定存在着化学键
14.下列关于胶体的认识错误的是:
A.鸡蛋清溶液中加入饱和(NH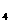 )SO
)SO 溶液生成白色沉淀,属于物理变化
溶液生成白色沉淀,属于物理变化
B.纳米材料微粒直径一般从几纳米到几十纳米(1nm=10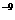 m),因此纳米材料属于胶体
m),因此纳米材料属于胶体
C.往Fe(OH) 胶体中逐滴加入稀硫酸会先产生沉淀而后沉淀逐渐溶解
胶体中逐滴加入稀硫酸会先产生沉淀而后沉淀逐渐溶解
 D.水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
D.水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
13.某溶液中只有NH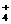 、Cl
、Cl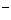 、H
、H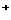 、OH
、OH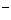 四种离子,且浓度大小的顺序为:c(NH
四种离子,且浓度大小的顺序为:c(NH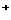 )>c(Cl
)>c(Cl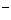 )>c(OH
)>c(OH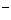 )>c(H
)>c(H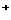 ),该溶液可能是:
),该溶液可能是:
A.由0.01molL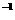 的NH
的NH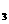 ·H
·H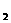 O溶液与0.01mol·L
O溶液与0.01mol·L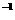 的HCl溶液等体积混合而成
的HCl溶液等体积混合而成
B.由0.01molL 的NH
的NH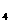 Cl溶液与0.01mol·L
Cl溶液与0.01mol·L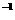 的HCl溶液等体积混合而成
的HCl溶液等体积混合而成
C.由10mL pH=11的NH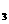 ·H
·H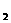 O溶液与1mLpH=3的HCl溶液混合而成
O溶液与1mLpH=3的HCl溶液混合而成
D.由0.01mol·L的NH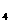 Cl溶液与0.01mol·L
Cl溶液与0.01mol·L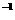 的NH
的NH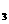 ·H
·H O溶液等体积混合而成
O溶液等体积混合而成
12.心酮胺是治疗冠心病的药物,它具有如下结构简式:
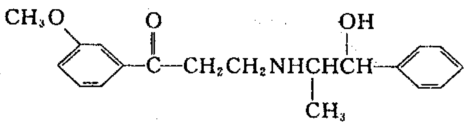
下列关于心酮胺的叙述错误的是:
A.1mol该物质最多可与7molH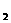 发生加成反应
发生加成反应
B.可以在催化剂作用下和溴反应
C.在碱性条件下可以发生水解反应
D.在一定条件下可以发生酯化反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com