
题目列表(包括答案和解析)
5.X、Y、Z三种元素的原子序数相连,元素X易获得电子成为稳定的离子,元素Z
易失去电子成为稳定的离子。下列说法中,不正确的是 ( )
A.Y原子中电子数较X原子多一个,但比Z原子少一个
B.Y单质和Z、X的单质均可以反应
C.元素Z为活泼的金属,其单质跟水反应放出氢气,生成物的水溶液显碱性
D.X原子与氢反应能形成HX
4.已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨)+O2(g)====CO2(g) △H= -393.51kJ•mol-1
C(金刚石)+O2(g)====CO2(g) △H= -395.41kJ•mol-1
据此判断,下列说法正确的是 ( )
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石高
3.已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少
量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是 ( )
A.上述实验证明还原性:MnO-4>Cl2>Fe3+>I2 B.上述实验中,共有两个氧化还原反应 C.实验①生成的气体能使湿润的淀粉KI试纸变蓝 D.实验②证明Fe2+既有氧化性又有还原性
2.下列各项中的表达正确的是 ( )
A.含1个中子的氦原子为:12He B.乙醛的结构简式为:CH3COH


C.H2O的结构式为:H-O-H D.CH4的分子模型示意图为:
1.化学与生活、生产有着密切的联系,下列说法正确的是 ( )
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” B.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源
C.凡含有食品添加剂的食物对人体健康均有害,不宜食用
D.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水
24、称取金属钠、铝、铁、各m g,在室温下分别与V L 4 mol·L-1的盐酸充分反应,试讨论在下列三种情况下,V值的取值范围(用含m的表达式表示)。
(1)铝与盐酸反应放出的H2最多:
(2)钠与盐酸反应放出的H2最多:
(3)铝与铁分别与盐酸反应,放出的H2一样多: 。
23、A、B、C、D是四种原子序数小于18的主族元素:(1)A原子的电子层数等于最外层电子数,(2)A与B处于同一周期,B与D可形成离子化合物的D2B,该化合物的水溶液呈碱性,(3)C的离子核内质子数与核外电子数之和为18,(4)A、C、D三种元素的离子具有相同的电子层排布。推断A-D各为何种元素,并填空:
(1)A B C D (均填元素符号)
(2)四种元素的离子半径由大到小的顺序为:
(3)用离子方程式表示D2B水溶液呈碱性的原因: 。
22、2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,恢复到常温常压时这种高聚物就变得极不稳定。 在这种高聚氮中氮原子间以共价单键相结合,N-N单键的键能为160 kJ/mol (N2的N≡N键能为942 kJ/mol),晶体结构如图所示。请仔细观察右图,回答下列问题:
(1)在这种晶体中,每个氮原子与 个氮原子结合;
(2)按键型分类时,该固体属于 晶体。
(3)这种固体的可能潜在应用是
,
这是因为: 。
21、乙硼烷(B2H6)是一种气态高能燃料。0.3 mol B2H6在氧气中充分燃烧,生成固态三氧化二硼和液态水,放出649.5 KJ热量,其热化学方程式为:
。
又已知:H2O(l)=H2O(g);△H =+44 KJ·mol-1,则11.2 L(标准状况)B2H6完全燃烧生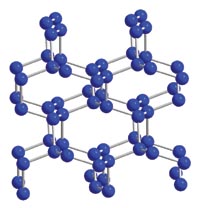 成气态水时放出的热量是
KJ。
成气态水时放出的热量是
KJ。
20、某固体A在一定温度下分解生成固体B、气体C和气体D,A(s)=B(s)+C(g)+4D(g),若测得生成的气体的质量是同温同压下相同体积氢气质量的10倍,且当所生成气体在标准状况下的体积约为22.4 L时,所得B的质量为30.4 g,则A的摩尔质量是( )
A、130.4 g·mol-1 B、50.4 g·mol-1 C、182.4 g·mol-1 D、252 g·mol-1
第Ⅱ卷 (非选择题 共40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com