
题目列表(包括答案和解析)
28.(12分) 已知 (注:R,R’为烃基)
A为有机合成中间体,在一定条件下发生消去反应,可能得到两种互为同分异构体的产物,其
中的一种B可用于制取合成树脂、染料等多种化工产品。A能发生如下图所示的变化。
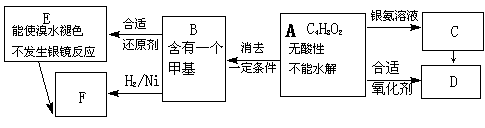
试回答
(1)写出符合下述条件A的同分异构体结构简式(各任写一种):
a.具有酸性______________________b.能发生水解反应______________________
(2)A分子中的官能团是 。
(3) D的结构简式是 ,该分子中含有 个手性碳。
(4)C→D的反应类型是___________,E→F的反应类型是___________
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
(5)写出化学方程式:A→B____________________________________________。
(6)写出E生成高聚物的化学方程式:____________________________________________。
(7)C的同分异构体C1与C有相同官能团,两分子C1脱去两分子水形成含有六元环的C2,写出C2的
结构简式:___________________________;该分子内的碳原子成键时有 种杂化类型。
高三模拟测试题(1)
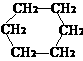
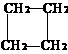
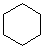
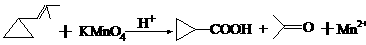
27. (8分)环丙烷可作为全身麻醉剂,环已烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某此有机化合物的反应式(其中Pt、Ni是催化剂)。
|
结构简式 |
 |
 |
Br-CH2-CH2-CH(CH3)-CH2-Br |
|
键线式 |
 |
 |
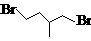 |
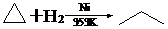 ①
①
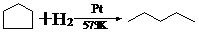
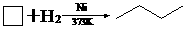 ②
②
 ③
③
④
回答下列问题:
.... ⑴环烷烃与相同碳原子数的 是同分异构体。
.... ⑵从反应①-③可以看出,最容易发生开环加成反应的环烷烃是 (填名称)。
判断依据为 。
.... ⑶环烷烃还可以与卤素单质,卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反
应,其化学方程式为 (用键线式表示,不需注明反应条件)。
.... ⑷写出鉴别环丙烷和丙烯的一种方法。试剂 ;现象与结论
。

26.(10分)若不上慎发生砒霜泄露,应急的措施是采用石灰中和,使被污染的河水含砷量降低到
国家允许的标准范围内,以消除可能造成的危害。 测定砷的含量是利用下述反应:
AsO33-+I2+H2O AsO43-+2I-+2H+
AsO43-+2I-+2H+
此反应为可逆反应,控制溶液的酸碱性,可以测定不同价态(+3或+5)的砷;调节溶液pH值,可以使平衡明显朝正反应方向移动,也可以明显朝逆反应方向移动。
(1)由此可知,AsO33-和AsO43-中,增大pH值, 的还原性增强;降低pH值, 的氧化性增强。
(2)要使反应顺利朝正反应方向进行,pH值不能太大,原因是 。
(3)今有一试样,含As2O3和As2O5及其对测定没有影响的杂质,将此试样用NaOH溶液溶解后,在中性溶液中用0.0200 mol·L-1的I2-KI溶液滴定,用去25.00mL。滴定完毕后,使溶液呈酸性,加入过量的KI。由此析出的碘又用0.125 mol·L-1的Na2S2O3溶液滴定,用去24.00mL。试计算试样中的质量:As2O3 g,As2O5 g。(已知2Na2S2O3+ I2 = Na2S4O6 +2NaI)
25. (9分)为了预防碘缺乏症,国家规定每千克食盐中应含40-50mg碘酸钾。碘酸钾晶体有较高的稳定性,但在酸性溶液中,碘酸钾是一种较强的氧化剂,能跟某些还原剂作用生成碘;在碱
性溶液中,碘酸钾能被氯气、次氯酸等强氧化剂氧化为更高价的碘的含氧酸盐。
工业生产碘酸钾的流程如下:
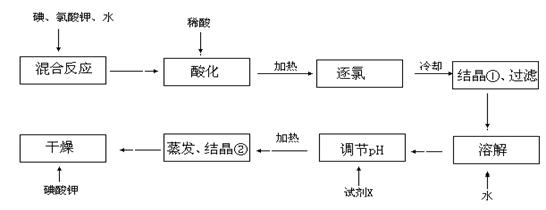
 (1)碘、氯酸钾和水混合后的反应为:I2+ KClO3
+ H2O KH(IO3)2 + KCl+ Cl2↑。已知反应时,两种还原产物所得电子数目相同,请配平该反应的化学方程式:
(1)碘、氯酸钾和水混合后的反应为:I2+ KClO3
+ H2O KH(IO3)2 + KCl+ Cl2↑。已知反应时,两种还原产物所得电子数目相同,请配平该反应的化学方程式:
。
(2)混合反应后,用稀酸酸化的作用是
(3)X的化学式为 ;写出用试剂X调节pH的化学方程式
(4)生产中,如果省去“酸化”、“逐氯”、“结晶①、过滤”这三步操作,直接用试剂X调整反应后溶液的pH,对生产碘酸钾的影响是 。
24. (8分)在元素周期表中,锌(30Zn)、镉(48Cd)、汞(80Hg)同属于锌族,锌和汞在自然界中
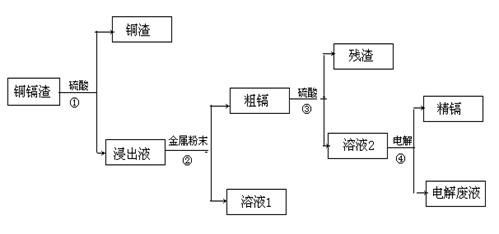
常共生,镉的金属活动性介于锌和汞之间。湿法炼锌过程中产生的铜镉渣中含有Cu、Cd、Zn等多种金属,可用于生产金属镉。镉的主要用途可以用作镍-镉电池,以及用于颜料生产,镉化合物还在PVC稳定剂、发光材料、半导体材料、杀菌剂等方面有广泛的应用。镉的生产流程如图示意如下:
请回答下列问题:
(1)镉元素的核外电子排布式为 ;周期表中第 周期,第 族。
(2)写出步骤①反应的离子方程式 。
(3)步骤②所加入的金属的名称是 。
(4)步骤④用“溶液2”作电解液,镉在 极析出,该电极材料是
(5)“电解废液”中含有镉,不能直接作为污水排放。目前含镉的废水处理的方式有两种,一种是在含镉污水中加入硫化钠,沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝,沉淀镉离子。写出硫化钠沉淀镉离子的离子方程式 。
23.(13分)已知FeS0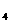 在高温下分解生成Fe
在高温下分解生成Fe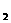 O
O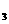 、S0
、S0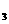 和SO
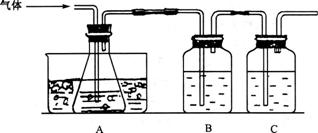
和SO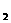 。某研究性学习小组先用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeS0
。某研究性学习小组先用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeS0 的质量。
的质量。
请回答下列问题:
(1)实验时,A瓶的作用是检验测定生成的S0 气体,A瓶内盛水,水中滴有数滴 溶液,B瓶内盛品红试液,C瓶内盛NaOH溶液,NaOH溶液的作用是___________________________________。
气体,A瓶内盛水,水中滴有数滴 溶液,B瓶内盛品红试液,C瓶内盛NaOH溶液,NaOH溶液的作用是___________________________________。
(2)A瓶内所盛试剂的作用是___________ __,A瓶要用冰水冷却的原因是_________________________________________________________________。
(3)检验后,用A瓶内的混合物测定FeS0 已分解的质量,此实验操作的第一步是(简述操作步骤)____________________________________________________________。
已分解的质量,此实验操作的第一步是(简述操作步骤)____________________________________________________________。
(4)测定过程中,在过滤器上将沉淀洗净后,将沉淀灼烧并冷却至室温,称量其质量为a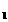 g,再次灼烧冷却至室温称量其质量为a
g,再次灼烧冷却至室温称量其质量为a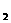 g,且a
g,且a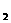 <a
<a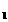 ,接下来的操作应当是
,接下来的操作应当是
________________________________________________ 。
(5)已经分解的FeS0 的质量是___________
_(沉淀质量用a表示,填计算式)。
的质量是___________
_(沉淀质量用a表示,填计算式)。
22.(12分)下图为研究苯和溴的取代反应的实验装置图。其中A试管下端开了一个小孔,塞好石棉绒,再加入适量的铁屑。

(1)向A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。有关A中反应的化学方程式为:
①
②
(2)试管C中苯的作用是 。
反应开始后,观察D和E两试管,D可以看到的现象是 ;
E可以看到的现象是 。
反应2-3min后,装置B中观察到的现象是 。
(3)在实验的整套装置中,具有防倒吸的装置有 (填字母代号)。
(4)该套实验装置的设计,构思巧妙,科学合理。除了具有操作方便,成功率高,各步现象明显,产物便于观察外,还有一个明显的优点是 。
21.(8分)现有下列仪器或用品:a.铁架台(含铁圈、铁夹) b.锥形瓶 c.滴定管 d.烧杯(若干)
e.玻璃棒 f.胶头滴管 g.托盘天平(含砝码) h.滤纸 i.量筒 j.漏斗 k.温度计
现有下列试剂:A.NaOH固体 B.碳酸钠溶液 C.氯化镁溶液 D.蒸馏水
 试填空:
试填空:
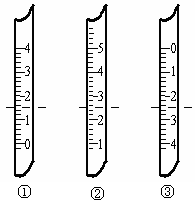
①如图分别是温度计、量筒、滴定管的一部分,
下述判断及读数(虚线刻度)不正确的是_______
A.①是量筒,读数为1.5mL
B.②是量筒,读数为2.5mL
C.③是滴定管,读数为2.50mL
D.②是温度计,读数是2.5℃
②用氢氧化钠配制一定物质的量浓度的氢氧化钠溶液时,还缺少的仪器是 。
③除去Mg(OH)2中混有的少量Ca(OH)2:可以用的试剂是: (选填序号),操作方法是滴加试剂、_______、洗涤。
④完成③,上述仪器或用品用到的有 (从上述仪器或用品中选择,并填上相应序号) 。
20. 某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿佛加德罗常数,下列说法中正确的是( )
A、氧元素的相对原子质量为12a/b B、1mol该氧原子的质量为aNAg
C、x g该氧原子所含的电子数为8x/a D、y g 该氧原子的中子数一定为8y/a
19.下列叙述正确的是( )
A. 只要含有金属阳离子的晶体就一定是离子晶体
B.在冰块中,每个水分子中存在2个氢键
C.理论上,所有氧化还原反应均可设计成原电池
D.极性分子中一定含有极性键,非极性分子中不一定含有非极性键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com