
题目列表(包括答案和解析)
7.现有A、B、C、D四种短周期元素,已知A、B同主族,B、C、D同周期,A、B的原子序数之和等于C、D的原子序数之和,C的单质能分别跟B和D的最高价氧化物的水化物反应。请回答:
(1)B和C的元素符号分别为______________;
(2)上述四种元素的原子半径由大到小的顺序(用元素符号表示)为_____________;
(3)D单质在A单质中燃烧的产物与二氧化碳反应的化学方程式为___________;
(4)B单质能跟D的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种盐的水溶液均呈碱性,该氧化还原反应的离子方程式为________________
6.有A、B、C、D四种短周期的非金属元素(其单质也可分别用A、B、C、D表示),四种元素的原子序数按B、D、C、A顺序增大,D、C元素在周期表中位置相邻。在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙化合物,C和D化合可得丁。已知乙、丙两个分子中各含有10个电子,并且甲、乙、丙、丁、戊有如下的变化关系:
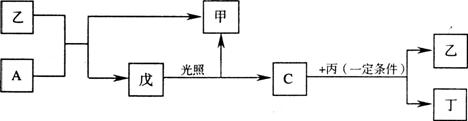
请填写下列空格:
(1)甲的浓溶液与一种黑色粉末共热可得A,则甲为_______,乙为___________。
(2)戊的结构式是______________,DB4+的电子式是_______________。
(3)丙+丁→D在一定条件下反应,是一种治理污染的好办法,写出该反应的化学方程式,并标明电子转移情况:___________________________________
5.下图表示各物质之间的转化关系。已知:常温下D、E、F、I、J为气体,且D、I是水煤气的主要成分;B是无色液体,M为红褐色固体,C的焰色反应为黄色。
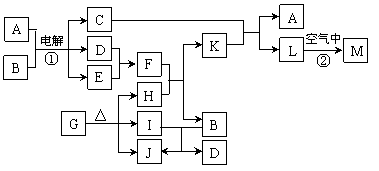 ⑴基于反应①原理的化学工业称为
,写出该反应的化学方程式
。
⑴基于反应①原理的化学工业称为
,写出该反应的化学方程式
。
⑵写出K和E反应的离子方程式_______________________________________。
写出F溶液和H反应的离子方程式___________________________________。
⑶已知:由G分解得到的H、I、J三者的物质的量之比为1∶1∶1,则G的化学式为___
4.以下物质A、B、C、X均属于中学常见的物质,已知它们之间有如下转化关系(其中副产物已被略去,例如H2O等):

请根据上述转化关系回答下列问题:
(1)若X是具有强氧化性的气体单质,且B的分子式是CH2O,则X的化学式是______。
(2)若X是非氧化性强酸,且C是一种酸性氧化物,则C的化学式是______(只写一例)。
(3)若X是金属单质,请写出反应②的离子方程式:____________________。
(4)若X是强碱,且A、B、C都含有同一种金属元素,请写出反应②的离子方程式:__________
3.已知A是一种由短周期元素组成的盐,H是引起温室效应的主要气体之一,Y是一种常见液体,E的相对分子质量比D大16,L、K均为白色沉淀,且K光照后无变化。它们存在如下转化关系(反应条件及部分产物已略去):
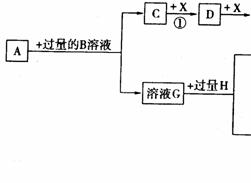
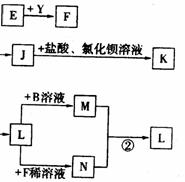
请回答下列问题:
⑴A的化学式是___________,Y的电子式是__________。
⑵反应①的化学方程式是____________________________。
⑶反应②的离子方程式是____________________________。
⑷将L加热后得到的固体在熔融条件下电解的化学方程式是________ ____
2. A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是电子层数的2倍;C的最高价氧化物对应的水化物与其氢化物反应生成一种盐x;E与A同主族;A、B、C这三种元素,每一种与D都能形成元素的原子个数比不相同的若干种化合物。
(1)写出元素的名称:C__________________ E______________________
(2)画出D的原子结构示意图____________________________
(3)B的最高价氧化物的电子式是____________________________
(4)盐X的水溶液显_________(填酸、碱或中性),其原因是_____ _______________(用离子方程式说明)。
1、A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:
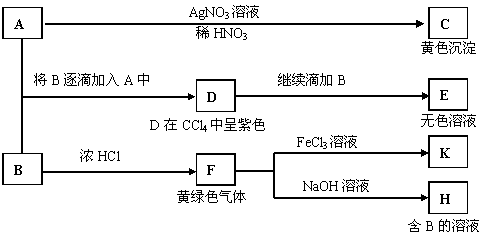
请回答:
(1)写出A、B和C的化学式:A ,B ,C 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
, 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式:
13.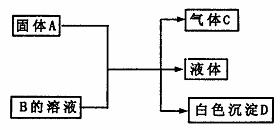 A、B、C、D、均为中学化学常见的物质,它们间的反应关系如下图所示。
A、B、C、D、均为中学化学常见的物质,它们间的反应关系如下图所示。
(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式 。有关反应的化学方程式为 。
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液。
①A是NaHCO3时,该反应的离子方程式为: 。
②A是一种淡黄色固体,且A与B以物质的量之比为2:1相混合时,推知B的化学式为 。
(3)若A是碳化钙(CaC2),A与B的溶液反应时只生成气体C、CaCO3和水;C的燃烧热为1300kJ·mol-1,则B的化学式为 ;C燃烧的热化学方程式为
12.A、B、C、D均为短周期主族元素,A、C、D在不同周期,A和C同主族,B、C同周期,A、B、C三种元素的原子序数之和为37,且B元素的最外层电子数与其电子层数相同,则:
(1)D元素的名称为 。
(2)写出元素A、D形成的化合物D2A的电子式 ,其熔点比D2C的熔点 (用“高”或“低”填写),理由是 。
(3)A、B、C三种元素所形成的常见化合物溶于水呈酸性,用离子方程式表示其原因 。
(4)A、B、C、D四种元素的原子半径从小到大的顺序为(用元素符号表示)
11. A、B、C、D、E均为短周期元素,且原子序数逐渐增大。A、D同主族,A与B的质子数之和等于C的质子数,A+离子与C2-离子的核外电子数之和等于D+离子的核外电子数,B原子与D+离子的核外电子数之和等于 E原子的核外电子数。
(1)A、B、C、D、E的元素符号分别为 。
(2)D、E元素可组成化合物甲,电解甲的水溶液时,反应的离子方程式为 ;A、C元素可组成原子个数比为1:1的化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为 。
(3)A、B、C、E中的任意三种元素可组成多种化合物,其中既含离了键又含共价键,且水溶液呈酸性的化合物有(写出两种化合物) 。
(4)A、C、D、E中的任意三种元素可组成多种化合物,其中溶于水时能抑制水电离的化合物有(各写一种不同类别的化合物) ,它们能抑制水电离的理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com