
题目列表(包括答案和解析)
22、酸雨主要是燃烧含硫的燃料引起的,现有一份雨水样品,每隔一定时间对它的PH值测定一次。
①雨水样品的pH变化的原因是(用化学方程式表示) ;
②如果将刚取样的上述雨水与自来水相混合,pH将变 ,原因是(用化学方程式表示) 。
③为防治酸雨,降低煤燃烧时向大气排放的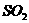 ,工业上将生石灰和含硫煤混合后使用,请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式:
,工业上将生石灰和含硫煤混合后使用,请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式:
, 。
21.已知A-L所代表的物质(或溶液中的溶质)都是中学化学里常见的物质。通常状况下,A、B均是淡黄色固体,D是气体单质,E是无色无味气体,K是不溶于水的酸。反应①-③是化学工业生产重要产品的全部反应,反应④是工业生产普通玻璃的反应之一。一定条件下,各物质间的相互转化关系如下图所示(反应时加入或生成的水均没标出)。
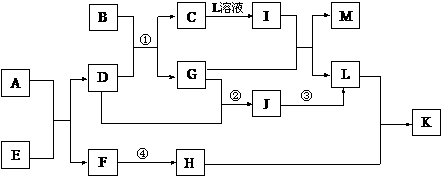
请填写下列空白:
(1)写出下列物质的化学式:H_________;D的同素异形体__________。(均填化学式)
(2)画出A中金属元素的原子结构示意图_____________;指出E分子中共价键的类型(填“极性键”或“非极性键”)____________。
(3)指出反应①②③是吸热反应,还是放热反应?____________。
(4)完成下列反应方程式:① I+G→M+L的离子方程式:_______________________________。
② 写出反应④的化学方程式:_____________________________________。
|
测试时间(小时) |
0 |
1 |
2 |
4 |
8 |
|
雨水 PH |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
20.有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物;B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物。
⑴写出只含有A、B、D、E四种元素的两种无水盐的化学 式 、 。
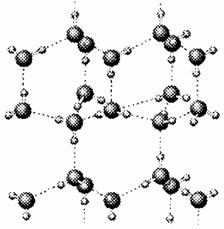
⑵右图是A与D形成的一种化合物的晶体结构示意图,其
中的虚线表示 ,与每个“构成粒子”相邻的粒子呈 空间构型。E与D按原子个数比1﹕1形成的化合物的电子式为 。
⑶人们通常把拆开l mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
|
化学键 |
F-D |
F-F |
B-B |
F-B |
C═D |
D═D |
|
键能/kJ·mol-1 |
460 |
176 |
347.7 |
347 |
745 |
497.3 |
①下列三种物质形成的晶体,熔点由高到低的顺序(用a、b、c表示):
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
②试估算F单质晶体的燃烧热:___________________________________________。
19、某同学运用已有的Na2O2和CO2反应的知识进行迁移,认为Na2O2也可和SO2反应,反应式可能为:2 Na2O2+2SO2=2Na2SO3+O2,为此设计如下一套装置,来验证Na2O2和SO2的反应产物。如图安装仪器,检查装置气密性后添加药品并滴入适量浓硫酸。回答下列问题:
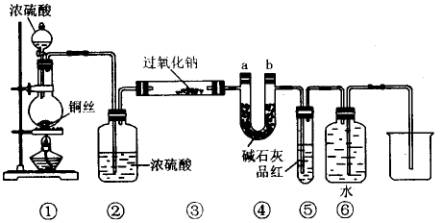
 (1)点燃①处酒精灯,不久,观察到①处产生大量气体;
③处两通管管壁发热,管内药品的颜色变化为:____________色逐渐变为__________色。
(2)在反应过程中如何用较简便的操作证明反应产生了O2?___________________。
(3)⑥处用排水法收集气体,从什么现象可证明收集的气体中已不含SO2?
。
(4)待反应结束后,取两通管内少量固体,装入试管中,加水溶解时未产生气体,如何证明产物中有Na2SO3?
。
(5)待反应结束后,取两通管内少量固体,装入试管中,加入足量盐酸溶液,再加入氯化钡溶液,有白色沉淀生成,试分析产生沉淀的原因。___________________________。
(1)点燃①处酒精灯,不久,观察到①处产生大量气体;
③处两通管管壁发热,管内药品的颜色变化为:____________色逐渐变为__________色。
(2)在反应过程中如何用较简便的操作证明反应产生了O2?___________________。
(3)⑥处用排水法收集气体,从什么现象可证明收集的气体中已不含SO2?
。
(4)待反应结束后,取两通管内少量固体,装入试管中,加水溶解时未产生气体,如何证明产物中有Na2SO3?
。
(5)待反应结束后,取两通管内少量固体,装入试管中,加入足量盐酸溶液,再加入氯化钡溶液,有白色沉淀生成,试分析产生沉淀的原因。___________________________。
18.碱式氯化铜(不溶于水的绿色结晶)是一种农药,分子式:CuCl2·3Cu(OH)2·XH2O
(X=1/2,1,2)为验证其组成并确定X值,某学生设计了以下几步实验。
① 取a g的晶体制成粉末。
② 晶体加热至确认质量不再变化为止(铜仍为二价),冷却后称其质量为b g。
③ 另取a g的晶体,溶于足量某溶剂中充分溶解得到溶液。
④ 向③得到的溶液中加入足量的硝酸银溶液,最后得到纯净固体称量为c g。
若以上操作均正确,试回答下列问题:
A.将晶体制成粉末,所用的主要化学仪器 (填仪器名称,下同);灼烧晶体时是在 中进行。以上四步中,用到玻璃棒的步骤有 (选填:①②③④)
B.步骤②灼烧后得到的固体应为:
C.步骤③所用的溶剂可能是
D.步骤④主要包括:加入足量硝酸银溶液→ → → 晾干→称量
E.若组成符合通式,则计算X的表达式为: (用字母表示)。
17.实验室制取氯气的方法有多种,下列所列物质是制取氯气的某一反应的部分反应物和生成物:HCl、K2Cr2O7、CrCl3、H2O请根据可能的反应原理,完成正确的化学方程式,并用单键头表示电子转移的情况,同时指出反应中的氧化剂和氧化产物。
氧化剂: 氧化产物:
16.在四个密闭容器中分别装有下表所示的一定量的物质,将它们加热至300oC,经充分反应后排出气体,则残留固体及其物质的量正确的是( )
|
|
A |
B |
C |
D |
|
反应前 |
1molNaOH、1molNaHCO3 |
1molNa2O、1molNaHCO3 |
1mo1Na2O2、lmolNaHCO3 |
1molNa2O2、1molNH4HCO3 |
|
反应后 |
1molNa2CO3 |
2molNaOH、0.5molNa2CO3 |
2molNaOH、0.5molNa2CO3 |
1molNa2CO3 |
班级 姓名 学号 得分
15.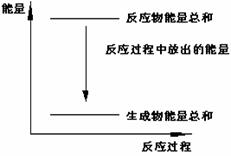 对于Zn(s)+H2SO4(l)==ZnSO4(l)+H2(g);ΔH
<0 的化学反应下列叙述不正确的是
对于Zn(s)+H2SO4(l)==ZnSO4(l)+H2(g);ΔH
<0 的化学反应下列叙述不正确的是
A.反应过程中能量关系可用右图表示
B.ΔH的值与反应方程式的计量系数有关
C.若将该反应设计成原电池锌为负极
D.若将其设计为原电池当有32.5g锌溶解时, 正极放出气体一定为11.2L
14.下列有关说法正确的是
A.物质熔沸点的高低顺序是:晶体硅>氯化钠>干冰>汞
B.分子晶体中一定存在分子间作用力 C.水是一种非常稳定的化合物,这是由于氢键所致
D.CO2、HClO、CF4、PCl3四种物质分子中的所有原子都满足最外层为8电子的稳定结构
13.下列离子方程式正确的是
A. 用铂作电极电解MgCl2溶液: 2Cl-+2H2O H2↑+Cl2↑+2OH-
用铂作电极电解MgCl2溶液: 2Cl-+2H2O H2↑+Cl2↑+2OH-
B.向次氯酸钙溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO
C.向硫酸氢钠溶液中滴加氢氧化钡至中性:2H++SO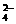 +Ba2++2OH-==BaSO4↓+2H2O
+Ba2++2OH-==BaSO4↓+2H2O
D.将氢氧化铁粉末加入氢碘酸中:Fe(OH)3+3H+→Fe3++3H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com