
题目列表(包括答案和解析)
2. 下列各组物质的分类正确的是
A.同位素: H2 D2 T2
B.非电解质: NH3、C2H5OH
C.非极性分子:C60、CO2、CH2Cl2
D.同系物:  -OH、CH3-
-OH、CH3- -OH、CH3-
-OH、CH3- -CH2OH
-CH2OH
1. 下列分子中所有原子都满足最外层8电子结构的是
A.N2 B.H2O C.BF3 D.SF6
25.(12分)用沉淀法测定NaHCO3和K2CO3混合物的组成。实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,每次实验均充分反应。实验记录见下表:
|
实验次数 |
样品的质量(g) |
Ba(OH)2溶液体积(L) |
生成沉淀质量(g) |
|
1 |
0.858 |
0.5 |
1.379 |
|
2 |
1.716 |
0.5 |
|
|
3 |
2.574 |
0.5 |
4.137 |
|
4 |
3.432 |
0.5 |
5.516 |
|
5 |
4.290 |
0.5 |
5.516 |
|
6 |
5.148 |
0.5 |
5.516 |
回答下列问题:
⑴第2次实验中产生沉淀质量是多少克?
⑵样品中NaHCO3和K2CO3的物质的量之比为多少?
⑶室温下,取第3组实验所得溶液体积的1/10,加水配成500mL溶液,计算稀释以后溶液的pH?
24.(6分)将97.5g锌投入100mL 18.5mol/L浓硫酸中充分反应,锌完全溶解,生成的混合气体中SO2和H2的体积比为1∶4。求:
⑴生成的混合气体在标准状况下的体积?
⑵室温下,若将反应后的溶液加水稀释至1L,则所得溶液溶质的物质的量浓度为多少?
23.(6分)某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种组成,取该溶液进行如下实验:
(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(B)在(A)所得溶液中再加入过量碳酸氢铵溶液。有气体生成;同时析出白色沉淀甲;
(c)在(B)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是_______________________________________;
(2)一定存在的离子是_______________________________________________;
(3)判断沉淀乙成份的方法是_________________________________________。
22.(6分)氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定。工业上曾普遍采用高纯硅与纯氮在1300℃反应获得。
(1)氮化硅晶体属于__________晶体(填晶体类型)。
(2)已知氮化硅的晶体结构中,原子都以单键相连,且N原子和N原子、Si原子和Si原子不直接相连,同时每个原子都满足8电子稳定结构。请写出氮化硅的化学式___________。
(3)现用四氯化硅和氮气在氢气气氛保护下,加强热反应发生,可得较高纯度的氮化硅。反应的化学方程式为__________ __________。
21.(8分)“绿色试剂”双氧水可作为矿业废液消毒剂,如要消除采矿业废液中的氰化物(如KCN),化学方程式为:KCN+H2O2+H2O=A+NH3↑
(1)生成物A的化学式为 。
(2)状况下有0.448L氨气生成,则转移的电子数为 。
(3)反应中被氧化的元素为 。
(4)H2O2被称为绿色氧化剂的理由是 。
20.(12分)A、B、C、D四种元素都是短周期元素。A元素的离子焰色反应时火焰呈黄色。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL 2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构最外层电子数是次外层电子数的三倍。根据条件,回答:
(1)C元素在元素周期表中的位置是 ,它的最高价氧化物的化学式为 。
(2)C与B元素形成化合物的晶体类型是______________。
(3)A与D形成稳定化合物的电子式为______________,判断该化合物在空气是否变质的简易方法是 。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为 。
19.(10分)下图中每个方框表示有关的一种反应物或生成物,方框中字母是物质代号。
已知:B、D、E、F、X均为单质。一定条件下,各物质可发生如下图所示的变化:
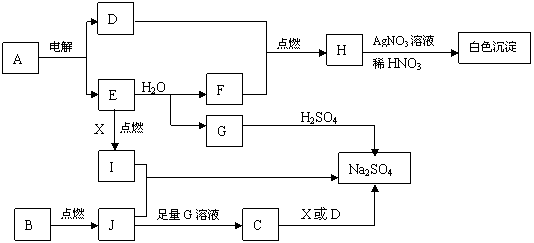
⑴写出A、B的化学式:A , B ;
⑵写出I和J反应的化学方程式 ;
⑶写出C溶液和D反应的离子方程式 ;
写出C溶液和X反应的离子方程式 。
18.(12分)工业纯碱中含有少量NaCl杂质,实验室利用下图装置通过纯碱与酸反应产生CO2的量测定工业纯碱中Na2CO3的质量分数。
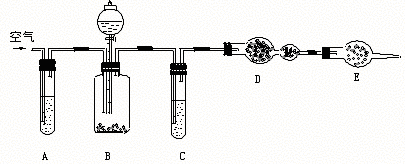
可供选择的试剂:
稀H2SO4,稀盐酸,NaOH溶液,浓硫酸,碱石灰,纯碱试样
(1)从B中反应开始到反应结束,要缓缓鼓入空气,其作用是 。
A中盛放的试剂是 。
(2)装置B中分液漏斗盛放的酸是 。B中反应的离子方程式是 。
(3)装置C中盛放的试剂是 ,装置E的作用是 。
(4)实验操作时,必须测定记录的数据是(用文字说明,需注明“反应前”或“反应后”,可不填满,也可补充)
① ② ③ ④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com