
题目列表(包括答案和解析)
23.(11分)我国“神舟”五号、六号载人飞船的成功发射,标志着“炎黄子孙千年飞天梦想实现了,中国人的太空时代开始了。” ⑴ 火箭升空时,由于与大气层的剧烈摩擦,产生高温。为了防止火箭温度过高, 在火箭表面涂上一种特殊的涂料,该涂料的性质最可能的是
A.在高温下不融化 B.在高温下可分解气化 C.在常温下就分解气化 D.该涂料不可能发生分解 ⑵ 火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,其反应的方程式是: N2 O4 + N2H4 → N2 + H2O 。请配平该反应方程式: N2O4 + N2H4 ===== N2 + H2O 该反应中被氧化的原子与被还原的原子物质的量之比是 。 这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。 ⑶ 为了向宇航员提供氧气,飞船上有专门的供氧装置。现有供氧剂过氧化钠与超氧化钾(KO2)。① 写出它们与二氧化碳反应的化学方程式(超氧化钾与二氧化碳的反应产物与过氧化钠类似): ________ ;
_____________________________________。 ② 你选择的供氧剂是: ____ ,原因是: ________________ 。
22.在含有1mol KAl(SO4)2的溶液中逐滴加入2mol Ba(OH)2
溶液,下列有关说法中正确的是
A.先生成沉淀,后沉淀全部溶解
B.当溶液中Al3+、SO42-全部沉淀出来时,沉淀的总物质的量最大
C.最后得到的沉淀是BaSO4
D.最后的沉淀为2mol BaSO4、1mol Al(OH)3
21.在一恒容的容器中充入2molA和1molB发生反应2A(气)+B(气)===XC(气),达到平衡后,C的体积分数为W%。若维持容器中的容积和温度不变,按起始物质的量:A为 0.6mol,B为0.3mol,C为1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则X值为
A.只能为2 B.只能为3 C.可能是2,也可能是3 D.无法确定
20..常温下经测定某溶液中离子只有Na+、Ac-、H+、OH―四种,且离子浓度大小的排列顺序为:c(Ac-)>c(Na+)>c(H+)>c(OH―)。其可能的情形是
A、该溶液由pH=3的HAc与pH=11的NaOH溶液等体积混合而成
B、0.2mol/L的HAc溶液与0.1mol/L的NaOH溶液等体积混合
C、在上述溶液中加入适量NaOH,可能使溶液中离子浓度大小改变为:
c(Ac-)>c(Na+) >c(OH-) >c(H+)
D、该溶液由0.1mol/L的HAc溶液与等物质的量浓度等体积的NaOH溶液混合而成
19.下列反应的离子方程式错误的是
A.等物质的量的Ba(OH)2与NH4HSO4在溶液中反应:
Ba2++2OH-+NH4++H++SO42-==BaSO4↓+NH3·H2O+H2O
B.碳酸钡溶于醋酸溶液BaCO3+2H+ ===Ba2++CO2↑+H2O
C.金属钠与饱和食盐水:Na+2H2O===Na++2OH-+H2↑
D.向碳酸氢钠溶液中滴入过量澄清石灰水:
Ca2++OH-+HCO3-====CaCO3↓+H2O
18.下列各种溶液中,能大量共存的离子组是
A.pH=1的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+
B.[H+]=10-14mol·L-1 的溶液中:Na+,AlO2- ,S2-,SO42-
C.pH=3的溶液中:Mg2+,Fe3+,Cu2+,SO42-
D.使紫色石蕊试液变红色的溶液中:K+,Na+,Ca2+,HCO3-
17.“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是
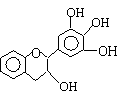 A、分子中所有的原子共一平面
A、分子中所有的原子共一平面
B、1molEGC与4molNaOH恰好完全反应
C、易发生氧化反应和取代反应,难发生加成反应
D、遇FeCl3溶液不发生显色反应
16.PH值和体积都相等的盐酸、硫酸和醋酸三种溶液分别与足量的小苏打反应,下列有关叙述正确的是
A.硫酸与小苏打反应最剧烈 B.相同条件下,三者产生的气体体积相同
C.醋酸与小苏打反应放出的气体最多 D.盐 酸、醋 酸 与小苏 打反应产生的气体体积相同
15. 在容积固定的密闭容器中存在如下反应:A(g)+3B(g)
2C(g)+Q (Q﹥0),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是
在容积固定的密闭容器中存在如下反应:A(g)+3B(g)
2C(g)+Q (Q﹥0),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是
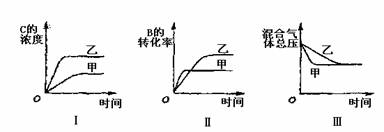
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图I研究的是压强对反应的影响,且乙的压强较高
C.图II研究的是温度对反应的影响,且甲的温度较高
D.图III研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
14.运用元素周期律分析下面的推断。其中错误的是
A.已知Ra是第七周期、IIA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强
B.已知As是第四周期、VA族的元素,故AsH3的稳定比NH3的稳定性强
C.已知Cs的原子半径比Na的大,故Cs与水反应比Na与水反应更剧烈
D.已知Cl的核电荷数比Al的核电荷数大,故 Cl的原子半径比Al的原子半径小
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com